預(yù)測HCC放射敏感性的新生物標(biāo)志物發(fā)現(xiàn)!還與鐵死亡相關(guān)!
放射耐藥性是肝細(xì)胞癌(HCC)放療失敗的罪魁禍?zhǔn)住CC中放射耐藥的調(diào)控基因和潛在機(jī)制的見解有待深入研究。本研究通過RNA-seq和生物信息學(xué)分析篩選出細(xì)胞因子信號傳導(dǎo)抑制因子2(SOCS2)作為HCC放療的潛在預(yù)后預(yù)測因子,隨后確定其在體內(nèi)或體外促進(jìn)HCC的放射敏感性。同時(shí),測定溶質(zhì)載體家族7成員11(SLC7A11)和谷胱甘肽過氧化物酶4(GPX4)的鐵死亡負(fù)調(diào)節(jié)蛋白、細(xì)胞內(nèi)脂質(zhì)過氧化和Fe2+濃度表明,高水平的鐵死亡有助于HCC的放射增敏。此外,SOCS2和SLC7A11在具有不同放射敏感性的HCC臨床組織和腫瘤異種移植腫瘤中表達(dá)相反。在機(jī)制上,SLC7A11的N端結(jié)構(gòu)域被SOCS2的SH2結(jié)構(gòu)域特異性識別。而SOCS162-BOX區(qū)域的L162和C166可以結(jié)合伸長蛋白B/C化合物以共同形成SOCS2/伸長蛋白B/C復(fù)合物以募集泛素分子。本文中,SOCS2作為將附著的泛素轉(zhuǎn)移到SLC7A11的橋梁,促進(jìn)了K48連接的多泛素化降解SLC7A11,最終導(dǎo)致HCC的鐵死亡和放射增敏的發(fā)生。綜上所述,本研究首次證實(shí)高表達(dá)的SOCS2是通過促進(jìn)SLC7A11的泛素化降解和促進(jìn)鐵死亡來預(yù)測HCC放射敏感性的生物標(biāo)志物之一,這表明靶向SOCS2可以提高HCC放療的效率并改善患者的預(yù)后。本文于2023年1月發(fā)表在《Cell death and differentiation》IF:12.4期刊上。
技術(shù)路線
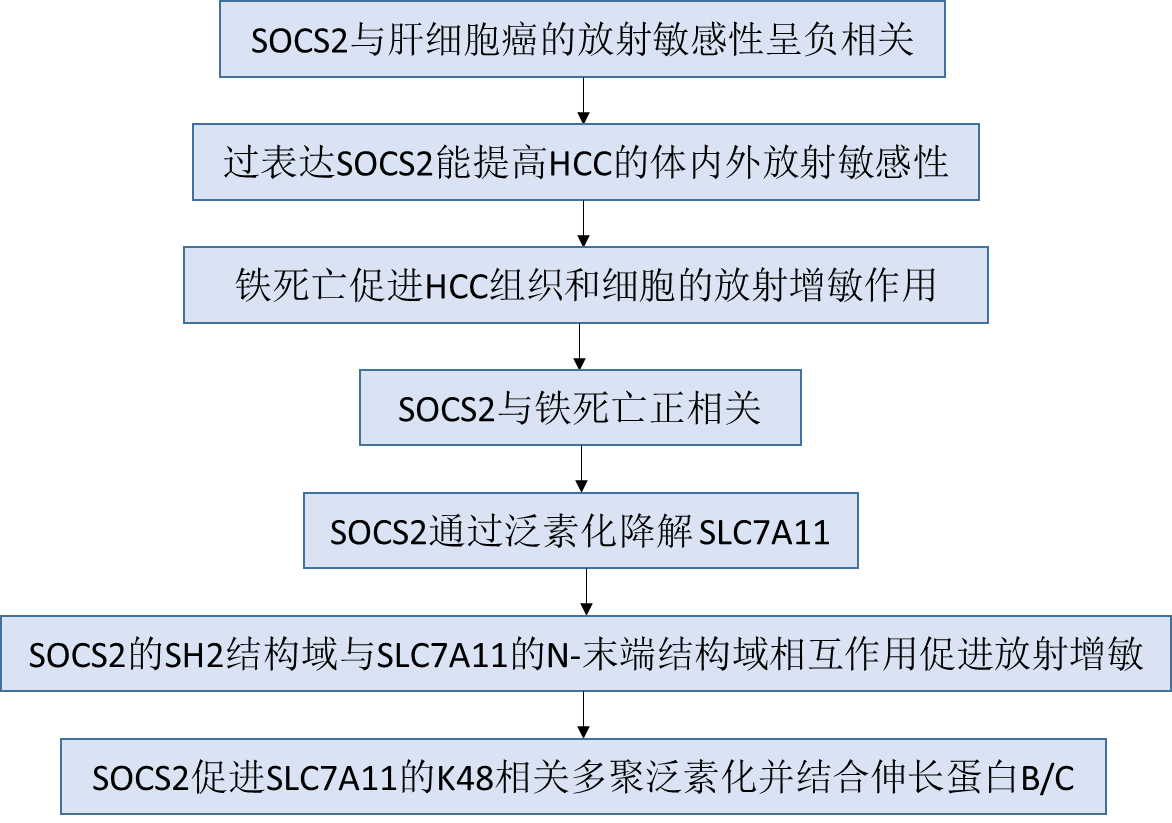
主要實(shí)驗(yàn)結(jié)果
1、SOCS2與肝細(xì)胞癌的放射敏感性呈負(fù)相關(guān)
文章首先由親本HCC細(xì)胞系SK-Hep-1和HepG2構(gòu)建得到兩種放射抗性HCC細(xì)胞系SK-Hep-1R和HepG2R,敏感性增強(qiáng)比(SER)分別為1.18和1.25(圖1A)。為確定參與HCC放射抗性的潛在基因,通過RNA-seq分析探索SK-Hep-1和SK-Hep-1R細(xì)胞之間的差異mRNA譜,鑒定總共255個(gè)mRNA。其中,189個(gè)mRNA上調(diào),66個(gè)mRNA下調(diào)(圖1B)。此外,通過GEPIA和TCGA數(shù)據(jù)庫的分析發(fā)現(xiàn),與正常肝組織相比,HCC組織中有5856個(gè)基因差異表達(dá)(圖1C),包括4282個(gè)上調(diào)基因和1572個(gè)下調(diào)基因。隨后作者根據(jù)GEPIA數(shù)據(jù)庫將上述差異表達(dá)基因(DEGs)與與HCC預(yù)后相關(guān)的存活基因結(jié)合起來,尋找調(diào)節(jié)HCC放射抗性和預(yù)后的DEGs。Venny分析顯示只有兩個(gè)基因,SOCS2和SMOX,在這些數(shù)據(jù)集中同時(shí)下調(diào)或上調(diào)(圖1D)。經(jīng)檢測,與正常組織和SK-Hep-1細(xì)胞相比,HCC組織和放射抗性SK-Hep-1R細(xì)胞中的SOCS2基因顯著降低(圖1E),而根據(jù)GEPIA數(shù)據(jù)庫的Kaplan-Meier總生存期(OS)分析顯示,SOCS2的低表達(dá)是指HCC患者預(yù)后不良(圖1F)。此外,與正常組織和SK-Hep-1細(xì)胞相比,HCC組織和SK-Hep-1R細(xì)胞中SMOX基因增加(圖1E),升高的SMOX表明HCC患者預(yù)后不良。
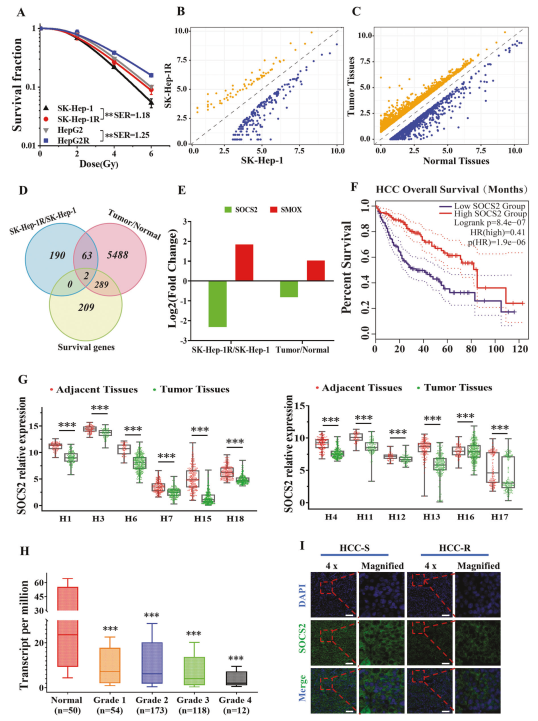
圖1 SOCS2的過表達(dá)與HCC的放射增敏有關(guān)
為進(jìn)一步證明這兩個(gè)基因在肝癌發(fā)生和發(fā)展中的作用,作者應(yīng)用HCCDB數(shù)據(jù)庫進(jìn)行進(jìn)一步的分析。發(fā)現(xiàn)SOCS2在腫瘤組織中的mRNA表達(dá)顯著低于鄰近正常組織(圖1G),表明SOCS2的高表達(dá)抑制HCC的發(fā)生和進(jìn)展。SMOX的HCC調(diào)節(jié)的一致性比SOCS2差,因此后續(xù)研究選用SOCS2作為肝癌放射抗性的潛在基因。此外,與正常肝臟樣本相比,HCC IV期SOCS2表達(dá)水平低于I,II和III期(圖1H),這與低SOCS2表達(dá)患者預(yù)后不良的現(xiàn)象一致。為確定SOCS2是否直接介導(dǎo)放療后HCC的預(yù)后,該研究通過免疫熒光對放射敏感性肝癌患者(HCC-S)和放射抗性肝癌患者(HCC-R)的腫瘤組織中SOCS2的表達(dá)水平進(jìn)行檢測,發(fā)現(xiàn)放射抗性組織的SOCS2表達(dá)較低(圖1I)。總之,這些結(jié)果表明SOCS2可能作為一種抑癌基因來抑制肝癌的進(jìn)展和放射抗性。
2、過表達(dá)SOCS2能提高HCC的體內(nèi)外放射敏感性
接下來,作者檢測SOCS2與肝癌細(xì)胞放射敏感性的關(guān)系。WB分析表明SOCS2在SK-Hep-1,SK-Hep-1R,HepG2和HepG2R細(xì)胞中有序下降(圖2A),與它們的放射敏感性一致(圖1A)。為闡明SOCS2的功能,用lvSOCS2或siSOCS2轉(zhuǎn)染HCC細(xì)胞以有效地增強(qiáng)或減少SOCS2的表達(dá)(圖2B,C)。過表達(dá)SOCS2降低SK-Hep-1和HepG2細(xì)胞的抗輻射能力,SER分別為1.11和1.16(圖2D)。相反,敲除SOCS2增加了HCC細(xì)胞的抗輻射能力,SER分別為0.86和0.89(圖2E)。
為研究是否可以在體內(nèi)觀察到同樣的現(xiàn)象,作者對小鼠進(jìn)行異種移植腫瘤實(shí)驗(yàn),發(fā)現(xiàn)放射(irradiation,IR)會引起腫瘤體積的減少,且在SK-Hep-1中比在SK-Hep-1R細(xì)胞中更明顯(圖2F,H),而過表達(dá)SOCS2會導(dǎo)致IR后腫瘤體積進(jìn)一步減少(圖2G,I)。
由于已有研究表明輻射會誘導(dǎo)鐵死亡,所以作者進(jìn)一步研究鐵死亡是否在腫瘤的放射敏感性中起作用。鐵死亡的特征是細(xì)胞毒性脂質(zhì)過氧化物的積累。鐵死亡及其調(diào)節(jié)蛋白,如谷胱甘肽過氧化物酶4(GPX4)、溶質(zhì)載體家族7成員11(SLC7A11)和P53在肝癌中起關(guān)鍵作用。免疫組織化學(xué)(IHC)檢測未照射和IR后12h異種移植腫瘤中SOCS2和鐵死亡蛋白的表達(dá),發(fā)現(xiàn)IR增加SOCS2和鐵死亡標(biāo)記物(4-HNE)的表達(dá),但抑制GPX4和SLC7A11的表達(dá)(圖2J)。此外,過表達(dá)SOCS2的異種移植腫瘤中GPX4和SLC7A11表達(dá)量降低,而4-HNE表達(dá)量升高(圖2J)。這些結(jié)果表明輻射誘導(dǎo)與過表達(dá)SOCS2都能出現(xiàn)鐵死亡。證明SOCS2可能通過誘導(dǎo)鐵死亡而促進(jìn)HCC的放射增敏作用。
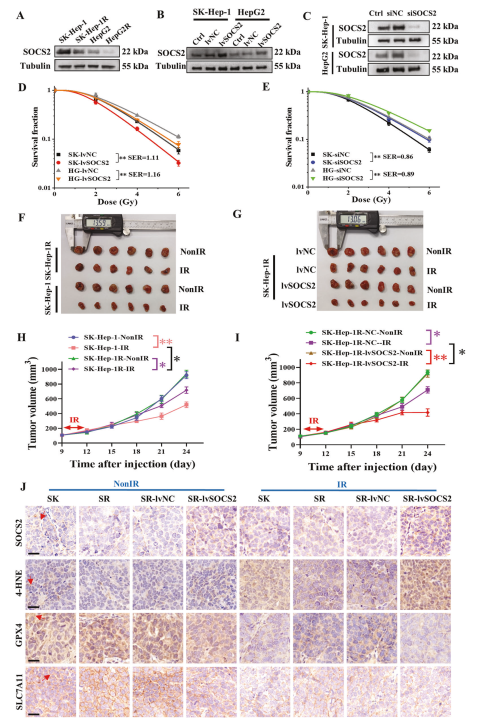
圖2 過表達(dá)SOCS2提高HCC的體內(nèi)外放射敏感性
3、鐵死亡促進(jìn)HCC組織和細(xì)胞的放射增敏作用
為進(jìn)一步驗(yàn)證上述推測,作者通過免疫熒光分析GPX4和SLC7A11在HCC臨床組織中的表達(dá),發(fā)現(xiàn)放射敏感組織GPX4和SLC7A11表達(dá)水平更低,表明具有更高水平的鐵死亡(圖3A)。接著WB檢測HCC細(xì)胞中GPX4和SLC7A11的表達(dá)水平,同樣發(fā)現(xiàn)GPX4和SLC7A11表達(dá)隨著細(xì)胞對IR的抗性而增強(qiáng)(圖3B)。接下來,liperfluo(脂質(zhì)過氧化物熒光探針)免疫熒光結(jié)果顯示,氫過氧化物脂質(zhì)水平隨著HCC放射敏感性增加,且IR后升高(圖3C,D)。這些結(jié)果提示放射抗性HCC細(xì)胞具有較低的鐵死亡水平。
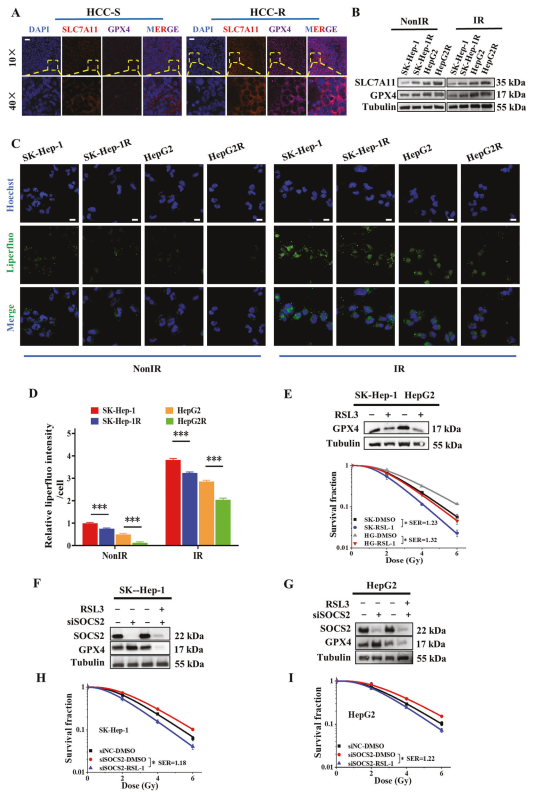
圖3增強(qiáng)的鐵濃度導(dǎo)致HCC的放射增敏作用
為進(jìn)一步檢測鐵死亡是否進(jìn)行HCC放射增敏,該研究使用RSL3(GPX4的抑制劑)促進(jìn)鐵死亡的產(chǎn)生,WB檢測發(fā)現(xiàn)RSL3處理后SK-Hep-1和HepG2細(xì)胞的放射敏感性增加(圖3E),而用RSL3處理siSOCS2轉(zhuǎn)染的HCC細(xì)胞后,放射增敏作用隨GPX4表達(dá)下降而降低(圖3F,G,H,I)。總之,鐵死亡有助于HCC細(xì)胞的放射增敏作用,而RSL3誘導(dǎo)的鐵死亡可以逆轉(zhuǎn)SOCS2抑制后獲得的放射抗性。
4、SOCS2與鐵死亡正相關(guān)
由于鐵死亡和SOCS2都有助于HCC的放射增敏,而圖2J暗示SOCS2促進(jìn)鐵死亡,因此作者試圖深入探討SOCS2與鐵死亡之間的關(guān)系。通過檢測IR 0~24h內(nèi)HCC細(xì)胞中SOCS2和GPX4的蛋白表達(dá)水平變化,發(fā)現(xiàn)與未照射的細(xì)胞相比,在IR后24小時(shí)內(nèi)SOCS2增加,而GPX4減少,在4小時(shí)內(nèi)變化最明顯(圖4A)。接下來測量未照射或IR后4小時(shí)細(xì)胞中的蛋白質(zhì)表達(dá),發(fā)現(xiàn)與GPX4和SLC7A11表達(dá)相反,SOCS2表達(dá)量隨著放射抗性的增加而下降(圖4B)。此外,無論在未照射和IR的細(xì)胞中,過表達(dá)SOCS2都會抑制GPX4和SLC7A11的表達(dá)(圖4C,D)。
上述結(jié)果表明SOCS2在蛋白質(zhì)水平上促進(jìn)鐵死亡的發(fā)生,因此該研究進(jìn)一步探討SOCS2與鐵死亡的特征表型:細(xì)胞內(nèi)Fe2+含量和脂質(zhì)過氧化物之間的關(guān)系。通過檢測過表達(dá)SOCS2的HCC細(xì)胞中脂氟的相對熒光強(qiáng)度,發(fā)現(xiàn)SOCS2的增加促進(jìn)細(xì)胞質(zhì)脂質(zhì)過氧化物在HCC細(xì)胞中的積累,在IR后更為明顯(圖4E,F(xiàn))。廣泛而言,SOCS2抑制GPX4和SLC7A11的表達(dá),并誘導(dǎo)脂質(zhì)過氧化物和Fe2+的積累,促進(jìn)鐵死亡。

圖4 SOCS2促進(jìn)肝癌細(xì)胞鐵死亡
5、SOCS2通過泛素化降解SLC7A11
為研究SOCS2如何介導(dǎo)鐵濃縮從而調(diào)節(jié)HCC放射敏感性,通過免疫熒光染色發(fā)現(xiàn)SOCS2的熒光密度與SLC7A11相反,表明SOCS2與SLC7A11呈負(fù)相關(guān)(圖5A)。接著通過Co-IP證明SLC7A11與SOCS2相互作用(圖5B,C)。為了解這種相互作用的功能后果,作者想知道SOCS2是否可以負(fù)調(diào)節(jié)SLC7A11的表達(dá)或誘導(dǎo)其降解。WB檢測發(fā)現(xiàn)在SOCS2過表達(dá)后,SLC7A11的穩(wěn)態(tài)水平顯著降低,并且SLC7A11的半衰期大大縮短(圖5D,E)。說明SOCS2通過蛋白質(zhì)方面而不是轉(zhuǎn)錄方面促進(jìn)SLC7A11的降解。
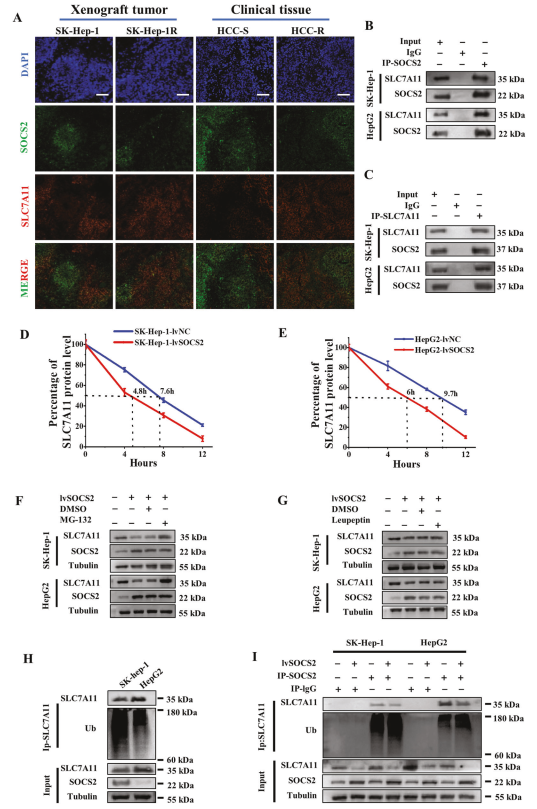
圖5 SOCS2與 SLC7A11相互作用,并通過泛素-蛋白酶體途徑降低其水平
接下來,為深入研究SLC7A11降解的機(jī)制,作者在HCC細(xì)胞中加入蛋白酶體抑制劑(MG-132)和溶酶體抑制劑(亮肽蛋白)。盡管高表達(dá)的SOCS2可以降低SLC7A11的蛋白質(zhì)水平,但是這種下調(diào)通過MG-132的處理被逆轉(zhuǎn),而亮肽蛋白不能逆轉(zhuǎn)(圖5F,G),表明SOCS2誘導(dǎo)的SLC7A11下降依賴于蛋白酶體途徑而非溶酶體途徑。
由于SOCS2作為一種E3泛素連接酶,作者推測SLC7A11可能被SOCS2特異性識別并經(jīng)歷泛素化降解。WB分析顯示SK-hep-1細(xì)胞中的泛素化SLC7A11水平顯著高于HepG2細(xì)胞(圖5H)。此外,在過表達(dá)SOCS2的HCC細(xì)胞中,SLC7A11表達(dá)量顯著降低,并且SLC7A11泛素化水平更高(圖5I)。
6、SOCS2的SH2結(jié)構(gòu)域與SLC7A11的N-末端結(jié)構(gòu)域相互作用促進(jìn)放射增敏
為闡明SOCS2和SLC7A11之間的相互作用區(qū)域,作者將SOCS2分為三個(gè)結(jié)構(gòu)域:NTD,SH2-結(jié)構(gòu)和CTD,構(gòu)建C-末端具有3×Flag標(biāo)簽的三個(gè)截短質(zhì)粒(質(zhì)粒A,B,C)和完整SOCS2序列的野生型(WT)質(zhì)粒,并將這些質(zhì)粒轉(zhuǎn)染到HCC細(xì)胞中(圖6A)。Co-IP分析顯示只有WT和B(SH2截短)的通道表現(xiàn)出SLC7A11條帶,表明SLC7A11與SOCS2的SH2結(jié)構(gòu)域相互作用(圖6B)。隨后,為研究SOCS2-SH2結(jié)構(gòu)域?qū)Ψ核鼗降挠绊懀髡咄ㄟ^從SOCS2全序列中刪除SH2結(jié)構(gòu)域來產(chǎn)生SOCS2-ΔSH2質(zhì)粒,發(fā)現(xiàn)SOCS2-ΔSH2突變體不能增加SLC7A11的泛素化水平,而SOCS2-WT質(zhì)粒顯著增加SLC7A11的泛素化水平(圖6C)。因此,SOCS2通過SOCS2的SH2結(jié)構(gòu)域誘導(dǎo)SLC7A11泛素化。
此外,為鑒定與SOCS2相互作用的SLC7A11的結(jié)構(gòu)域,作者還基于SLC7A11的結(jié)構(gòu)域建立三個(gè)截?cái)噘|(zhì)粒A,B,C(圖6D),發(fā)現(xiàn)SOCS2與SLC7A11的NTD相互作用(圖6E)。與SOCS2-ΔSH2質(zhì)粒的構(gòu)建一致,作者還構(gòu)建無N-末端的SLC7A11-ΔNTD突變質(zhì)粒,發(fā)現(xiàn)Flag-ΔNTD的泛素化水平檢測不到,而WT組中仍存在高水平的泛素化Flag-SLC7A11(圖6F)。表明SLC7A11-NTD與SOCS2相互作用并因此介導(dǎo)其自身的泛素化。此外,將SOCS2-ΔSH2或SOCS2-WT質(zhì)粒轉(zhuǎn)染HCC細(xì)胞后觀察IR后存活數(shù),發(fā)現(xiàn)SOCS2-ΔSH2組的存活數(shù)與其陰性對照相比沒有顯著差異,但顯著高于SOCS2-WT組(圖6G,H),這意味著SOCS2由于其SH2結(jié)構(gòu)域在HCC細(xì)胞中發(fā)揮放射增敏作用。

圖6 SOCS2-SH2結(jié)構(gòu)域與SLC7A11的N-末端結(jié)構(gòu)域相互作用以降低輻射抗性
7、SOCS2促進(jìn)SLC7A11的K48相關(guān)多聚泛素化并結(jié)合伸長蛋白B/C
確定SOCS2-SH2能通過識別SLC7A11-NTD介導(dǎo)SLC7A11泛素化后,作者想知道SLC7A11中發(fā)生的多聚泛素化的類型。到目前為止,K48和K63連接的鏈已被報(bào)道為最豐富和功能表征良好的多泛素鏈。為確定其中哪些存在于多泛素化的SLC7A11中,構(gòu)建SLC7A11的K48R和K63R泛素突變體,泛素化測定K48R突變體泛素化積累減少,而K63R突變體泛素化積累不變(圖7A),這意味著SLC7A11多泛素化主要以K48連接的泛素鏈而不是K63連接的形式產(chǎn)生。值得注意的是,K48R突變降低SLC7A11多聚泛素化的水平,但沒有完全降低,暗示其他連鎖類型也可能有助于這種多聚泛素化。
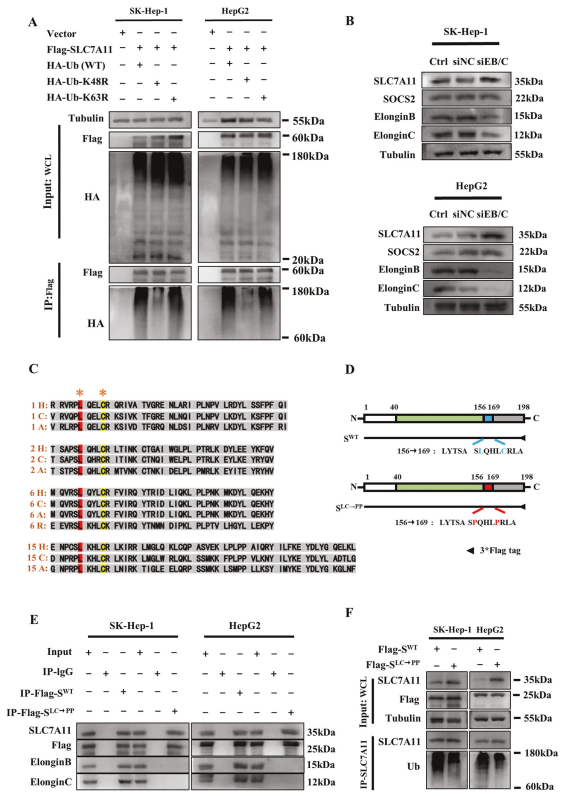
圖7 SOCS2通過延伸蛋白B/C泛素復(fù)合物介導(dǎo)K48連接的多聚泛素化鏈到SLC7A11上
如前所述,SOCS1和SOCS6通常通過SOCS-BOX區(qū)域與伸長蛋白B/C結(jié)合以組裝成E3泛素連接酶復(fù)合物介導(dǎo)泛素化,所以作者探究HCC細(xì)胞中SOCS2介導(dǎo)的SLC7A11泛素化是否也需要伸長蛋白B/C的參與。WB檢測顯示在HCC細(xì)胞中敲低伸長蛋白B/C不影響SOCS2表達(dá),但是SLC7A11表達(dá)量升高(圖7B),表明延伸蛋白B/C復(fù)合物是SOCS2介導(dǎo)的SLC7A11的泛素化降解所必需的。
接下來研究SOCS2與伸長蛋白B/C復(fù)合物相互作用的氨基酸位點(diǎn)。通過比較不同物種SOCS1、SOCS2、SOCS6和SAB15蛋白SOCS2-BOX區(qū)的氨基酸序列,發(fā)現(xiàn)只有Leu和Cys在不同的序列中保守(圖7C)。因此,作者假設(shè)Leu和Cys可能是SOCS2與伸長蛋白B/C相互作用的靶位點(diǎn)。為驗(yàn)證這一猜想,該研究構(gòu)建SOCS2突變質(zhì)粒(SOCS2LC→PP),其中SOCS2的Leu 162(L162)和Cys 166(C166)突變?yōu)镻ro,SOCS2WT質(zhì)粒作為對照(圖7D)。Co-IP顯示SOCS2WT可以與SLC7A11,伸長蛋白B和伸長蛋白C分別互作,而SOCS2LC→PP僅與SLC7A11互作,不與伸長蛋白B和伸長蛋白C互作(圖7E)。此外,SOCS2LC→PP也導(dǎo)致SLC7A11泛素化降低(圖7F),意味著伸長蛋白B/C在L162和C166位點(diǎn)與SOCS2互作以形成SOCS2/伸長蛋白B/C復(fù)合物,從而共同促進(jìn)SLC7A11的泛素化降解。
總而言之,本研究詳細(xì)研究SOCS2介導(dǎo)的HCC放射增敏促進(jìn)鐵死亡的過程。IR增加SOCS2表達(dá),導(dǎo)致SLC7A11的減少,隨后SOCS2-SH2與SLC7A11-NTD特異性識別,通過SOCS2的L162和C166位點(diǎn)與伸長蛋白B/C結(jié)合,并與E2泛素結(jié)合酶連接,誘導(dǎo)多聚泛素化(圖8A,B)。最終,具有泛素鏈的SLC7A11被26S蛋白酶體識別并分解成蛋白質(zhì)片段(圖8C)用于降解,這最終有助于HCC鐵死亡和放射增敏的發(fā)生。
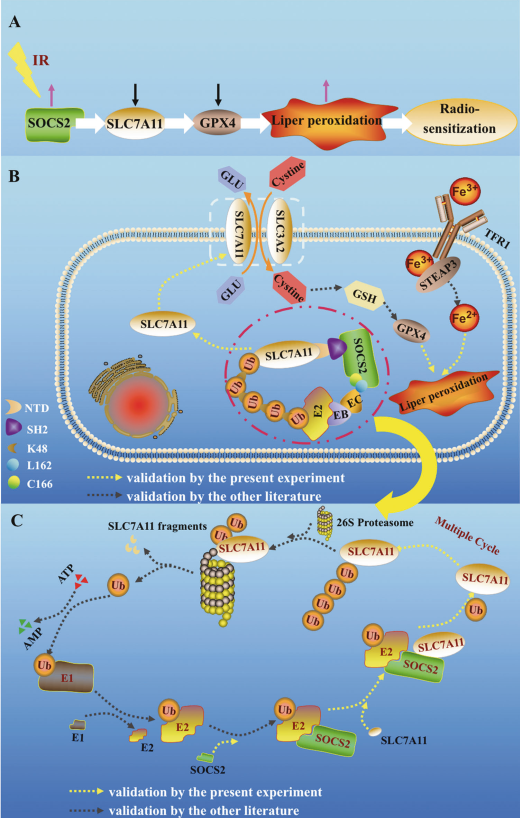
圖8 增量SOCS2促進(jìn)SLC7A11的泛素化降解,誘導(dǎo)HCC的鐵死亡和放射增敏作用
實(shí)驗(yàn)方法
RNA-seq和測序分析,小鼠異種植腫瘤模型,免疫熒光(IF)檢測,免疫組織化學(xué)(IHC)檢測,WB,細(xì)胞內(nèi)Fe2+的含量測定,細(xì)胞內(nèi)脂質(zhì)過氧化的測量,qRT-PCR,小干擾RNA(siRNA)轉(zhuǎn)染,質(zhì)粒轉(zhuǎn)染,Co-IP,泛素化測定
參考文獻(xiàn)
Chen Q, Zheng W, Guan J, Liu H, Dan Y, Zhu L, Song Y, Zhou Y, Zhao X, Zhang Y, Bai Y, Pan Y, Zhang J, Shao C. SOCS2-enhanced ubiquitination of SLC7A11 promotes ferroptosis and radiosensitization in hepatocellular carcinoma. Cell Death Differ. 2023 Jan;30(1):137-151. doi: 10.1038/s41418-022-01051-7.






