circPRMT5通過吸附miR-30c誘導EMT,促進膀胱癌的轉移
Circular RNAs (circRNAs)是一類新的,在人類癌癥中備受關注。但是其在癌細胞上皮間質轉化(EMT)的角色仍不清楚。本成果于2018年10月12日發表雜志Clin. Cancer Res(IF=10.2),在本研究中,作者的目的想識別新的circRNAs調節膀胱癌(UCB)細胞的EMT,探究他們的調節機制。首先UCB組織VS鄰近正常組織,做了circRNA芯片,篩選出了上調的circPRMT5。然后探究circPRMT5的功能和EMT機制。circPRMT5作為miRNA海綿體能夠吸附miR-30c,調節SNAIL1/E-cadherin通路,進一步調節UCB細胞的惡性和EMT。并且作者進一步識別了circPRMT5在UCB病人的血漿和尿液外泌體中也是上調的,并且與腫瘤轉移有相關性。circPRMT5可以考慮作為UCB病人的預后biomarker和治療靶點。
技術路線
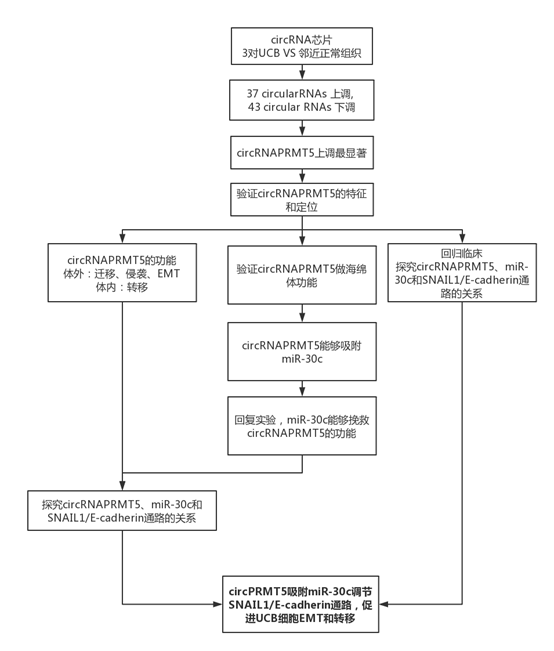
結果
1. CircRNAs在UCB組織中的表達譜和circPRMT5的特征。
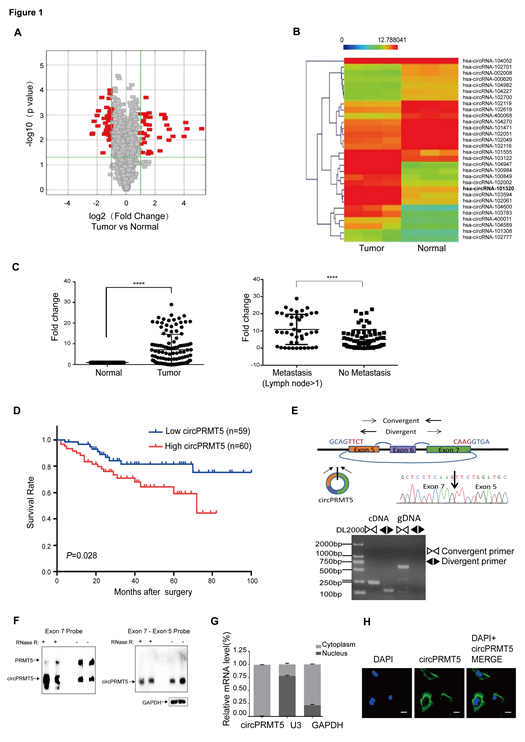
圖1. CircPRMT5在UCBs中上調并與患者的不良預后相關
A, UBC組織 VS 鄰近的膀胱組織中,火山圖展示了circRNAs 的表達改變倍數,紅色代表顯著改變的circRNAs。B, 聚類圖展示,UBC組織 VS 鄰近的膀胱組織中,差異表達的circRNAs。C, 散點圖表示,UBC組織 VS 鄰近的膀胱組織中,circPRMT5的表達。D, 低 VS 高表達circPRMT5的病人進行Kaplan-Meier曲線分析。E, 發散的和收斂的引物和F, Northern blots分析驗證circPRMT5是circRNA。G, 核質分離PCR 和H, FISH實驗驗證circPRMT5主要定位在細胞質中。
2. CircPRMT5 促進UCB 細胞的惡性發展。
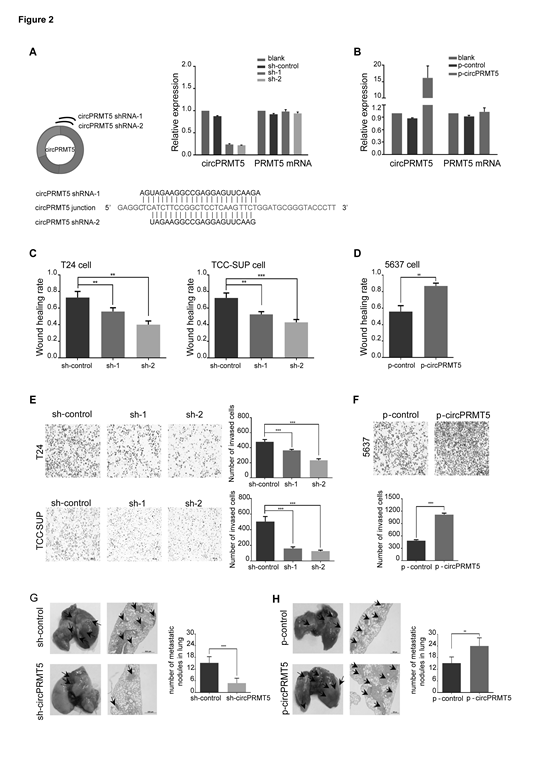
圖2. 沉默circPRMT5 能夠抑制UCB細胞的侵襲
A, 2個shRNA和示意圖和下調效果。B, circPRMT5過表達的效果。C和D,Wound healing assay展示下調circPRMT5能夠抑制UCB細胞的遷移,上調circPRMT5能夠促進UCB細胞的遷移。E和F, Transwell assay下調circPRMT5能夠抑制UCB細胞的侵襲,上調circPRMT5能夠促進UCB細胞的侵襲。G和H,裸鼠成瘤實驗展示下調circPRMT5能夠抑制肺轉移結節的數量或上調circPRMT5能夠促進肺轉移結節的數量。
3. CircPRMT5誘導UCB細胞的EMT。
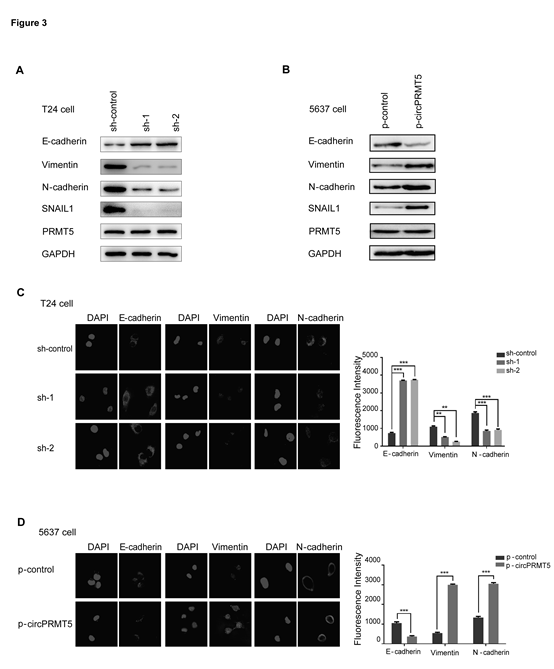
圖3. CircPRMT5激活SNAIL1通路誘導UCB細胞的EMT
A和B, Western blots 展示下調circPRMT5或上調circPRMT5后,EMT相關的marker表達情況。E-cadherin, Vimentin, N-cadherin, SNAIL1,PRMT5。C and D, 免疫熒光展示下調circPRMT5或上調circPRMT5后,EMT相關的marker表達情況,E-cadherin, Vimentin and N-cadherin。
4. CircPRMT5 在UCBs細胞中吸附miRNAs。
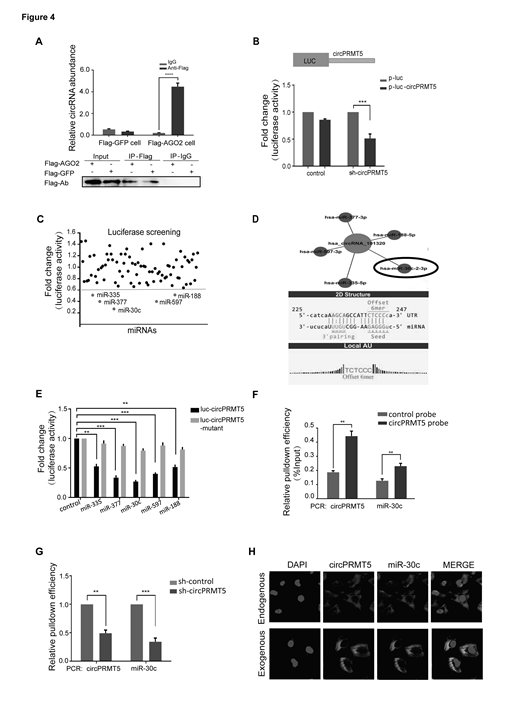
圖4. CircPRMT5在UCB細胞中吸附miR-30c
A, Ago2-RIP assay展示circPRM5顯著被富集。B, Luciferase reporter assay展示轉染shRNA后LUC-circPRMT5的活性。C, Luciferase reporter assay展示轉染83 miRNA mimicsLUC-circPRMT5的活性,進一步識別與circPRMT5結合的miRNA。D, miRNAs 和circPRMT5結合位點示意圖。E, Luciferase reporter assay 展示轉染miRNA mimics后LUC-circPRMT5 or LUC-circPRMT5-mutant的活性。F和G, RNA pull down assay展示circPRMT5和 miR-30c和circPRMT5相結合。H, IF 展示circPRMT5和miR-30c能共定位在對照和過表達circPRMT5的細胞中。
5. CircPRMT5調節miR-30c/SANIL1/E-cadherin通路并促進UCB細胞的惡性和EMT。
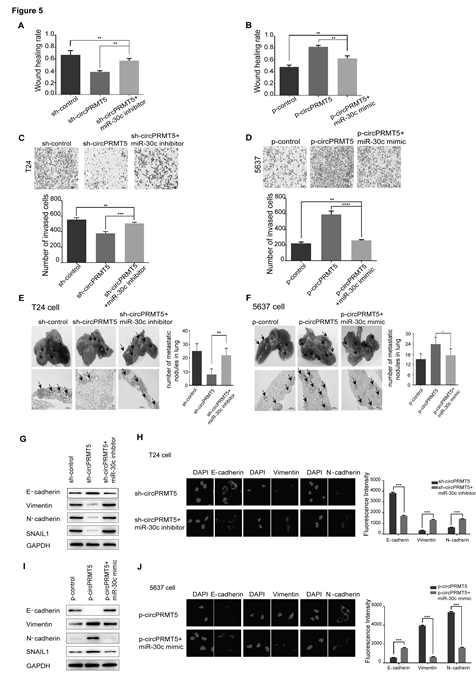
圖5. CircPRMT5封閉miR-30c的抑癌效應
A和C,下調circPRMT5抑制細胞遷移(A) 侵襲(C),這種現象能夠被加入miR-30c inhibitor后挽救。B and D, 上調circPRMT5促進細胞遷移 (B) 侵襲 (D),這種現象能夠被加入miR-30c mimics后挽救。E,下調circPRMT5抑制肺轉移結節的數量,這種現象能夠被加入miR-30c inhibitor后挽救。 (F),上調circPRMT5促進肺轉移結節的數量,這種現象能夠被加入miR-30c mimic后挽救。G和H,下調circPRMT5抑制Vimentin, N-cadherin和SNAIL1/E-cadherin通路,這種現象能夠被加入miR-30c inhibitor后挽救。I和J, 上調circPRMT5促進Vimentin, N-cadherin和SNAIL1/E-cadherin通路,這種現象能夠被加入miR-30c mimic后挽救。
6. CircPRMT5通過外泌體被釋放到UCB病人的血漿和尿液中并與腫瘤轉移相關。

圖6. CircPRMT5被miR-30c/SANIL1/E-cadherin通路調節在UCB病人中
A, CircPRMT5與miR-30c的表達呈負相關性。B, CircPRMT5與SNAIL1的表達呈正相關性。C, CircPRMT5與E-cadherin的表達呈負相關性。D, miR-30c的Kaplan-Meier curves分析。E, miR-30c在結節轉移中的表達情況。F, miR-30c與SNAIL1的表達呈負相關性。G, SNAIL1和E-cadherin的表達呈負相關性。H, 本文的機制模型: circPRMT5吸附miR-30c調節SNAIL1/E-cadherin通路,促進UCB細胞EMT和轉移。






