當(dāng)殺手變成小偷:PD-1胞啃作用抑制NK細(xì)胞消除腫瘤的能力
胞啃作用(trogocytosis)調(diào)節(jié)免疫反應(yīng),其分子機(jī)制尚不清楚。在白血病小鼠模型中,淋巴細(xì)胞對腫瘤細(xì)胞進(jìn)行高速率的胞啃作用。自然殺傷細(xì)胞(NK)和CD8+ T細(xì)胞在進(jìn)行胞吞作用時(shí),都從白血病細(xì)胞獲得檢查點(diǎn)受體PD-1。體外和體內(nèi)研究表明,NK細(xì)胞表面的PD-1并非內(nèi)源性表達(dá),而是完全來源于白血病細(xì)胞,并以SLAM受體依賴的方式表達(dá)。通過胞啃作用獲得的PD-1能有效抑制NK細(xì)胞的抗腫瘤免疫。克隆性漿細(xì)胞疾病患者的PD-1促紅細(xì)胞增多得到證實(shí),其中PD-1染色的NK細(xì)胞也可染色腫瘤細(xì)胞標(biāo)記物。我們的研究結(jié)果除了揭示了PD-1在NK細(xì)胞和細(xì)胞毒性T細(xì)胞上存在的一種以前未被認(rèn)識的機(jī)制外,還揭示了免疫細(xì)胞接觸腫瘤細(xì)胞時(shí)發(fā)生的膜轉(zhuǎn)移的免疫調(diào)節(jié)作用。本文于2022年4月發(fā)表于Science Advances (IF=14.957)。
技術(shù)路線:
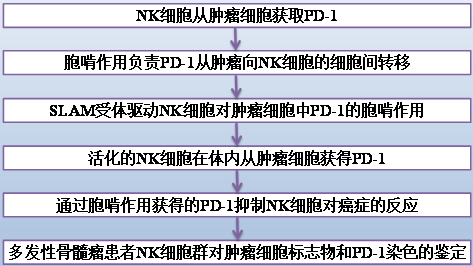
結(jié)果:
(1) NK細(xì)胞從腫瘤細(xì)胞獲取PD-1
小鼠NK細(xì)胞在體外被一組炎癥介質(zhì)急性刺激時(shí),未能在蛋白水平上上調(diào)PD-1。缺乏PD-1誘導(dǎo)與Pdcd1位點(diǎn)的表觀遺傳學(xué)分析相一致,在細(xì)胞因子刺激之前或之后,脾臟NK細(xì)胞中都無法獲得Pdcd1位點(diǎn),與NK細(xì)胞中另一種檢查點(diǎn)受體(Tigit)的啟動子或CD8+ T細(xì)胞中的Pdcd1位點(diǎn)形成對比(補(bǔ)充圖未展示)。
考慮到PD-1在NK細(xì)胞上表達(dá)的相互矛盾的證據(jù),我們假設(shè)NK細(xì)胞不是內(nèi)源性表達(dá)PD-1,而是從其他細(xì)胞獲得PD-1。為了驗(yàn)證這一假設(shè),我們最初使用了RMA細(xì)胞,它來源于小鼠T細(xì)胞的轉(zhuǎn)化,表達(dá)高水平的PD-1(圖1A,紅色)。我們生成了表達(dá)同基因標(biāo)記Thy-1.1 (C57BL/6小鼠不表達(dá)Thy-1.2等位變異)的RMA細(xì)胞,并使用CRISPR-Cas9靶向PD-1 (RMA-pdcd1?/?Thy1.1)(圖1A,分別為藍(lán)色和紫色)。當(dāng)與RMA細(xì)胞孵育時(shí),來自Pdcd1+/+和Pdcd1?/?小鼠的NK、T和B細(xì)胞均表達(dá)PD-1陽性,而RMA-Pdcd1?/?細(xì)胞則不表達(dá)PD-1(圖1B, C),這表明PD-1不是由先天和適應(yīng)性淋巴細(xì)胞內(nèi)源性表達(dá)的,而是在這些環(huán)境中從腫瘤細(xì)胞獲得的。使用從Pdcd1+/+或Pdcd1?/?小鼠中分離的NK細(xì)胞(純度約為90%)獲得一致的結(jié)果(圖1D)。無論PD-1在腫瘤細(xì)胞上是否表達(dá),免疫細(xì)胞表面都能大量檢測到Thy-1.1(圖1B, C)。為了確定RMA細(xì)胞內(nèi)源性表達(dá)的其他蛋白是否被NK細(xì)胞獲得,我們將表達(dá)cd45.1的NK細(xì)胞與表達(dá)CD45.2的RMA細(xì)胞共培養(yǎng)。結(jié)果表明,當(dāng)與RMA細(xì)胞相互作用時(shí),NK細(xì)胞獲得了幾種它們不會內(nèi)源性表達(dá)的蛋白質(zhì)。
我們接下來使用了C1498細(xì)胞,這是常用的白血病模型。部分C1498細(xì)胞(約5%)在培養(yǎng)中內(nèi)源性表達(dá)PD-1(圖2A)。我們對PD-1+C1498細(xì)胞進(jìn)行分類,確認(rèn)它們在培養(yǎng)2周后穩(wěn)定表達(dá)PD-1(圖2B),然后與來自Pdcd1+/+或Pdcd1?/?窩友的脾細(xì)胞孵育。根據(jù)RMA細(xì)胞獲得的結(jié)果,當(dāng)與C1498細(xì)胞孵育時(shí),Pdcd1?/?小鼠的NK細(xì)胞和CD8+ T細(xì)胞都獲得了PD-1,如果腫瘤細(xì)胞具有更高的PD-1表達(dá),則獲得PD-1的幾率更高(圖2C)。在Pdcd1?/?小鼠中觀察到的PD-1染色與在Pdcd1+/+小鼠中觀察到的PD-1染色非常相似,這表明即使在C1498模型中,大部分PD-1也不是由免疫細(xì)胞內(nèi)源性表達(dá),而是來自腫瘤細(xì)胞。使用Pdcd1?/?NK細(xì)胞純化的NK細(xì)胞重復(fù)類似實(shí)驗(yàn)。24小時(shí)后,NK細(xì)胞與PD-1+C1498細(xì)胞孵育后,PD-1染色呈陽性(圖2D)。PD-1染色在72小時(shí)后進(jìn)一步增加,同時(shí)與C1498親本細(xì)胞孵育的NK細(xì)胞發(fā)生了變化(圖2D)。這些數(shù)據(jù)表明NK細(xì)胞和CD8 T細(xì)胞在體外從白血病腫瘤細(xì)胞系獲得PD-1。
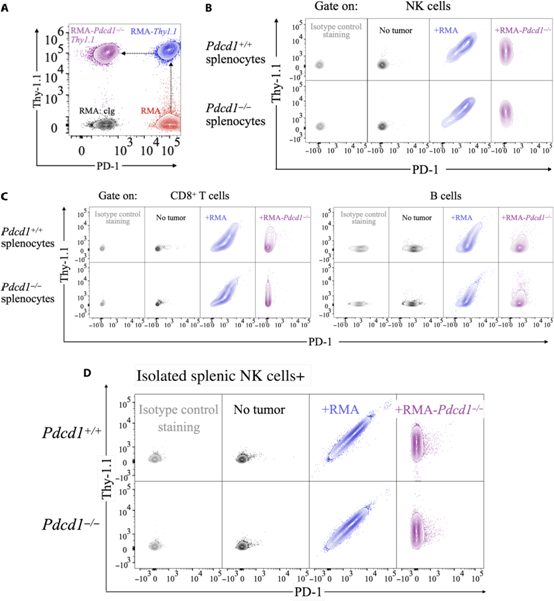
圖1:淋巴細(xì)胞從RMA癌細(xì)胞獲得PD-1和Thy-1.1
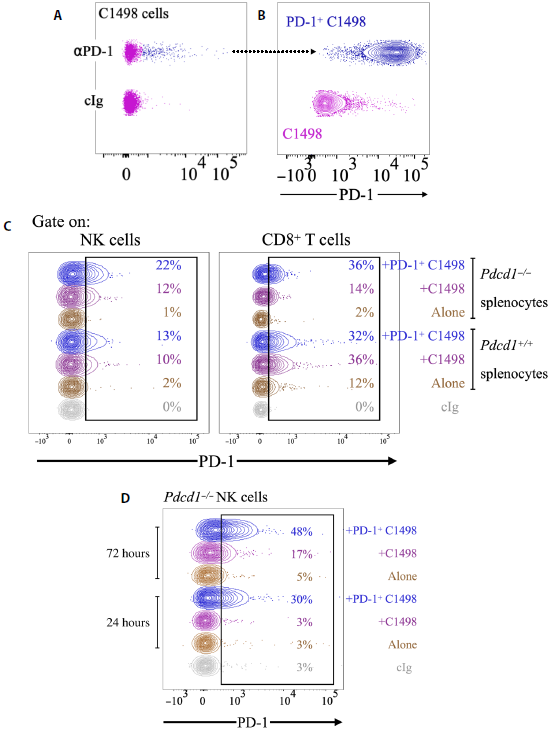
圖2:NK細(xì)胞和T細(xì)胞從C1498癌細(xì)胞中獲得PD-1
(2) 胞啃作用負(fù)責(zé)PD-1從腫瘤向NK細(xì)胞的細(xì)胞間轉(zhuǎn)移
一旦我們確定NK細(xì)胞從腫瘤細(xì)胞中獲得PD-1,我們就研究了胞啃作用是否負(fù)責(zé)PD-1的轉(zhuǎn)移。細(xì)胞-細(xì)胞接觸是胞啃作用所必需的。與我們的假設(shè)一致,PD-1是通過胞啃作用獲得的,與腫瘤細(xì)胞一起培養(yǎng)的Pdcd1?/?NK細(xì)胞未能對PD-1和Thy-1.1進(jìn)行染色(圖3A, B)。此外,用RMA細(xì)胞修飾的上清液培養(yǎng)的NK細(xì)胞未能對PD-1進(jìn)行染色(圖3)。這些實(shí)驗(yàn)揭示了細(xì)胞間的接觸是NK細(xì)胞獲取PD-1所必需的,并表明可溶性或外泌體PD-1不負(fù)責(zé)PD-1的轉(zhuǎn)移。
雖然目前還沒有一種特定的胞啃作用的藥理抑制劑,但已知阻斷三磷酸腺苷(ATP)合成或肌動蛋白聚合會干擾胞啃作用。與PD-1是通過NK細(xì)胞的胞啃作用獲得的觀點(diǎn)一致,疊氮化鈉或抗霉素A(兩者都阻止ATP合成)或拉赤菌素A(阻止肌動蛋白聚合)預(yù)處理NK細(xì)胞,導(dǎo)致PD-1和Thy-1.1獲取的強(qiáng)烈減少(圖3E, F)。最后,用放線菌素D(阻止轉(zhuǎn)錄)預(yù)處理NK細(xì)胞,并沒有阻止Pdcd1+/+NK細(xì)胞對PD-1的染色。證實(shí)NK細(xì)胞表面的PD-1蛋白并非來源于內(nèi)源性Pdcd1轉(zhuǎn)錄本(補(bǔ)充圖未展示)。
蛋白質(zhì)通過胞啃作用的轉(zhuǎn)移伴隨著膜脂的轉(zhuǎn)移。PD-1轉(zhuǎn)移與從腫瘤細(xì)胞中獲取脂質(zhì)相結(jié)合,如實(shí)驗(yàn)所示,NK細(xì)胞與先前用CellVue標(biāo)記的RMA細(xì)胞共培養(yǎng),CellVue是一種嵌入細(xì)胞膜脂質(zhì)區(qū)域的染料(圖3G)。不僅NK細(xì)胞對該染料呈強(qiáng)烈陽性,而且PD-1染色在從腫瘤細(xì)胞中獲得脂質(zhì)的NK細(xì)胞上檢測得更豐富(圖3G)。
為了獲得PD-1被NK細(xì)胞胞啃的直接證據(jù),我們用PD-1綠色熒光蛋白(GFP)融合蛋白補(bǔ)充PD-1缺陷的RMA細(xì)胞。在活體成像實(shí)驗(yàn)中,NK細(xì)胞與腫瘤細(xì)胞共孵卵幾分鐘后獲得GFP信號(補(bǔ)充圖未展示)。這些實(shí)驗(yàn)表明,PD-1與其他蛋白質(zhì)一起,通過NK細(xì)胞的胞啃作用獲得。
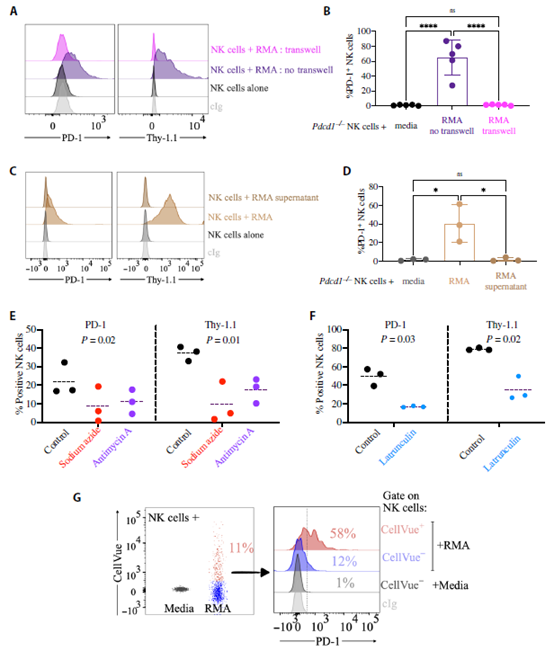
圖3:Trogocytosis (胞啃作用)負(fù)責(zé)PD-1從腫瘤向NK細(xì)胞的細(xì)胞間轉(zhuǎn)移
(3) SLAM受體驅(qū)動NK細(xì)胞對腫瘤細(xì)胞中PD-1的胞啃作用
從供體細(xì)胞獲取蛋白質(zhì)可以通過受體-配體接合來促進(jìn),這一過程被稱為反式內(nèi)吞作用,已知NK細(xì)胞介導(dǎo)。在培養(yǎng)中,NK細(xì)胞不表達(dá)PD-L2,但表達(dá)PD-L1 (圖4A),因此,PD-L1可以作為反式內(nèi)吞作用驅(qū)動的PD-1獲取的配體。然而,飽和劑量的PD-L1阻斷抗體并沒有減少PD-1的獲取(圖4B, C)。用一種抗體阻斷RMA細(xì)胞上的PD-1也得到了類似的結(jié)果,這種抗體可以阻止PD-L1的結(jié)合。這些實(shí)驗(yàn)不僅表明PD-1/PD-L1的結(jié)合不是PD-1轉(zhuǎn)移所必需的,而且還表明PD-1抗體與Fc受體的接合不能促進(jìn)胞吞作用。我們使用來自兩種不同小鼠品系的PD-L1缺陷NK細(xì)胞尋求遺傳證實(shí):全身PD-L1敲除(Cd274?/?)和NK細(xì)胞特異性PD-L1敲除(Ncr1+/Cre×Cd274fl/fl),我們將其與PD-1缺陷小鼠(Pdcd1?/?Ncr1+/CreCd274fl/fl)進(jìn)行雜交。PD-L1缺陷NK細(xì)胞獲得PD-1和Thy-1.1的水平與PD-L1表達(dá)對照組分離的NK細(xì)胞相似(圖4D, E)。在CD8+ T細(xì)胞和B細(xì)胞中,PD-L1對于PD-1和Thy-1.1的獲取也是不可或缺的(補(bǔ)充圖未展示)。
SLAM受體是造血細(xì)胞之間細(xì)胞-細(xì)胞相互作用的重要介質(zhì),不僅在NK細(xì)胞中大量表達(dá),還在T細(xì)胞和B細(xì)胞中大量表達(dá)。考慮到PD-1同時(shí)被先天和適應(yīng)性淋巴細(xì)胞胞啃,我們假設(shè)SLAM受體促進(jìn)了PD-1的胞啃。為了驗(yàn)證這一假設(shè),我們將整個(gè)SLAM位點(diǎn)被刪除的小鼠脾細(xì)胞與腫瘤細(xì)胞一起培養(yǎng),然后評估NK細(xì)胞、T細(xì)胞和B細(xì)胞的PD-1和Thy-1.1染色。與我們的假設(shè)一致,來自SLAM缺陷小鼠的NK細(xì)胞不能從RMA細(xì)胞獲得PD-1(圖4F)。不僅PD-1的獲取被取消,而且SLAM缺陷的NK細(xì)胞不能與腫瘤細(xì)胞進(jìn)行胞吞作用,如缺乏Thy-1.1轉(zhuǎn)移所示(圖4F)。由于SLAM受體在許多白細(xì)胞中廣泛表達(dá),我們研究了NK細(xì)胞的細(xì)胞內(nèi)表達(dá)是否對PD-1嗜噬作用是必需的。為此,我們從CD45.1 (SLAM-充足)或CD45.2 (SLAM-缺乏)小鼠中分離出脾臟NK細(xì)胞,并以競爭性或非競爭性方式與RMA細(xì)胞共培養(yǎng)。缺乏SLAM受體的分離NK細(xì)胞從腫瘤細(xì)胞獲取PD-1的效率較低。這不僅在SLAM充足和SLAM缺乏細(xì)胞與腫瘤細(xì)胞共培養(yǎng)時(shí)是正確的,而且在競爭環(huán)境中也是如此,在腫瘤細(xì)胞存在的情況下,兩種基因型一起培養(yǎng)(圖4G)。
考慮到SLAM受體在介導(dǎo)細(xì)胞-細(xì)胞相互作用中的重要性,我們分析了其他粘附分子的缺失是否也會干擾胞啃作用。LFA-1是一個(gè)關(guān)鍵的粘附分子,但缺乏CD11a表達(dá)(LFA-1的亞基)的NK細(xì)胞在PD-1或Thy-1.1獲取方面并不存在缺陷(補(bǔ)充圖未展示)。NKG2D是一種由NK細(xì)胞普遍表達(dá)的激活受體,它也不參與介導(dǎo)NK細(xì)胞和RMA細(xì)胞之間的胞啃作用(補(bǔ)充圖未展示)。這些結(jié)果表明SLAM受體介導(dǎo)PD-1從腫瘤到免疫細(xì)胞的胞啃作用。

圖4:SLAM受體是胞啃作用所必需的
(4) 活化的NK細(xì)胞在體內(nèi)從腫瘤細(xì)胞獲得PD-1
我們進(jìn)行了體內(nèi)研究以確定瘤內(nèi)NK細(xì)胞是否胞啃PD-1。將Pdcd1+/+或Pdcd1?/?littermates與表達(dá)Thy-1.1的RMA或RMA-Pdcd1?/?細(xì)胞一起注射,當(dāng)腫瘤達(dá)到~300 mm3時(shí),我們分析瘤內(nèi)淋巴細(xì)胞的PD-1染色(補(bǔ)充圖未展示)。在所有小鼠隊(duì)列中,NK細(xì)胞浸潤腫瘤,Thy-1.1染色強(qiáng)烈(圖5A-D, y軸),表明體內(nèi)發(fā)生了胞啃現(xiàn)象。只有當(dāng)腫瘤細(xì)胞不僅在Pdcd1+/+小鼠中表達(dá)PD-1,而且在Pdcd1?/?小鼠中也表達(dá)PD-1時(shí),NK細(xì)胞表面才檢測到高水平的PD-1(圖5A, C相對于B, D)。這些數(shù)據(jù)表明,PD-1不僅被腫瘤浸潤的NK細(xì)胞獲得,而且在RMA模型中,胞啃作用是導(dǎo)致PD-1在NK細(xì)胞表面存在的主要機(jī)制。對CD8+ T細(xì)胞的觀察結(jié)果一致(圖5A-D)。Pdcd1?/?小鼠兩側(cè)注射RMA或RMA-Pdcd1?/?細(xì)胞,只有NK細(xì)胞浸潤RMA腫瘤,但沒有PD-1缺陷腫瘤或脾臟NK細(xì)胞,PD-1染色(圖5E, F)。這些數(shù)據(jù)表明NK細(xì)胞從腫瘤微環(huán)境中的癌細(xì)胞獲得PD-1。
PD-1染色在活化的NK細(xì)胞上更高。對Pdcd1?/?小鼠浸潤RMA腫瘤的NK和T細(xì)胞的分析證實(shí),PD-1+NK和T細(xì)胞對Sca-1和CD69等激活標(biāo)記的染色也更亮(圖5G)。當(dāng)分析腫瘤微環(huán)境中PD-1+與PD-1?NK細(xì)胞時(shí),我們發(fā)現(xiàn)獲得PD-1的NK細(xì)胞更被激活,表達(dá)更高水平的激活受體,并且分布在CD11b/CD27定義的三種成熟狀態(tài),略微偏向成熟且有功能的CD11b+CD27+ (R2)細(xì)胞(補(bǔ)充圖未展示)。我們沒有觀察到與KLRG1表達(dá)的相關(guān)性,只注意到與NKG2A的弱相關(guān)性(補(bǔ)充圖未展示),而其他檢查點(diǎn)受體包括CTLA-4, TIM3和TIGIT只是低表達(dá)。獲得PD-1的NK細(xì)胞是更好的干擾素-γ(IFN-γ)生產(chǎn)者,并且脫顆粒性更強(qiáng)(補(bǔ)充圖未展示)。這些數(shù)據(jù)表明,與腫瘤細(xì)胞相遇激活的NK細(xì)胞也是更容易獲得PD-1的細(xì)胞,因此更容易被PD-1抑制。
我們在體內(nèi)測試了SLAM受體對PD-1胞啃作用的需求。與體外實(shí)驗(yàn)一致(圖4F, G),浸潤RMA腫瘤的SLAM缺陷NK細(xì)胞獲得較低水平的PD-1和Thy-1.1(圖5H),突出了SLAM受體作為胞啃作用的驅(qū)動因素的重要性。
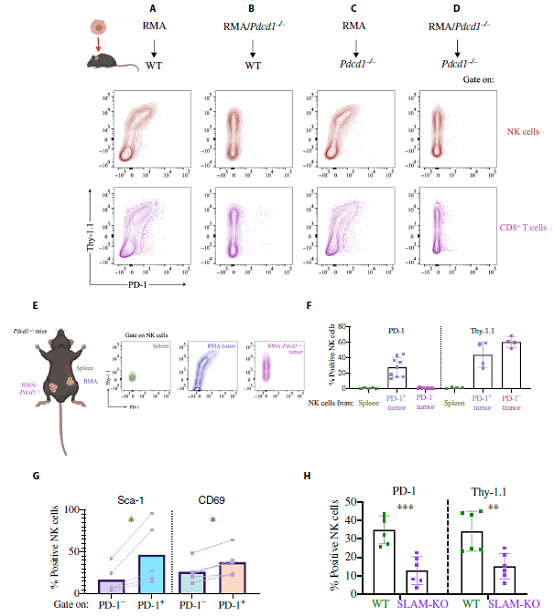
圖5:瘤內(nèi)淋巴細(xì)胞從腫瘤細(xì)胞獲得PD-1
(5) 通過胞啃作用獲得的PD-1抑制NK細(xì)胞對癌癥的反應(yīng)
一旦我們確定NK細(xì)胞在體內(nèi)胞啃PD-1,我們就試圖確定胞啃PD-1是否抑制抗腫瘤免疫。使用CRISPR-Cas9,生成了缺乏PD-1表達(dá)的RMA-S-Pdl1變體(圖6A)。注射到Pdcd1?/?小鼠(其中NK細(xì)胞上PD-1的唯一來源是腫瘤細(xì)胞)時(shí),缺乏PD-1表達(dá)的腫瘤細(xì)胞的生長明顯減慢(圖6B)。然而,缺乏PD-1并不會延遲體外細(xì)胞的生長,也不會阻止RMA-S-Pdl1-Pdcd1?/?細(xì)胞在免疫缺陷小鼠中生長腫瘤(圖6C)。結(jié)果表明,缺乏PD-1的腫瘤細(xì)胞形成異位腫瘤的能力降低,而不是具有細(xì)胞固有的生長缺陷,因?yàn)樗鼈儾荒芡ㄟ^PD-1轉(zhuǎn)移抑制NK細(xì)胞。
通過RMA-S-Pdl1模型,我們先前證明PD-1阻斷可以挽救NK細(xì)胞在體內(nèi)控制腫瘤生長的能力。考慮到PD-1在腫瘤細(xì)胞中的表達(dá)以細(xì)胞外源性方式促進(jìn)體內(nèi)生長,我們認(rèn)為PD-1阻斷劑的治療作用也應(yīng)在Pdcd1?/?小鼠中觀察到。當(dāng)我們用PD-1阻斷抗體(RMP1-14)注射RMA-S-Pdl1細(xì)胞治療PD-1缺陷小鼠時(shí),腫瘤生長顯著減少(圖6D)。當(dāng)我們向PD-1缺陷小鼠注射PD-1缺陷RMA-S-Pdl1細(xì)胞時(shí),PD-1阻斷劑沒有治療效果(圖6E)。
為了證實(shí)腫瘤來源的PD-1抑制了NK細(xì)胞,而沒有其他免疫反應(yīng)成分,我們在使用單克隆抗體(PK136)減少NK細(xì)胞的小鼠中注射了RMA-S-Pdl1細(xì)胞,并用PD-1阻斷劑治療小鼠。NK細(xì)胞的減少足以消除阻斷抗體的治療效果,而PD-1阻斷在對照組中延緩了腫瘤的生長(圖6F)。PD-1抗體在免疫受損小鼠中失效(圖6G)。免疫受損小鼠體內(nèi)腫瘤細(xì)胞的類似生長(圖6G)排除了PD-1阻斷抗體的腫瘤細(xì)胞固有效應(yīng)。
為了排除PD-1抗體的治療效果是由于NK細(xì)胞對PD-1抗體包被的癌細(xì)胞可能介導(dǎo)的抗體依賴細(xì)胞細(xì)胞毒性(ADCC),我們使用了一種缺乏與Fc受體結(jié)合能力的抗PD-1的工程版本(Fc-silent RMP1-14)。使用Fc沉默的PD-1抗體治療可以延緩表達(dá)PD-1的腫瘤的生長(圖6H),這表明PD-1抗體在Pdcd1?/?小鼠中的治療效果不是由于ADCC。這些結(jié)果表明,受血小板胞啃的PD-1抑制了NK細(xì)胞的抗腫瘤活性,而PD-1阻斷抗體可以拯救NK細(xì)胞。
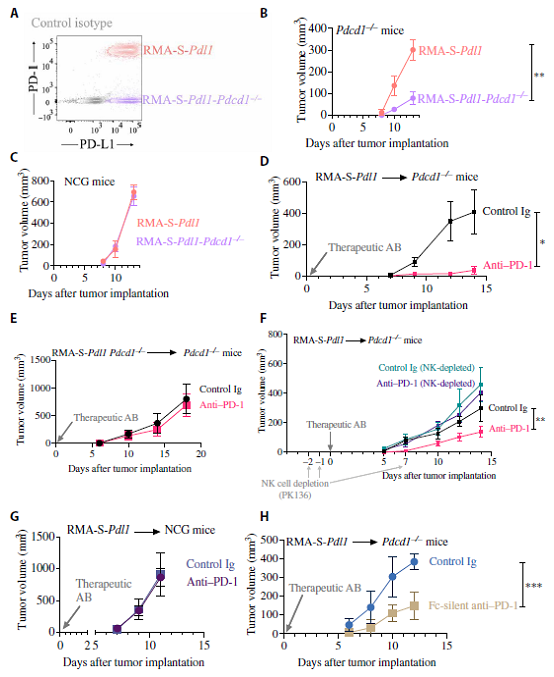
圖6:NK細(xì)胞存在且腫瘤細(xì)胞表達(dá)PD-1時(shí),PD-1阻斷劑對Pdcd1?/?小鼠有效
(6) 多發(fā)性骨髓瘤患者NK細(xì)胞群對腫瘤細(xì)胞標(biāo)志物和PD-1染色的鑒定
為了確定NK細(xì)胞是否從癌癥患者的腫瘤細(xì)胞中獲得PD-1,我們分析了來自克隆漿細(xì)胞疾病患者骨髓(BM)的NK細(xì)胞的PD-1染色。我們依賴于CD138,一種經(jīng)常由無性系漿細(xì)胞表達(dá)但不由NK細(xì)胞表達(dá)的蛋白,作為替代促紅細(xì)胞增多標(biāo)記物。流式細(xì)胞術(shù)分析證實(shí),在一些患者中存在高散射CD138+群體(補(bǔ)充圖未展示),我們將其鑒定為克隆漿細(xì)胞。在大多數(shù)樣本中,高散射CD138+細(xì)胞表達(dá)PD-1(補(bǔ)充圖未展示)。NK細(xì)胞進(jìn)行胞啃作用的指示來自于BM抽吸液的分析,其中鑒定出CD138+NK細(xì)胞群,在CD56brightCD16?和CD56dimCD16+NK細(xì)胞亞群中(圖7,粉紅色和綠色),證實(shí)了在小鼠模型中獲得的結(jié)果。CD138和PD-1染色的NK細(xì)胞數(shù)量可觀且一致(圖7綠色),這支持了克隆漿細(xì)胞疾病患者的NK細(xì)胞從腫瘤細(xì)胞中獲得PD-1和癌細(xì)胞標(biāo)記物的觀點(diǎn)。
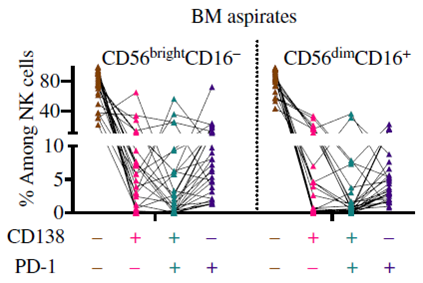
圖7:NK細(xì)胞可抑制CD138和PD-1在克隆漿細(xì)胞疾病患者骨髓中的作用
結(jié)論:胞啃作用是NK細(xì)胞和T細(xì)胞從腫瘤細(xì)胞中獲得PD-1的一種新機(jī)制。PD-1胞啃作用強(qiáng)烈依賴SLAM受體,在體內(nèi)功能上抑制NK細(xì)胞消除腫瘤的能力。
參考文獻(xiàn):
Hasim, M. S., Marotel, M., Hodgins, J. J., Vulpis, E., Makinson, O. J., Asif, S., Shih, H. Y., Scheer, A. K., MacMillan, O., Alonso, F. G., Burke, K. P., Cook, D. P., Li, R., Petrucci, M. T., Santoni, A., Fallon, P. G., Sharpe, A. H., Sciumè, G., Veillette, A., Zingoni, A., … Ardolino, M. (2022). When killers become thieves: TrogocytosedPD-1 inhibits NK cells in cancer. Science advances, 8(15), eabj3286. https://doi.org/10.1126/sciadv.abj3286.






