去泛素化酶UCHL3通過Hippo信號通路促進間變性甲狀腺癌的進展和轉移
YAP是Hippo通路的主要關鍵效應因子之一,YAP在間變性甲狀腺癌(ATC)中異常表達的機制尚不明確。在這里,我們鑒定了UCHL3是ATC中真正的YAP去泛素化酶。UCHL3以去泛素化活性依賴的方式穩定YAP。UCHL3缺失顯著降低ATC進展、干細胞樣和轉移,并增加細胞對化療的敏感性。UCHL3缺失降低ATC中YAP蛋白水平和YAP/TEAD靶基因表達。UCHL3啟動子分析顯示,TEAD4通過結合UCHL3啟動子激活UCHL3轉錄。總的來說,我們的研究結果表明,UCHL3在穩定YAP中起著關鍵作用,進而促進ATC的腫瘤發生,這表明UCHL3可能是治療ATC的潛在靶點。本文于2023年2月發表于“Cell Death & Differentiation”(IF=12.067)上。
技術路線:

結果:
1)UCHL3通過去泛素化活性穩定YAP
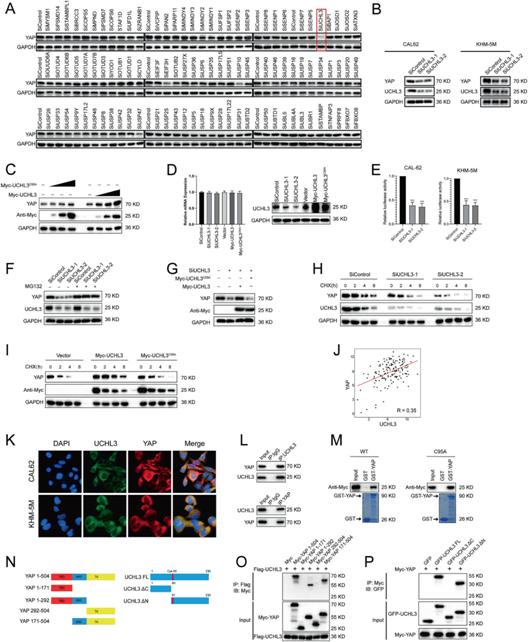
我們之前報道過YAP促進ATC細胞增殖。我們利用siRNA篩選文庫來鑒定ATC中負責YAP去泛素化和穩定的去泛素化酶。每種DUBs特異性的四種非重疊siRNA混合物被轉染到CAL-62細胞中。研究發現,沉默UCHL3顯著降低了YAP(圖1A)。我們檢測了UCHL3在10種甲狀腺癌細胞系(TPC-1、B-cpap、IHH4、FTC133、TT、CAL-62、8505c、KHM-5M、8305c、BHT-101)和永久化正常甲狀腺上皮細胞系(Nthy-ori3-1)中的表達,我們觀察到ATC細胞系中UCHL3的表達有上調趨勢,尤其是在CAL-62和KHM-5M細胞中(補充圖)。然后,我們在CAL-62和KHM5M細胞中敲低UCHL3,進一步驗證UCHL3在調節YAP蛋白水平方面的功能(圖1B)。一致地,UCHL3的異位表達以劑量依賴的方式深刻上調YAP。而催化失活的突變體C95A (UCHL3C95A)失去了上調YAP的能力,提示UCHL3對YAP的調控依賴于DUB活性(圖1C)。RT-PCR分析表明,UCHL3沒有改變YAP mRNA的豐度(圖1D)。熒光素酶報告基因實驗結果表明,UCHL3的缺失降低了CAL-62細胞中YAP/TEAD-熒光素酶報告基因的活性(圖1E)。我們檢測了UCHL3參與YAP去泛素化的可能性,并發現UCHL3缺失會降低YAP蛋白水平,這種影響可以通過添加蛋白酶體抑制劑MG132或過表達UCHL3-WT來逆轉,但其催化失活突變體UCHL3C95A不能逆轉(圖1F, G)。然后,我們用蛋白質合成抑制劑環己亞胺處理細胞,以確定UCHL3是否會影響YAP的穩定性。我們發現,在UCHL3缺失的細胞中,YAP的穩定性降低(圖1H)。在過表達UCHL3- WT而非UCHL3C95A的細胞中,YAP的半衰期延長(圖1I)。此外,我們觀察到UCHL3和YAP蛋白水平在人甲狀腺癌樣品中呈正相關(圖1J)。綜上所述,UCHL3通過穩定YAP調控Hippo信號通路。然后我們進行免疫熒光檢測評估UCHL3和YAP的細胞定位。免疫染色結果表明,YAP和UCHL3同時存在于ATC細胞的核和細胞質中(圖1K)。我們的免疫共沉淀(CoIP)實驗表明,內源性UCHL3可以與內源性YAP免疫共沉淀(圖1L)。GST-pulldown實驗表明,UCHL3在體外與YAP相互作用,其相互作用方式不依賴于其DUB活性(圖1M)。此外,缺失分析表明,UCHL3的C端與YAP的WW結構域存在物理相互作用(圖1N-P)。這些發現表明UCHL3與YAP相互作用。
2)UCHL3去泛素化YAP
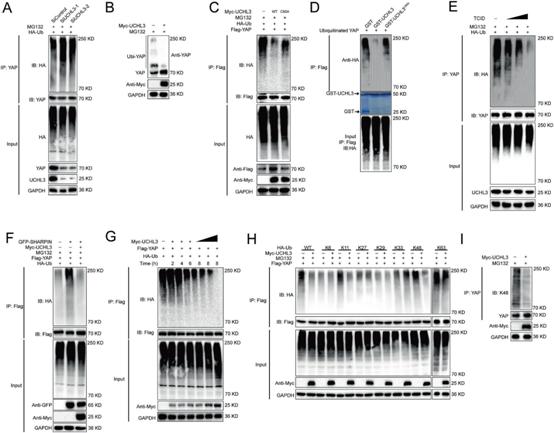
由于UCHL3是一種去泛素化酶,我們繼續研究UCHL3去泛素化YAP的可能性。UCHL3的缺失顯著增加了泛素化-YAP的水平(圖2A)。然后我們進行了內源性泛素化試驗,并檢測了YAP上的內源性泛素。如圖2B所示,UCHL3過表達降低了YAP上的內源性泛素。一致地,UCHL3-WT的異位表達,而不是UCHL3C95A,在體內和體外都顯著降低了細胞中YAP的泛素化(圖2C, D)。然后,我們用UCHL3的小分子抑制劑TCID處理CAL-62細胞,發現與UCHL3 siRNA類似,TCID抑制UCHL3以劑量依賴的方式增強了YAP的泛素化(圖2E)。此外,UCHL3降低了E3連接酶SHARPIN誘導的YAP泛素化(圖2F)。體內去泛素化實驗也顯示,UCHL3以時間和劑量依賴的方式去除YAP的泛素鏈(圖2G)。我們進一步對一系列泛素突變體進行泛素化實驗,以研究UCHL3對YAP的哪一種泛素鏈進行了去泛素化。結果發現,UCHL3有效地去除了YAP上的K11和K48連接的泛素鏈(圖2H)。綜上所述,UCHL3被證明是一種特異性去泛素化酶,其去多泛素化并穩定YAP。
3)UCHL3缺失抑制ATC細胞增殖和遷移
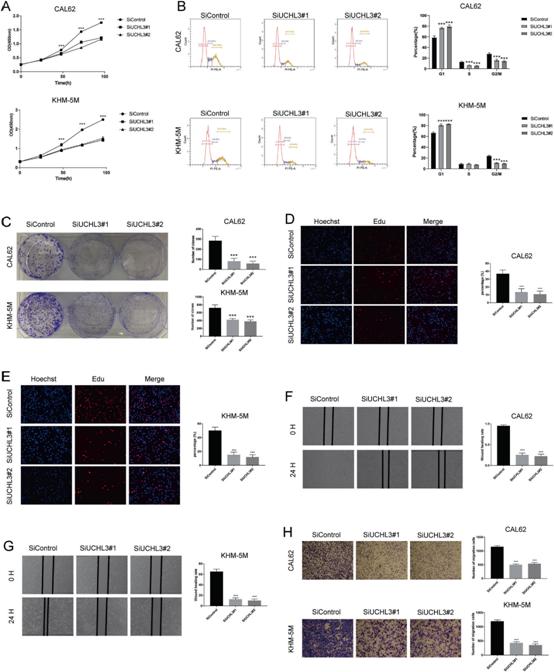
接下來,我們研究了UCHL3在調節ATC進展中的作用。我們的研究結果表明,UCHL3的缺失顯著降低了細胞的增殖和遷移。UCHL3的缺失降低了細胞增殖,增加了G1期的細胞數量,表明UCHL3可能調節ATC細胞從G1到S的轉變(圖3A, B)。克隆形成實驗結果顯示,UCHL3缺失顯著降低了CAL-62和KHM-5M細胞的克隆形成能力(圖3C)。同樣,EdU摻入實驗表明,UCHL3 siRNA處理的CAL-62和KHM-5M細胞的DNA合成受到抑制(圖3D, E)。此外,傷口愈合和transwell實驗顯示,UCHL3缺失顯著降低了細胞遷移能力(圖3F-H)。
4)UCHL3增強間變性甲狀腺癌干細胞的致瘤能力
由于ATC是一種未分化癌,我們隨后研究了UCHL3在間變性甲狀腺癌干性特征中的作用。研究發現,UCHL3缺失顯著減少了CAL-62和KHM-5M細胞球的形成(圖4A, B)。值得注意的是,與對照細胞相比,UCHL3的缺失顯著降低了多能轉錄因子Sox2、Nanog、KLF4和Oct4的表達(圖4C),并降低了ATC細胞的ALDH活性(圖4D)。此外,與對照細胞相比,表達shUCHL3的CAL-62細胞在NOD-SCID小鼠中顯示出較弱的腫瘤啟動能力(圖4E)。總的來說,UCHL3的沉默消除了間變甲狀腺癌干細胞的致瘤能力。

5)增加YAP表達可以恢復UCHL3缺失的影響
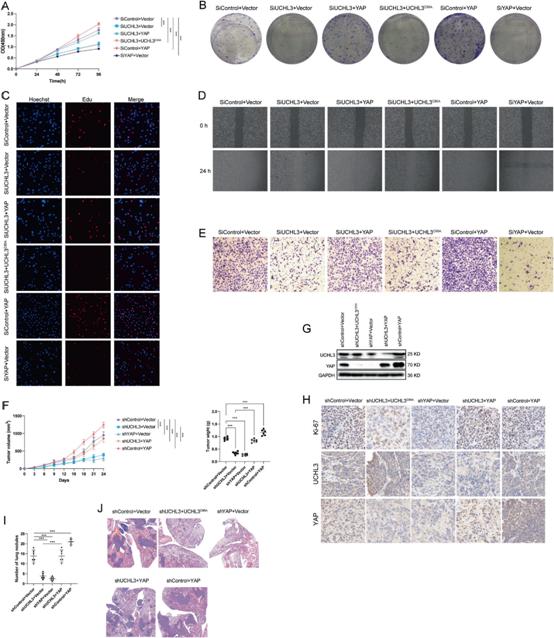
為了確定UCHL3通過穩定YAP調節ATC細胞增殖和遷移的機制,我們在UCHL3敲除的CAL-62細胞中進行異位表達YAP或UCHL3C95A的拯救實驗。CCK8實驗表明,過表達YAP在很大程度上恢復了CAL-62細胞的增殖速度(圖5A)。YAP表達的增加逆轉了CAL-62細胞的克隆形成能力(圖5B)。同樣,過表達YAP也促進了UCHL3缺失的CAL-62細胞的DNA合成(圖5C)。傷口愈合和transwell實驗表明,過表達YAP在很大程度上逆轉了UCHL3缺失誘導的抑制功能(圖5D, E)。但UCHL3C95A失去了促進增殖和遷移的能力。UCHL3的下調顯著抑制了體內腫瘤的生長,而YAP表達的恢復則消除了UCHL3缺失引起的抑制(圖5F-H)。我們進一步使用尾靜脈注射小鼠模型進行體內轉移評估。UCHL3缺失可顯著抑制小鼠的肺轉移,過表達YAP可緩解這一效應(圖5H, I)。綜上所述,這些結果表明UCHL3通過YAP促進ATC進展。
6)TCID抑制ATC細胞的生長和轉移
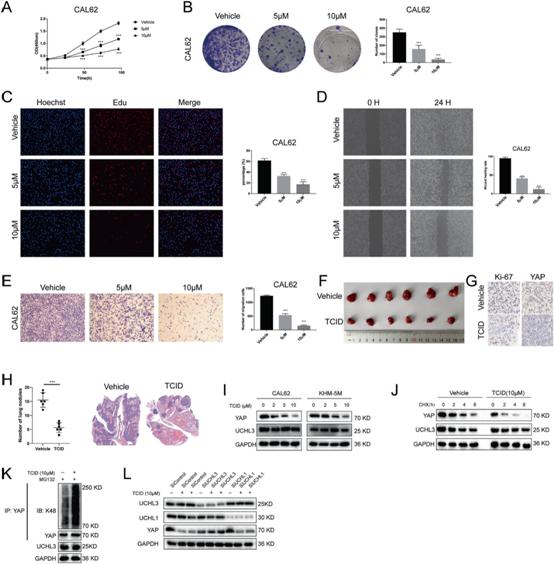
我們還研究了UCHL3抑制劑TCID (0,5,10 μM)對間變甲狀腺癌細胞增殖和遷移的影響。TCID抑制UCHL3對ATC細胞的生長和轉移具有劑量依賴性抑制作用(圖6A-E)。此外,我們在體內研究了TCID是否影響ATC的生長和轉移,發現TCID治療后裸鼠的腫瘤生長和轉移明顯降低(圖6F-H)。為了進一步確定TCID的抗腫瘤和抗轉移作用是否由UCHL3和YAP介導,我們構建了UCHL3和YAP敲除細胞。結果發現TCID對UCHL3和YAP敲除細胞的生長和轉移影響極小(補充圖)。符合我們之前的實驗,TCID抑制UCHL3顯著降低ATC細胞中YAP蛋白質水平(圖6I)。環己酰亞胺和TCID的聯合更快地減少內源性YAP水平(圖6J)。TCID對YAP的作用主要依賴于UCHL3,TCID對UCHL3敲除細胞中的YAP蛋白水平沒有影響,UCHL1的缺失不影響YAP蛋白水平(圖6K,6L)。
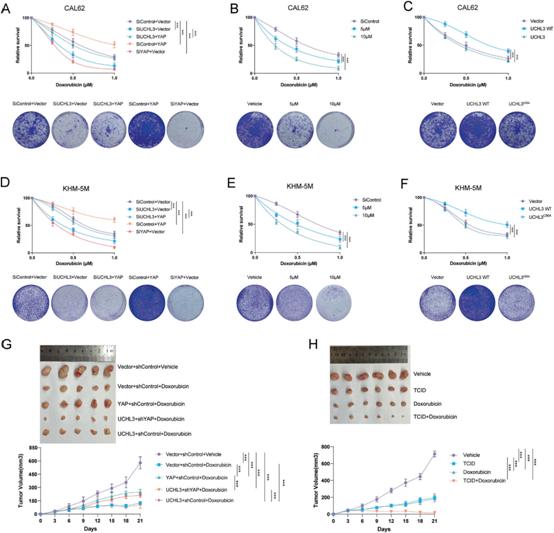
7)UCHL3通過YAP降低ATC細胞對化療的反應
阿霉素是ATC最常用的化療藥物。YAP活化已被證明在卵巢癌、乳腺癌和肝細胞癌等多種惡性腫瘤的化療耐藥中發揮作用。我們檢查了抑制UCHL3是否影響細胞對阿霉素的反應。如圖7所示,siRNA或TCID對UCHL3的抑制使CAL-62細胞對化療藥物的治療敏感(圖7A, B),而UCHL3缺失所引起的作用可以通過YAP重建來消除(圖7A)。一致地,過表達WT UCHL3的CAL-62細胞對阿霉素治療產生耐藥性,而過表達催化失活的突變體UCHL3的細胞則沒有這種效果(圖7C)。在KHM-5M細胞中觀察到同樣的結果(圖7G,F)。為了在體內證實UCHL3的抗化療功能,將過表達空載體、UCHL3、YAP或靶向YAP的shRNA的CAL-62細胞移植到裸鼠體內。我們發現,在阿霉素處理后,對照組CAL-62細胞的腫瘤生長顯著降低,而過表達UCHL3或YAP的腫瘤細胞比阿霉素處理的對照組細胞生長更快,YAP的缺失消除了過表達UCHL3引起的化療耐藥效應(圖7G)。TCID和阿霉素聯合應用比TCID或阿霉素單獨應用在體內顯著抑制腫瘤生長(圖7H)。
結論:
我們證明了UCHL3是一種YAP去泛素化酶,通過其去泛素化活性穩定YAP,促進腫瘤生長、轉移和腫瘤干性。我們的研究結果為UCHL3在Hippo信號通路中的作用提供了新的見解,并提示UCHL3可能被證明是治療ATC的潛在靶點。
參考文獻:
Tang J, Yang Q, Mao C, Xiao D, Liu S, Xiao L, Zhou L, Wu G, Tao Y. The deubiquitinating enzyme UCHL3 promotes anaplastic thyroid cancer progression and metastasis through Hippo signaling pathway. Cell Death Differ. 2023 Feb 22. doi: 10.1038/s41418-023-01134-z.






