抑制線粒體蛋白OPA1可抑制乳腺癌的生長
線粒體融合和裂變蛋白已被提名為癌癥的藥物靶點。而由于三陰性乳腺癌(TNBC)幾乎總是發生化療耐藥性,它們的抑制作用對TNBC是否有效尚不清楚。目前,有研究發現靶向抑制線粒體融合蛋白OPA1可抑制TNBC的生長,并將OPA1指定為TNBC中的藥物靶點。該研究發表在《Journal of Experimental & Clinical Cancer Research》,IF:11.161。
技術路線:
主要研究結果:
1.乳腺癌中OPA1水平升高與預后差有關
作者首先在TNMplot數據庫中比較了OPA1, MFN1和MFN2在健康組織和腫瘤組織中的表達。分析表明,在融合基因中,OPA1在AML、乳腺癌、結腸癌、食管癌、肺癌、卵巢癌、胰腺癌、直腸癌、腎癌、胃癌、睪丸和子宮癌組織中顯著過度表達(圖1a)。同樣, OPA1 mRNA在乳腺癌中上調(圖1b),不同乳腺癌亞型之間沒有任何差異(圖1c),而MFN1和MFN2差異不明顯。另外,OPA1水平越高,乳腺癌預后越差(圖1d),MFN1表達水平也與較差的預后相關,而MFN2表達水平與預后無關。這些分析表明,在乳腺癌中,當這兩個線粒體融合基因水平降低時,OPA1和MFN1上調,預后更差,而MFN2水平降低,但與不同的預后無關。
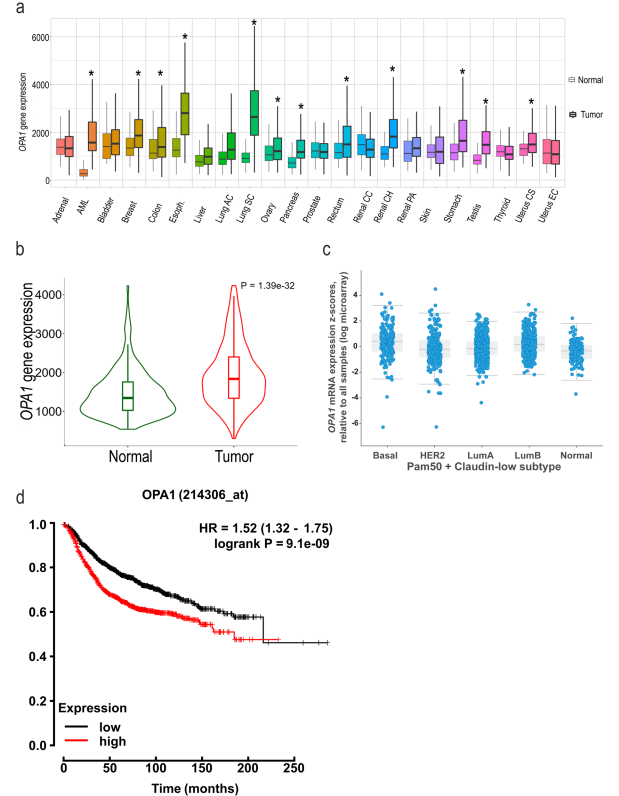
圖1 OPA1在乳腺組織中過表達
2.OPA1是乳腺癌細胞多種癌癥特征所必需的
鑒于MFNs的水平與較差的乳腺癌預后有明確的關聯,作者選擇研究OPA1在乳腺癌中的作用上。作者選OPA1兩種不同的siRNA研究對MDA-MB-231影響(圖2a,b),發現siRNA-OPA1減少了MDA-MB-231細胞遷移能力(圖2c-f),降低了細胞增殖(圖2g)、侵襲(圖2h-i)和纖維連接蛋白的粘附(圖2j),而不影響細胞在明膠上的粘附(圖2k),且CrispR/ Cas9生成的MDA-MB-231 OPA1敲除細胞株(MDA-MB-231 OPA1 -/-)也得到了驗證。在其他乳腺癌亞型中,沉默OPA1也抑制了其他乳腺癌細胞的遷移、增殖和粘附(圖2l-q)。另外,無毒劑量的MYLS22(OPA1抑制劑)可以抑制乳腺癌細胞的遷移、增殖和粘附(圖3a-f)。這些結果表明,基因或藥理抑制OPA1可降低乳腺癌細胞的增殖、遷移和侵襲能力。
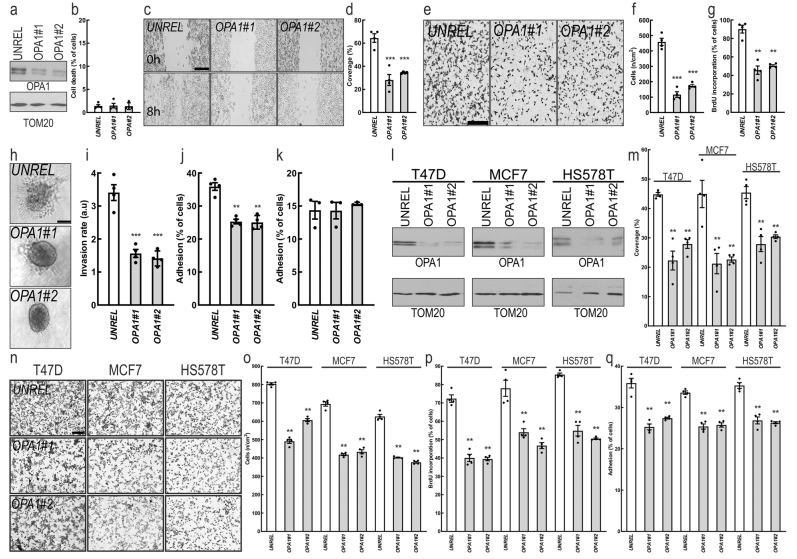
圖2 OPA1是乳腺癌細胞特征所必需的
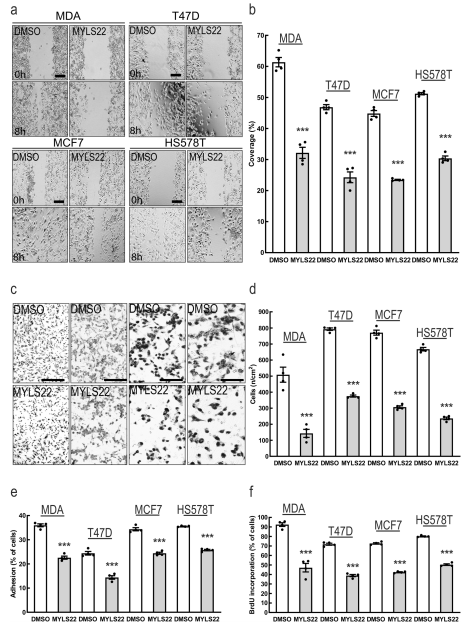
圖3 體外研究表明,藥理抑制OPA1可以降低乳腺癌的特征
3.OPA1消融會損害乳腺癌體內生長
下一步研究TNBC細胞在體內生長是否需要OPA1。將MDA-MB-231 OPA1 -/-和MDA-MB-231 OPA1 -/-:OPA1原位植入6周齡NOD-SCID小鼠的乳腺。結果發現,沒有觀察到MDA-MB-231 OPA1 -/-細胞的生長,和MDA-MB-231 OPA1 -/-:OPA1的移植和生長(圖4a)。為了避免植入問題,將MDA-MB-231 OPA1 -/-和MDA-MB-231 OPA1 -/-:OPA1細胞植入母體基質細胞 (3/8 engrafted MDA-MB-231 OPA1 -/- vs. 8/8 MDA-MB-231 OPA1 -/-:OPA1),但由于37.5%的植入物附著,可以比較MDA-MB-231 OPA1 -/-與MDA-MB-231 OPA1 -/-:OPA1移植物幾乎為零的腫瘤生長(圖4b,c)。一段時間后,移植腫瘤并測量細胞周期蛋白D(Cyclin D),與MDA-MB-231 OPA1 -/-相比,MDA-MB-231 OPA1 -/-:OPA1中幾乎沒有Cyclin D (圖4d)。此外,當通過乳腺癌免疫染色觀察內皮標記物CD31的腫瘤血管時,發現MDA-MB-231 OPA1 -/-腫瘤中血管直徑減少而血管數量沒有減少(圖4e-g)。這些數據表明,急性抑制OPA1可以抑制腫瘤的生長。因此,后續建立一個原則性實驗來驗證急性藥物OPA1抑制是否可以抑制腫瘤生長。MDA-MB-231被原位植入乳腺,21天后,每隔一天通過瘤周注射10 mg/kg MYLS22進行分娩,發現足以抑制MDA-MB-231腫瘤的生長(圖4h-i)。因此,靶向抑制OPA1可以有效減弱體內乳腺癌的生長。

圖4 基因或藥理抑制OPA1抑制腫瘤生長
4.MicroRNA圖譜鑒定了OPA1抑制后上調的miRNA
進一步研究OPA1調控乳腺癌的分子機制。首先發現,基因或藥理抑制OPA1可誘導MDA-MB-231細胞線粒體破碎(圖5a-g),但在OPA1沉默和OPA1消融的MDA-MB-231細胞中,線粒體膜電位、ATP水平和線粒體呼吸沒有受到影響(圖5 h-j)。有多篇文獻已報道在乳腺癌中,已經發現了幾種miRNAs可以調節由OPA1缺失引起的相同的生物學效應。因此,作者通過miRCURY LNA Cancer Focus PCR Panel對miRNA進行了分析,以研究OPA1缺失是否影響了miRNA的表達。最終發現對照和去除OPA1中84個miRNA中只有6個差異表達(圖6a)。結合miR-148a-3p和miR-152是上調量最高的兩個miRNAs,并屬于同一個miRNA148/152家族:MiR-148/152家族的成熟成員長度為21-22個核苷酸,相同的種子序列為6-7個核苷酸(圖6b)。qPCR證實,在所有測試的乳腺癌細胞類型中,隨著OPA1下調或藥理抑制,miRNAs-148a、148b和152的水平都有所增加(圖6c-h)。在MDA-MB-231 OPA1+/+細胞中過表達OPA1時(MDA-MB-231 OPA1 OPA1+/+:OPA1),這些miRNA的水平進一步降低(圖6i-k)。總之,這些結果表明,148/152家族的miRNAs水平與OPA1呈負相關。

圖5體外切除OPA1不影響乳腺癌細胞線粒體代謝
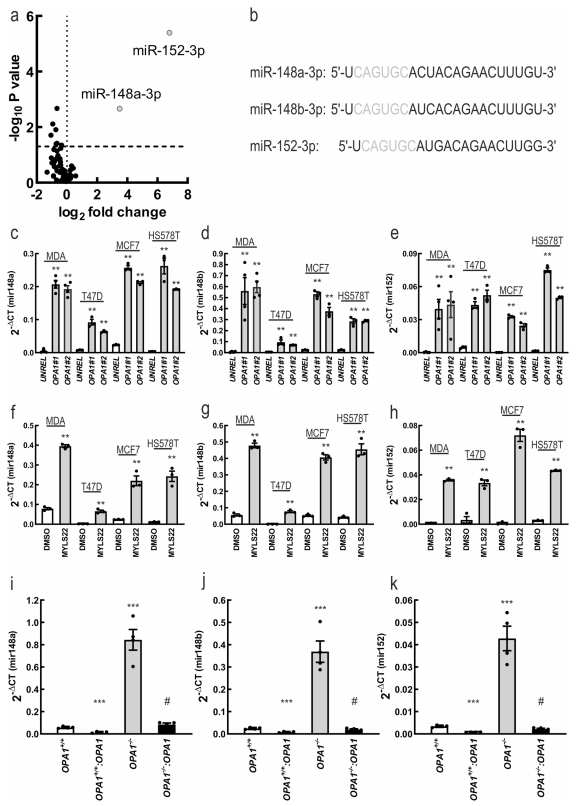
圖6 OPA1消融提高miR-148a、miR-148b和miR-152表達水平
5.148/152家族的miRNAs介導MDA-MB-231細胞中OPA1下調的作用
為了確定miR-148a、148b和152過表達是否可以解釋MDA-MB-231細胞中OPA1下調的表型,首先通過miRpaths (microT-CDS)分析了這三種miRNAs表達水平變化可能干擾的信號通路和細胞功能:miR-148a、148b和152具有調控RAS和PI3K/AKT信號通路的潛能。此外,miR-148a、148b和152還可以控制細胞外基質(ECM)與受體的相互作用、局灶性粘連和聚糖降解作用(圖7a)。實驗分析表明,這些miRNA的過表達降低了MDA-MB-231細胞的遷移、增殖和粘附(圖7b-d),降低了CYCLIN D2和D3, INTEGRIN-β mRNA和蛋白的水平,從而降低了ERK磷酸化(圖7e)。相反,沉默miR-148a、miR-148b或miR-152可以拯救沉默了OPA1的乳腺癌細胞的遷移、增殖和粘附(圖7f-t)。這些結果證實了148/152家族的miRNAs在乳腺癌細胞中作為OPA1沉默的媒介的作用。
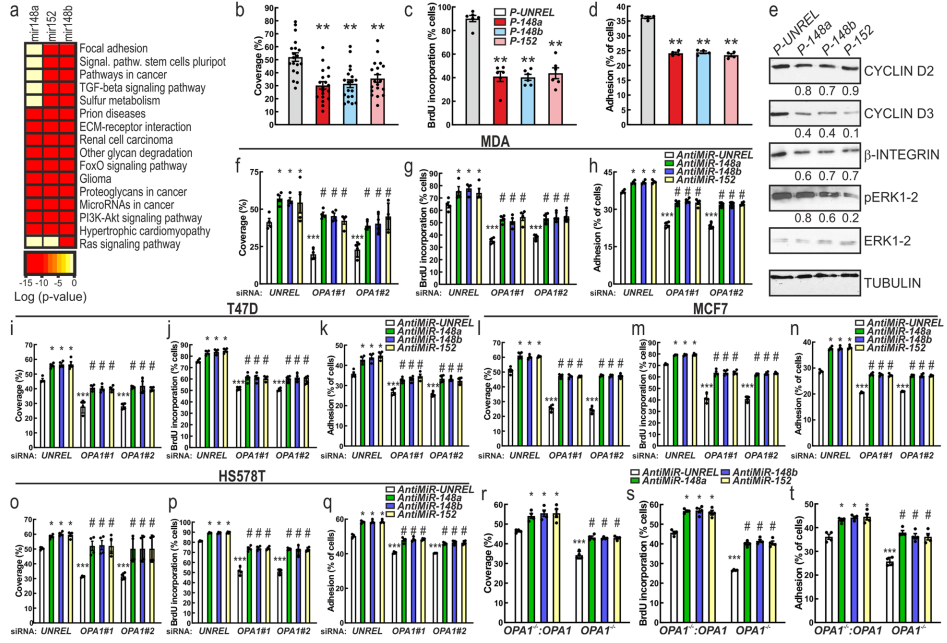
圖7 OPA1消融通過增加miRNA 148a、148b和152的表達來抑制乳腺癌細胞的特征
結論:
總之,作者證明了OPA1在乳腺癌中高表達,而其水平與較差的預后相關。多種實驗證實,抑制OPA1可以抑制腫瘤生長、侵襲性和新生血管的形成,抑制TNBC在體外和體內的生長。確定了OPA1在調節148/152家族miRNAs表達中的作用,這是OPA1在調節乳腺癌特征中的上位性作用。該研究將OPA1作為癌癥治療提供了一個潛在靶點。
參考文獻:
Zamberlan M, Boeckx A, Muller F, Vinelli F, Ek O, Vianello C, Coart E, Shibata K, Christian A, Grespi F, Giacomello M, Struman I, Scorrano L, Herkenne S. Inhibition of the mitochondrial protein Opa1 curtails breast cancer growth. J Exp Clin Cancer Res. 2022; 41:95.






