FGF21減輕鐵過量引起的肝損傷和纖維化
鐵死亡在一些疾病中發揮作用,如鐵過量引起的肝臟疾病。鐵死亡已成為一種潛在的治療相關疾病的策略。許多抗氧化劑已被證實可以控制鐵死亡,但調控鐵死亡的細胞自主機制仍不清楚。在本研究中,我們發現鐵過量通過過度誘導HO-1表達促進了肝細胞鐵死亡,促進了肝損傷和纖維化的進展,并伴有體外和體內FGF21蛋白水平的上調。重組FGF21和FGF21過表達都能通過抑制鐵死亡顯著保護鐵過量誘導的肝細胞線粒體損傷、肝損傷和纖維化。相反,FGF21的缺失加重了鐵過量誘導的鐵死亡。值得注意的是,FGF21誘導的HO-1抑制和NRF2激活為這一現象提供了機制解釋。綜上所述,我們確定FGF21是一種新的鐵死亡抑制因子。FGF21激活可能為鐵過量誘導的鐵死亡相關疾病的潛在治療提供了一種有效的策略。本文于2021年9月發表在“Redox Biology”(IF: 11.799)期刊上。
技術路線

結果
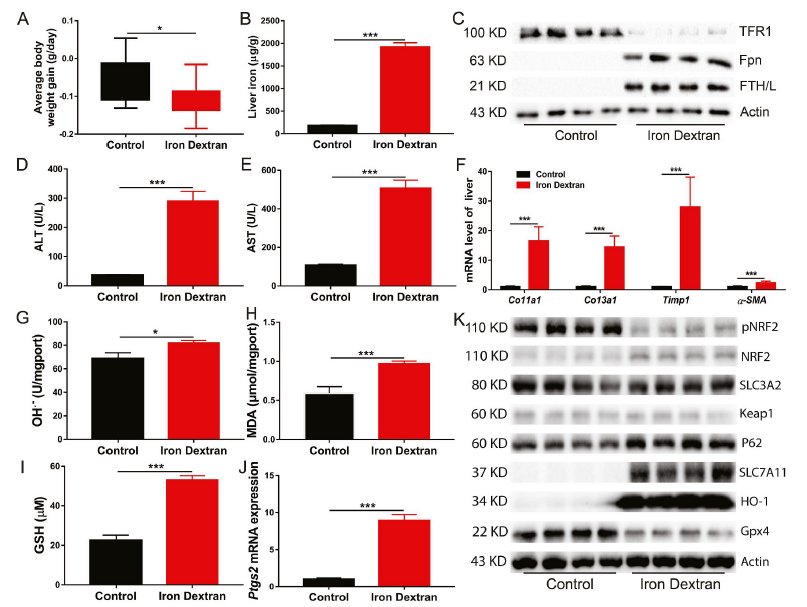
雖然鐵是幾乎所有生物必需的微量營養素,但其高氧化還原活性可能是活性氧的來源,使鐵具有潛在的細胞毒性。右旋糖酐鐵注射導致體重下降(圖1A),鐵在肝臟(圖1B)中積累。與對照組相比,右旋糖酐鐵注射組的鐵代謝相關基因、蛋白和血液學參數明顯改變,表現為Hamp1、Fth、Ftl和Fpn表達上調,Tfr1表達下調(圖1C)。此外,右旋糖酐鐵注射導致肝損傷(圖1D和E)和纖維化(圖1F)。鐵過量可誘導肝臟中羥基自由基(OH.?)、MDA(脂質過氧化產物)和谷胱甘肽(GSH)的積累(圖1G-I)。鐵過量顯著增加了鐵死亡相關基因Ptgs2的mRNA表達(圖1J)。我們還發現鐵過量強烈地抑制了NRF2的磷酸化并降低GPX4蛋白的表達水平,可能導致原代肝細胞和小鼠肝臟中ROS清除能力受損(圖1K)。相比之下,鐵過量顯著上調了原代肝細胞和小鼠肝臟中的SLC7A11和HO-1蛋白水平(圖1K)。這些結果表明鐵過量導致鐵死亡,這可能導致隨后的肝損傷和纖維化。
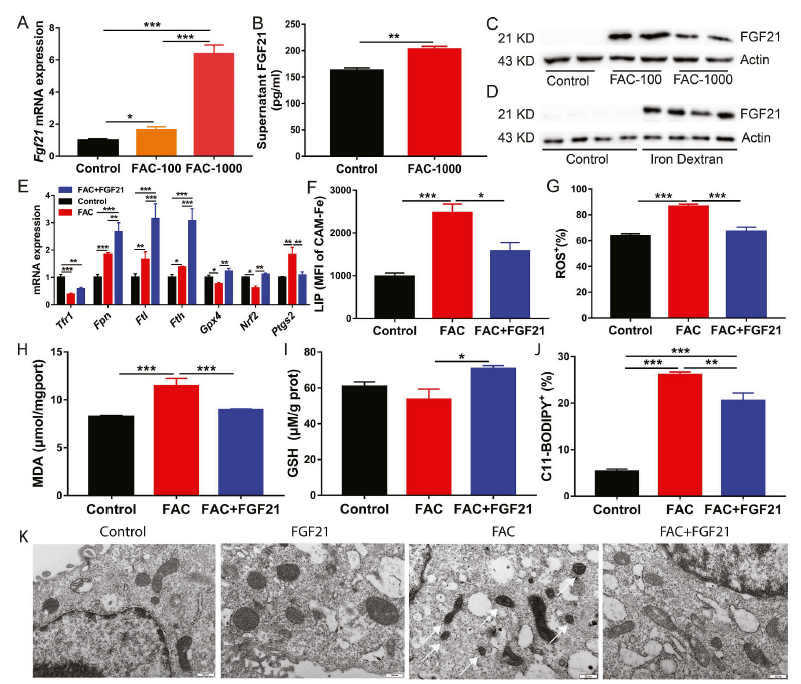
FGF21被認為是一種緩解氧化應激的因子。因此,在鐵過量條件下,我們檢測了原代肝細胞和小鼠肝臟中FGF21的mRNA和蛋白水平。100 μM或1000 μM FAC處理原代肝細胞24 h后,與對照組相比,FGF21 mRNA和蛋白表達水平顯著升高(圖2A-C)。與體外實驗結果一致的是,鐵過量顯著增強了右旋糖酐鐵注射小鼠肝臟中FGF21蛋白的表達(圖2D)。
為了確定FGF21激活在鐵過量誘導的鐵死亡中的作用,將FGF21重組蛋白添加到添加了1000 μM FAC的原代肝細胞培養基中。研究發現,與單獨的FAC處理相比,FGF21處理進一步上調了Fpn、Fth和Ftl的mRNA表達。此外,FGF21的添加挽救了鐵過量導致的Nrf2和Gpx4 mRNA表達的下降(圖2E)。FGF21下調鐵過量誘導的鐵死亡相關基因Ptgs2的mRNA表達(圖2E)。這些結果表明FGF21可能通過改變細胞鐵代謝和氧化還原平衡來抑制鐵死亡。流式細胞術結果證實了這一發現。在FGF21處理的原代肝細胞中,FGF21降低了細胞內LIP、ROS、MDA和脂質過氧化水平,但增加了GSH,這可能有助于抑制鐵過量誘導的鐵死亡(圖2F-J)。此外,與對照組肝細胞相比,FAC處理的肝細胞有更小、破裂的線粒體。通過FGF21治療,可以完全挽救FAC誘導的線粒體損傷和形態學改變(圖2K)。
3)FGF21基因敲低可誘導氧化應激,加重鐵過量所致的鐵死亡
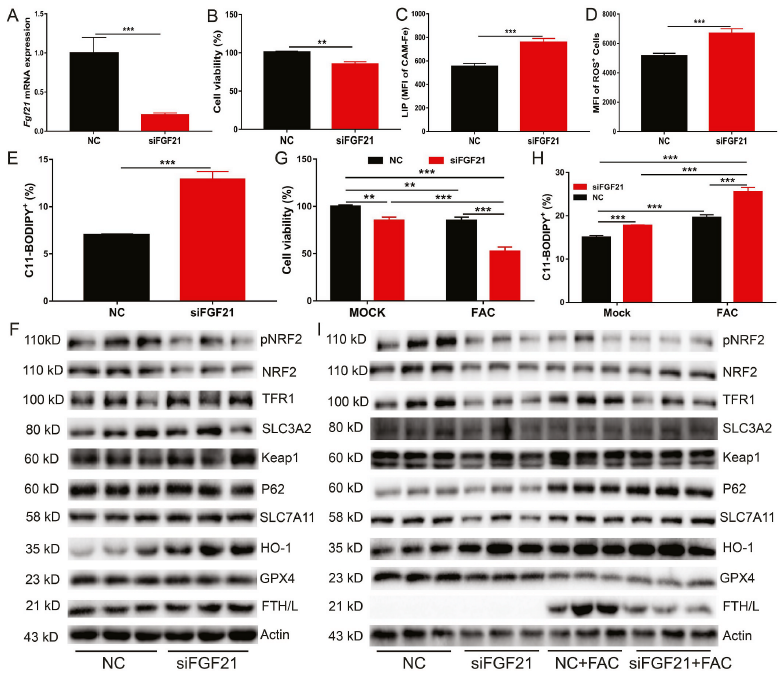
為了進一步闡明FGF21在鐵過量誘導的鐵死亡中的作用,我們使用FGF21 siRNA下調了原代肝細胞中的FGF21(圖3A)。與重組FGF21蛋白處理或腺病毒介導的FGF21過表達相比,FGF21敲低顯著損害了細胞活力(圖3B),并顯著增加了細胞內LIP、ROS和C11-BODIPY水平(圖3C-E)。FGF21敲低也抑制NRF2的磷酸化以及NRF2和GPX4的蛋白表達。相比之下,FGF21的敲除顯著增加了HO-1蛋白的表達(圖3F)。隨后,將FGF21敲除的原代肝細胞用1000 μМ FAC處理24小時,發現與對照細胞相比,FGF21敲除細胞的鐵死亡增加(圖3G和H)。經FAC處理后HO-1蛋白水平進一步升高。然而,在FGF21敲低的原代肝細胞中,添加FAC降低了FTH/L蛋白的表達(圖3I)。綜上所述,這些結果表明FGF21是一種新的鐵死亡抑制因子。
4)重組FGF21蛋白挽救了FGF21基因敲低誘導的鐵死亡
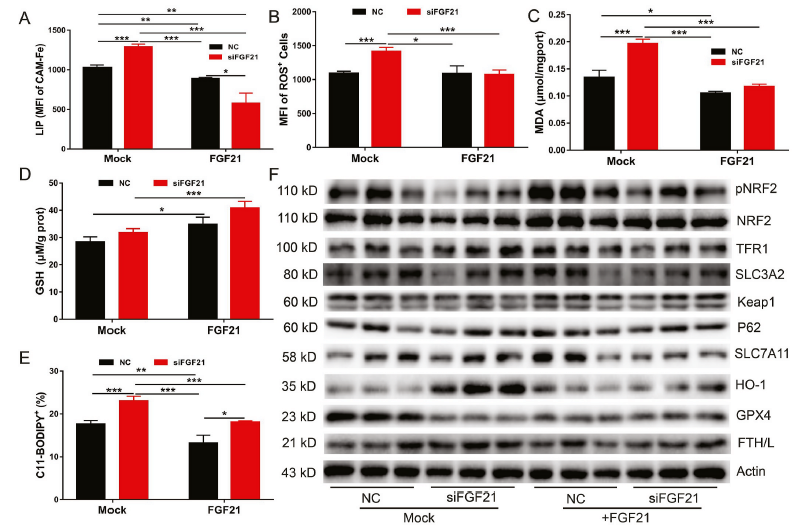
我們采用外源性FGF21治療研究其是否可以減輕FGF21基因敲低引起的鐵死亡。我們將FGF21基因敲低的原代肝細胞用200 ng/ml FGF21重組蛋白處理24 h,然后通過檢測LIP、ROS和脂質過氧化(C11-BODIPY)水平來評估肝細胞的鐵死。如預期的那樣,外源性FGF21治療完全挽救了FGF21基因敲減引起的鐵死亡,降低了細胞內LIP、ROS、脂質過氧化和MDA水平,但增加了GSH(圖4A-E)。與我們之前的研究結果一致,FGF21處理增加了正常和FGF21敲低原代肝細胞的NRF2磷酸化和總NRF2蛋白水平。有趣的是,外源性FGF21治療可以逆轉FGF21敲低的原代肝細胞HO-1蛋白水平的升高(圖4F)。
5)FGF21過表達通過抑制鐵死亡保護小鼠免受鐵過量誘導的肝損傷和纖維化
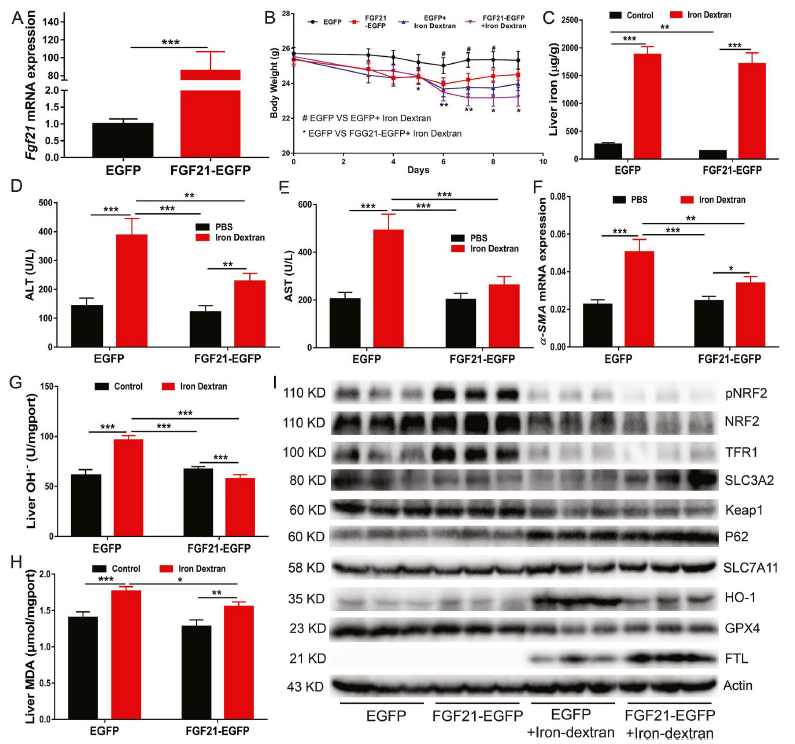
為了進一步闡明FGF21在鐵過量誘導的鐵死亡中的作用,我們利用重組腺病毒表達系統構建了肝臟中過表達FGF21的小鼠模型。與對照組相比,FGF21過表達小鼠的肝臟中FGF21 mRNA水平大約增加了80倍(圖5A)。FGF21過表達減弱鐵過量誘導的體重減輕(圖5B)。出乎意料的是,與給予PBS的EGFP對照組小鼠相比,肝臟FGF21過表達小鼠的血清和肝臟鐵含量降低(圖5C)。對TFR1蛋白水平(圖5I)的評估也顯示,FGF21過表達改善了WT小鼠的鐵代謝。然而,在給予右旋糖酐鐵后,WT和過表達FGF21小鼠之間的鐵代謝差異消失了(圖5C)。隨后,研究發現FGF21過表達可降低鐵過量小鼠的血清ALT和AST水平(圖5D和E),并減輕肝損傷和纖維化(圖5F)。此外,FGF21過表達也降低了肝臟中的OH-和MDA水平(圖5G和H)。肝臟中FGF21過表達降低了PBS給藥小鼠HO-1的表達,增加了FTH/L的表達(圖5 I)。這些結果表明FGF21過表達可以通過抑制WT小鼠的鐵死亡來保護小鼠免于鐵過量誘導的肝損傷和纖維化。
6)FGF21通過促進HO-1泛素化和降解來減輕鐵死亡
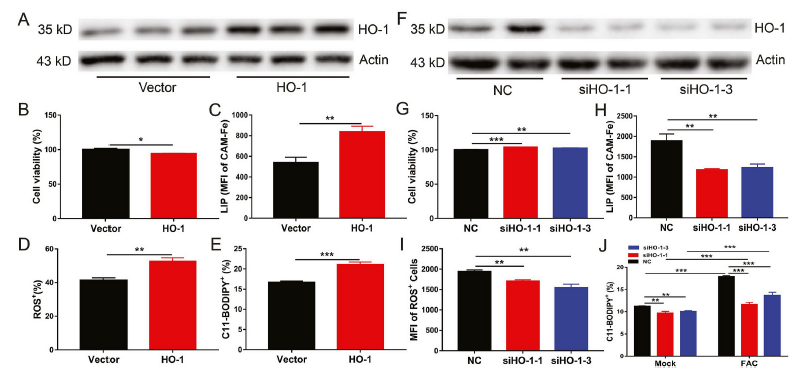
為了闡明FGF21介導的HO-1抑制在肝細胞保護鐵死亡的作用,我們將表達HO-1的質粒轉染原代肝細胞(圖6A)。HO-1過表達可增加細胞死亡和細胞內LIP、ROS和脂質過氧化水平(圖6B-E)。與此觀察相一致的是,即使在鐵過量的情況下,HO-1敲低也能降低原代肝細胞鐵死亡和細胞內LIP、ROS和脂質過氧化水平(圖6F-J)。這些結果表明HO-1是肝細胞內鐵死亡的激活因子。
為了揭示FGF21調控HO-1蛋白水平的潛在機制,我們分析了FGF21過表達小鼠的肝臟(圖7A)和FGF21處理的原代肝細胞(圖7B)中HO-1 mRNA的表達水平。FGF21沒有改變HO-1 mRNA的表達水平,表明FGF21以轉錄獨立的方式抑制HO-1的表達。接下來,我們使用氯己亞胺(CHX,一種化學蛋白合成抑制劑)來評估FGF21介導的HO- 1蛋白表達下調的轉錄獨立機制。研究發現FGF21影響HO-1蛋白的穩定性,FGF21的處理縮短了HO-1的半衰期,從而加速了其降解(圖7C)。隨后,FGF21也被發現促進HO-1泛素化。與載體對照相比,FGF21過表達增加了HEK293T細胞中HA標記的HO-1蛋白的泛素化(圖7D)。綜上所述,這些發現表明FGF21通過促進HO-1的泛素化和降解來減弱鐵過量誘導的鐵死亡。
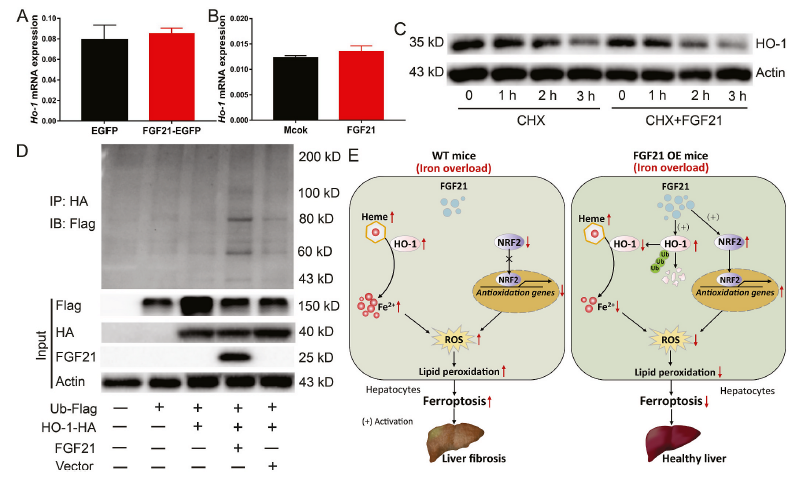
結論:構成性HO-1活化是鐵過量誘導肝細胞鐵死亡的一種新介質,FGF21可以通過刺激HO-1泛素化和隨后的降解來保護肝細胞免受鐵過量誘導的鐵死亡。FGF21-HO-1途徑可用于治療鐵過量誘導的鐵死亡相關疾病。
參考文獻:
Wu A, Feng B, Yu J, Yan L, Che L, Zhuo Y, Luo Y, Yu B, Wu D, Chen D. Fibroblast growth factor 21 attenuates iron overload-induced liver injury and fibrosis by inhibiting ferroptosis. Redox Biol. 2021 Oct;46:102131. doi: 10.1016/j.redox.2021.102131. Epub 2021 Sep 11. PMID: 34530349; PMCID: PMC8445902.






