腸道菌群——國自然研究又一熱點
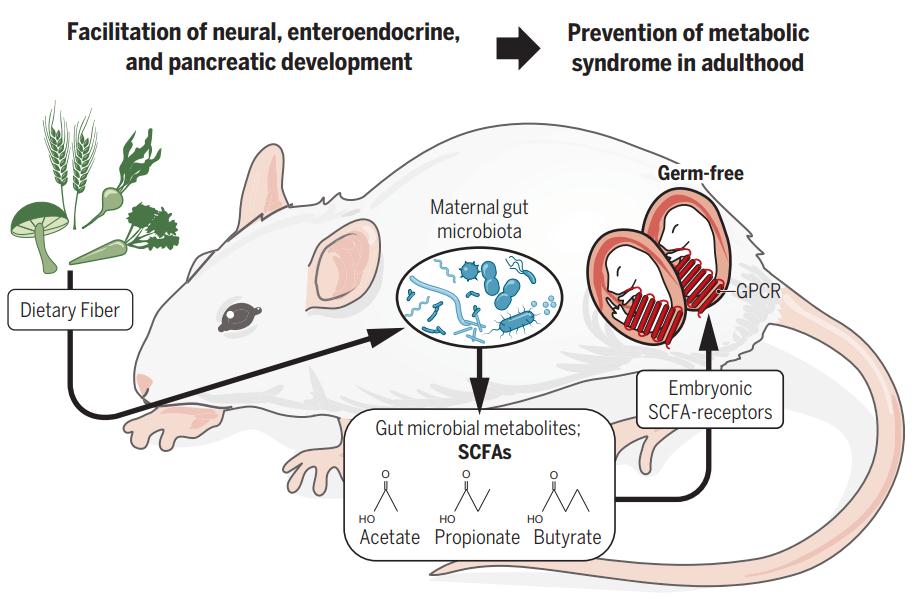
腸道菌群作為寄居在人體腸道內的微生物群落,是近年來微生物學、醫(yī)學、基因學等領域最引人關注的研究焦點之一。隨著抗生素的迅速使用和高熱量、低纖維飲食的攝入導致腸道微生物群落紊亂,使人類易患代謝綜合征等多種疾病。雖然已有大量的研究致力于微生物群對個體出生后的環(huán)境影響,但是作者對于胚胎期腸道微生物群的作用卻知之甚少。然而,2020年2月28日,日本東京農工大學Ikuo Kimura、慶應大學Koji Hase等研究人員在science上在線發(fā)表了題為“Maternal gut microbiota in pregnanc influences offspring metabolic phenotype in mice“的研究性論文,該研究發(fā)現了孕期母體微生物群對后代的肥胖具有抵抗力,進一步揭示了妊娠期間母體腸道環(huán)境影響后代代謝的具體機制。

結果一、GF母親的后代與肥胖癥的發(fā)展
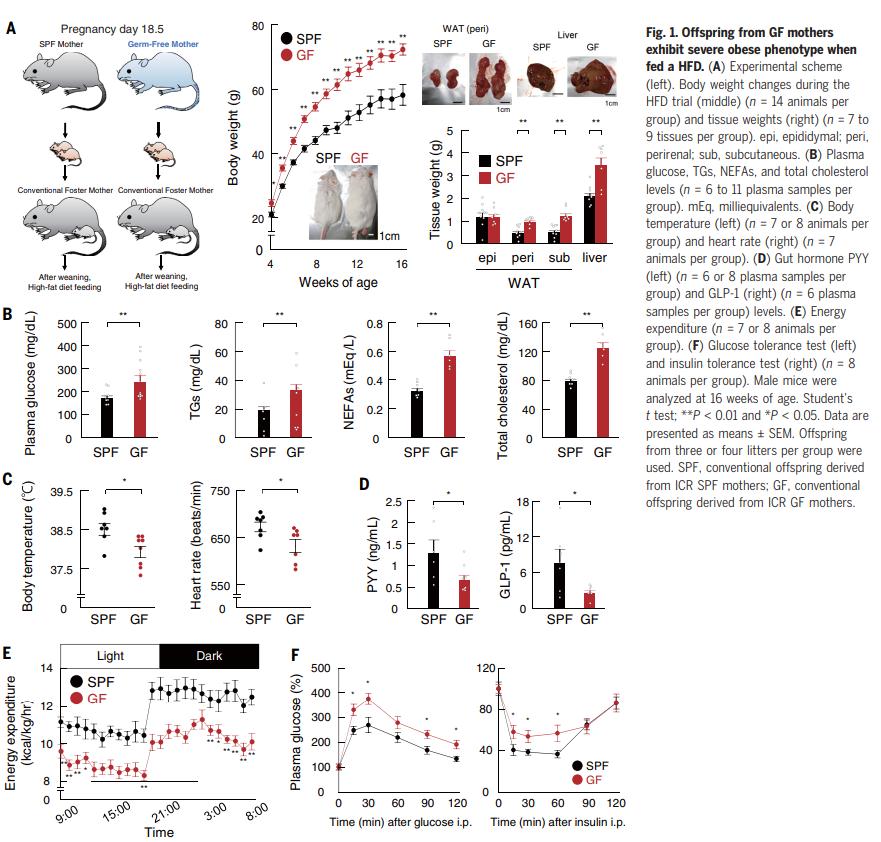
為了研究懷孕期間母體腸道菌群對后代的影響,在SPF和GF條件下繁殖了懷孕的小鼠。在妊娠的第18.5天,懷孕的GF小鼠從相應菌株的SPF小鼠接受了糞便微生物菌群移植,以防止不利微生物過度生長。寄養(yǎng)母親在常規(guī)條件下飼養(yǎng)新生動物,以適應出生后的生長環(huán)境。斷奶后,給雄性小鼠喂食高脂飲食(HFD)以誘導肥胖(圖1A)。結果表明,GFD后代在HFD喂養(yǎng)后表現出肥胖表型。為了支持這種解釋,GF后代中HFD誘導的葡萄糖耐量和胰島素抵抗顯著加速,表明胰島素敏感性受損。因此,或多或少地普遍觀察到GF后代的代謝紊亂,而與菌株和性別無關。
結果二、感知胚胎中的母體SCFA
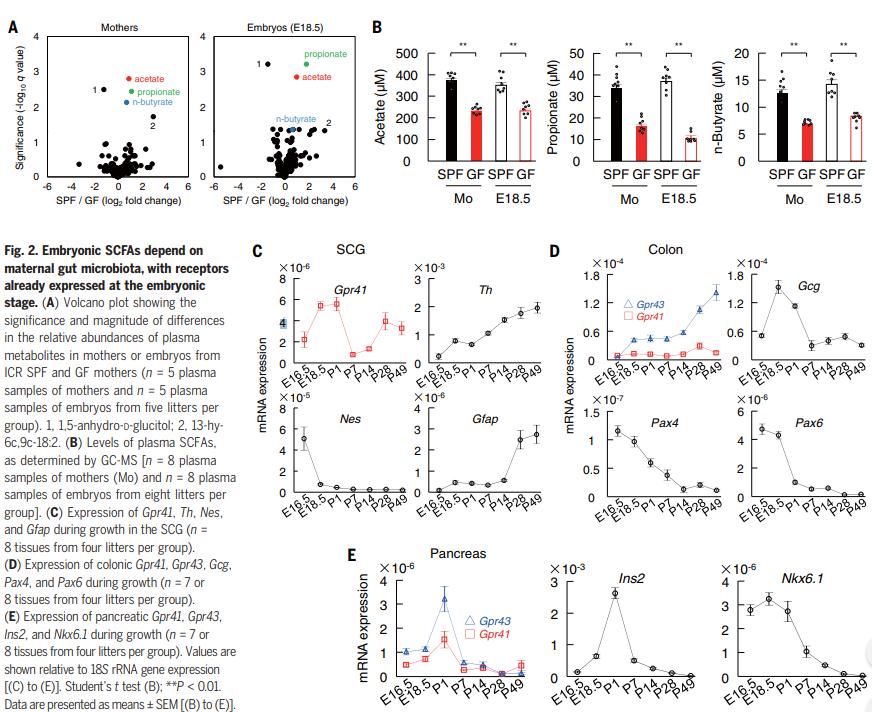
作者在小鼠懷孕期間分析了SPF和GF ICR母親及其胚胎中親水和親脂代謝產物的血漿水平,只有5種代謝物對繁殖條件的反應在母體和胚胎中表現出相似的變化(圖2A)。特別是,GF母親和胚胎的血漿SCFA水平顯著低于SPF對應物(圖2B)。作者在胚胎交感神經節(jié)中檢測到Gpr41 mRNA(圖2C)在胚胎和成年階段具有雙相表達(圖2C)。結果表明,胚性代謝組織,如交感神經系統(tǒng),腸道和胰腺,可能通過表達GPR41和GPR43來感知母體腸道微生物衍生的SCFA。
結果三、通過GPR41進行同情發(fā)展
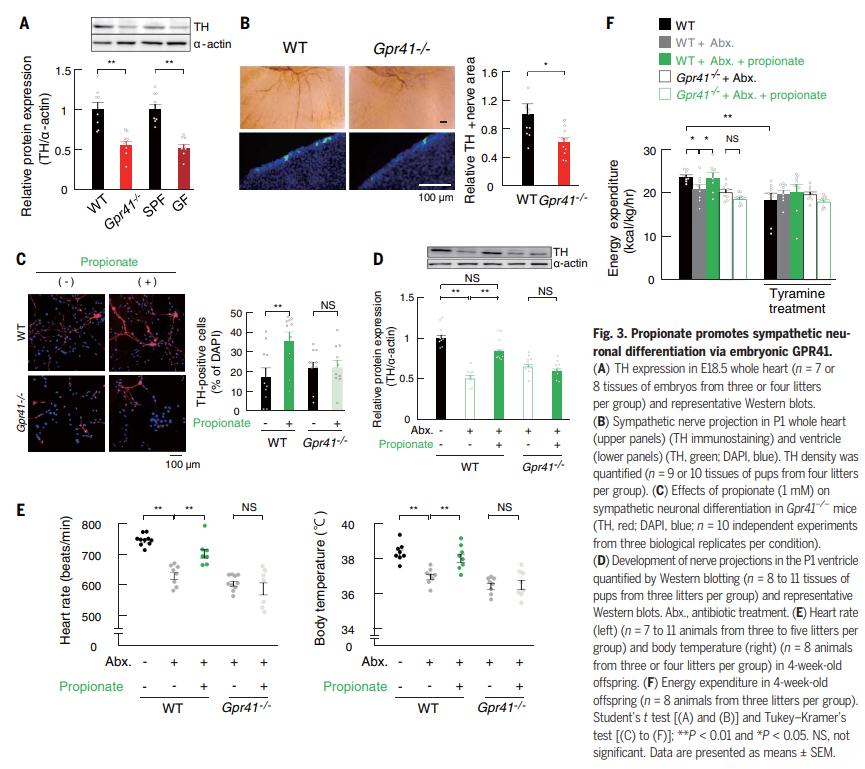
作者進一步研究了GPR41在交感神經系統(tǒng)中的功能以及GPR43在腸道和胰腺胚胎發(fā)育過程中的功能。作者發(fā)現與野生型(WT)胚胎相比,Gpr41-/-C57BL / 6J胚胎在心臟的交感神經投射明顯減少,并且在具有相同背景的GF胚胎中這種異常也很明顯(圖3A) 。此外,在出生后第1天(P1),Gpr41-/-幼崽向心臟的交感神經投射明顯減少,即使這些幼崽是從SPF條件下維持的母親分娩的(圖3B)。propionic acid誘導的交感神經元分化在來自Gpr41-/-胚胎的交感神經細胞中被消除(圖3C)。這些發(fā)現強烈表明propionic acid介導的GPR41活化促進交感神經元分化。為了驗證這一觀點,作者用抗生素混合物處理了WT懷孕小鼠,以消除腸道菌群。在P1上,經抗生素處理的小鼠的幼崽向心臟的交感神經投射明顯減弱。值得注意的是,在懷孕期間服用propionic acid可改善這種異常(圖3D)。斷奶后的心律和體溫是交感神經投射的指標,與耗氧量相似(圖3,E和F)。用酪胺治療顯著降低了未經治療或經propionic acid或抗生素治療的WT母親的后代的耗氧量,而這些影響在經過抗生素治療的WT母親或未經治療的Gpr41-/-母親的后代中減弱了(圖3F)。基于這些觀察,作者認為來自母體腸道菌群的propionic acid可通過GPR41促進交感神經的發(fā)育,如在GF的后代中觀察到的,propionic acid的缺乏導致交感神經功能障礙,包括體溫和心率波動的降低。
結果四、通過GPR43調節(jié)胚胎胰島素
作者研究了GPR43在胚胎期對腸內分泌細胞分化的影響。與WT胚胎相比,Gpr43-/-C57BL / 6J胚胎的結腸中Pax4和Pax6明顯上調(圖4A)。PMP是一種比乙酸酯或butyrate更有效的GPR43配體(EC50:?30 mM)可顯著促進WT小腸類器官中GLP-1 +腸內分泌細胞的分化。胚胎(圖4,B和C),這種作用在來自Gpr43-/-胚胎的類器官中消失了(圖4,B和C)。與WT和SPF小鼠相比,Gpr43-/-和GF小鼠胚胎的胰腺中Nkx6.1明顯上調,而Gpr43-/-和GF小鼠的Ins2表達和胰島素水平下調(圖4D)。盡管WT和Gpr43-/-母親之間沒有差異,但Gpr43-/-胚胎中的血漿胰島素水平明顯低于WT胚胎(圖4F)。作者推測在產前期缺乏SCFA-GPR43信號轉導會導致成年期代謝綜合征,最可能的原因是能量消耗降低胚胎體內的穩(wěn)態(tài)。
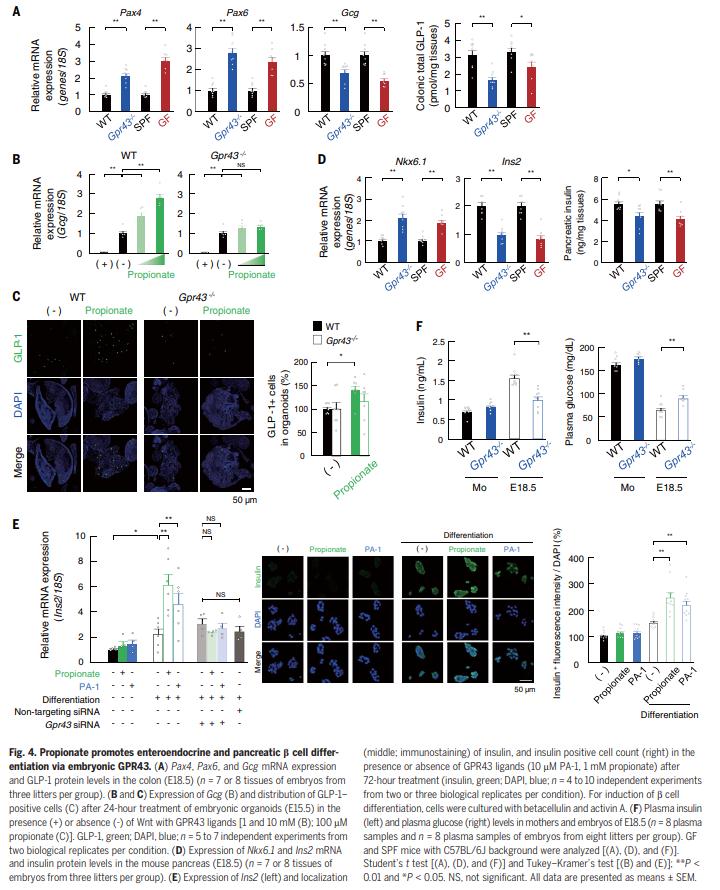
結果五、懷孕期間的膳食纖維攝入量
為了提供SCFA在肥胖抵抗力發(fā)展起源中的重要性的進一步證據,作者進行了一項飲食干預研究,在該飲食干預研究中,對懷孕的ICR小鼠在常規(guī)條件下飼喂高纖維(HFi)或低纖維(LFi)飲食檢查了他們的后代對肥胖的易感性(圖5A)。結果表明膳食纖維的微生物發(fā)酵有助于抑制肥胖。與LFi后代相比,HFi后代的血漿代謝參數也得到了改善(圖5B)。在HFi后代中,LFi后代的交感神經功能障礙,例如體溫降低和心率波動降低,得到改善(圖5C)。而由PMP喂養(yǎng)的母親及其胚胎中通常有4種代謝物增加(圖5D)。在這4種代謝產物中,SCFA是SPF與GF和LFi與HFi的比較中唯一的共同因素。用PMP喂養(yǎng)的小鼠的胚胎(HFi胚胎)中的SCFA水平顯著高于使用LFi喂養(yǎng)的小鼠的胚胎(LFi胚胎)(圖5E)。作者還觀察到,HFi胚胎中的血漿胰島素水平顯著高于LFi胚胎(圖5F),因此HFi胚胎中的血漿葡萄糖水平顯著降低(圖5F)。因此,由母體腸道菌群通過膳食纖維的發(fā)酵產生的SCFA通過母體循環(huán)提供給胚胎,從而改善胎兒的葡萄糖穩(wěn)態(tài),并賦予后代抵抗肥胖的能力。
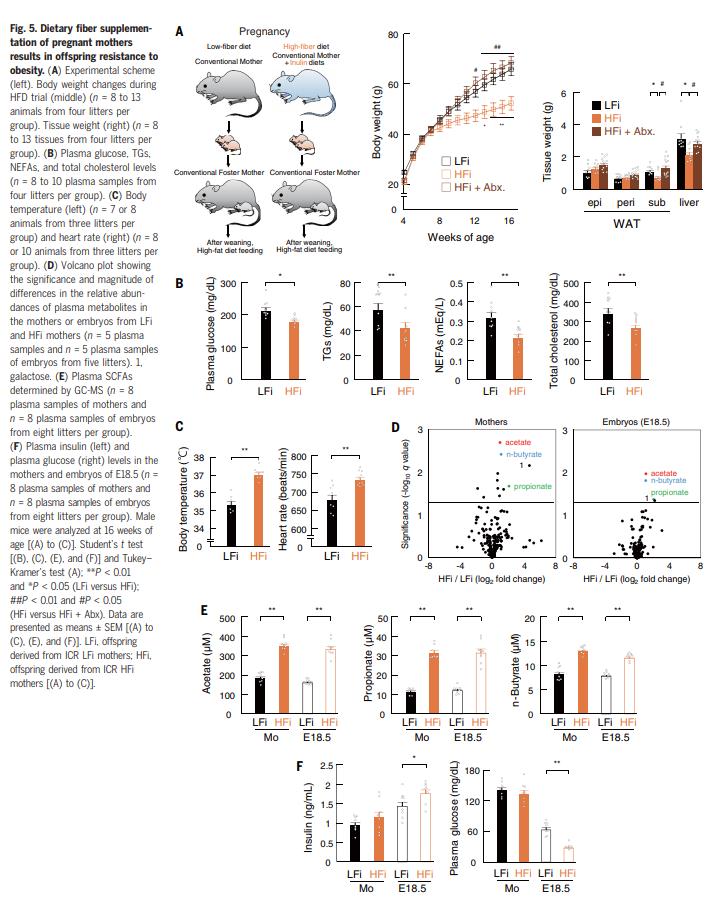
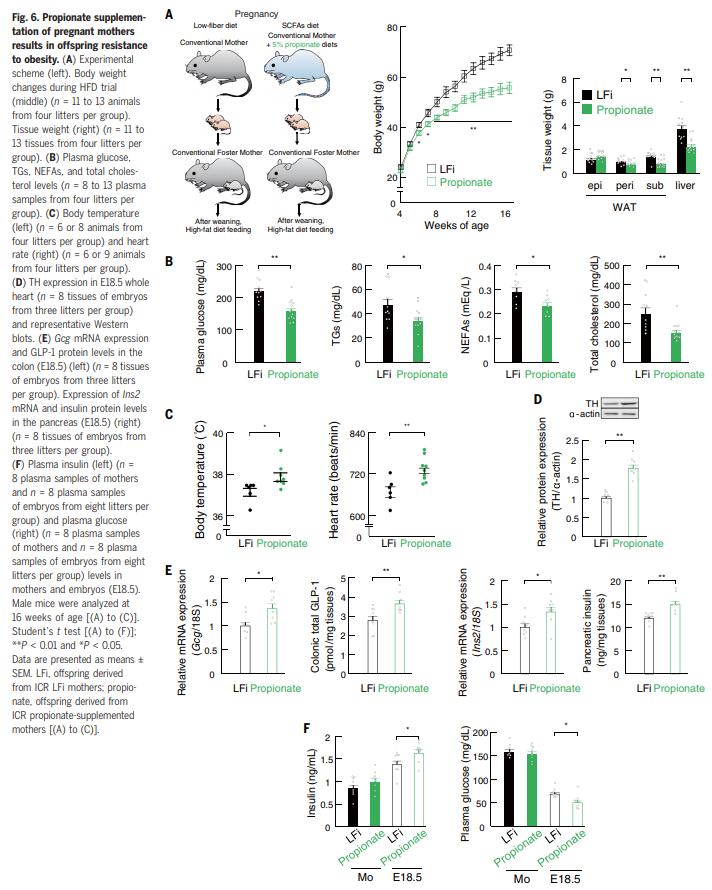
結果六、懷孕期間補充SCFA
考慮到測定值優(yōu)于其EC50值,HFi胚胎中的血漿propionic acid水平可能足以激活GPR41和/或GPR43受體(圖5E)。因此,為了嚴格檢驗PMP在后代肥胖抵抗中的作用,作者給懷孕的ICR小鼠喂食了補充PMP的LFi飲食(圖6A)。PMP治療可抑制HFD誘導的成年后代體重,腎周或皮下WAT量以及肝臟重量的增加(圖6A)。與對照LFi后代相比,經propionic acid處理的母親(Pro后代)的血漿代謝參數也得到了改善(圖6B)。此外,在Pro后代中挽救了LFi后代的交感神經功能障礙(圖6C)。此外,產婦用PMP干預可逆轉由LFi喂養(yǎng)的母親的胚胎中向心神經投射的延遲以及GLP-1 +腸內分泌細胞和胰腺b細胞分化的延遲(圖6,D和E);它也增強了胚胎中的血漿胰島素水平,使其恢復到與HFi胚胎相當的水平(圖6F)。因此,在給予propionic acid的母親的胚胎中,對照胚胎中的血漿葡萄糖水平的增加被有效地抑制了(圖6F)。結果表明,母體PMP的重要性,這使得后代對肥胖具有抵抗力。
結論:
在妊娠期間,母體腸道菌群通過SCFAGPR41和SCFA-GPR43軸賦予了后代肥胖抵抗力。 懷孕期間,交感神經、腸道和胰腺中的GPR41和GPR43感測到來自母體腸道菌群的SCFA,影響了產前代謝和神經系統(tǒng)的發(fā)育。 這些發(fā)現表明,懷孕期間的母體腸道環(huán)境是防止后代代謝綜合征的新陳代謝程序的關鍵因素。 因此,懷孕小鼠的腸道菌群提供了一種環(huán)境提示,可微調子代的能量穩(wěn)態(tài),從而防止代謝綜合征的發(fā)展。






