神經(jīng)肽VIP通過(guò)調(diào)節(jié)ILC3活性激活腸道粘膜免疫
神經(jīng)肽血管活性腸肽(VIP)通過(guò)調(diào)節(jié)3型先天性淋巴樣細(xì)胞(ILC3)活性賦予腸道粘膜免疫力,這一成果由澳大利亞維多利亞墨爾本大學(xué)Gabrielle T. Belz、Cyril Seillet等研究人員合作完成。2019年12月23日, 《Nature Immunology》在線發(fā)表了這一最新研究成果“The neuropeptide VIP confers anticipatory mucosal immunity by regulating ILC3 activity”。IF=27.586 。該研究發(fā)現(xiàn)了ILC3s的功能在一天中不是恒定的,而是在活躍期和靜止期之間振蕩。腸內(nèi)ILC3s的協(xié)同反應(yīng)依賴(lài)于食物誘導(dǎo)的神經(jīng)肽血管活性腸肽 (VIP)的表達(dá)。腸ILC3s具有高表達(dá)的G蛋白偶聯(lián)受體血管活性腸肽受體2 (VIPR2),VIP激活顯著增加了IL-22的產(chǎn)生和上皮的屏障功能。相反,通過(guò)VIPR2的信號(hào)缺失導(dǎo)致ILC3s生成IL-22的能力受損,并增加炎癥誘導(dǎo)的腸道損傷的易感性。因此,內(nèi)在細(xì)胞節(jié)律與食物攝入的循環(huán)模式協(xié)同作用,驅(qū)動(dòng)IL-22的產(chǎn)生,并通過(guò)ILC3s中的VIP–VIPR2途徑同步保護(hù)腸上皮。

結(jié)果一、ILC的細(xì)胞因子產(chǎn)生全天振蕩
上皮細(xì)胞表現(xiàn)出轉(zhuǎn)錄調(diào)控的晝夜波動(dòng),可以暫時(shí)調(diào)控上皮的完整性29。為了研究ILC在胃腸道中的轉(zhuǎn)錄組和功能是否受到周期性調(diào)節(jié),將C57BL/6小鼠飼養(yǎng)在嚴(yán)格的24小時(shí)暗光周期下(開(kāi)燈12 h,開(kāi)燈時(shí)間記為t 0),隨意喂食。在體外用細(xì)胞刺激細(xì)胞后,在第4天(光照開(kāi)始后4小時(shí))和第16天(光照后4小時(shí))分離出從小腸,肺和腸系膜淋巴結(jié)分離的ILC和其他淋巴細(xì)胞產(chǎn)生細(xì)胞因子的能力。佛波醇12-肉豆蔻酸酯13-醋酸酯(PMA)和離子霉素持續(xù)4.5小時(shí)。這些數(shù)據(jù)表明,在淋巴細(xì)胞中,ILC2和ILC3對(duì)時(shí)間調(diào)節(jié)特別敏感。
為了更好地了解IL-5和IL-22產(chǎn)生變異的性質(zhì),分析了這些細(xì)胞因子的離體表達(dá),在t4,t10,t16和t23時(shí)在小腸和肺的ILC2s和ILC3s中沒(méi)有進(jìn)一步刺激。結(jié)果表明,ILCs在基因調(diào)控中表現(xiàn)出明顯的周期性,特別是在腸粘膜免疫保護(hù)的關(guān)鍵基因中。
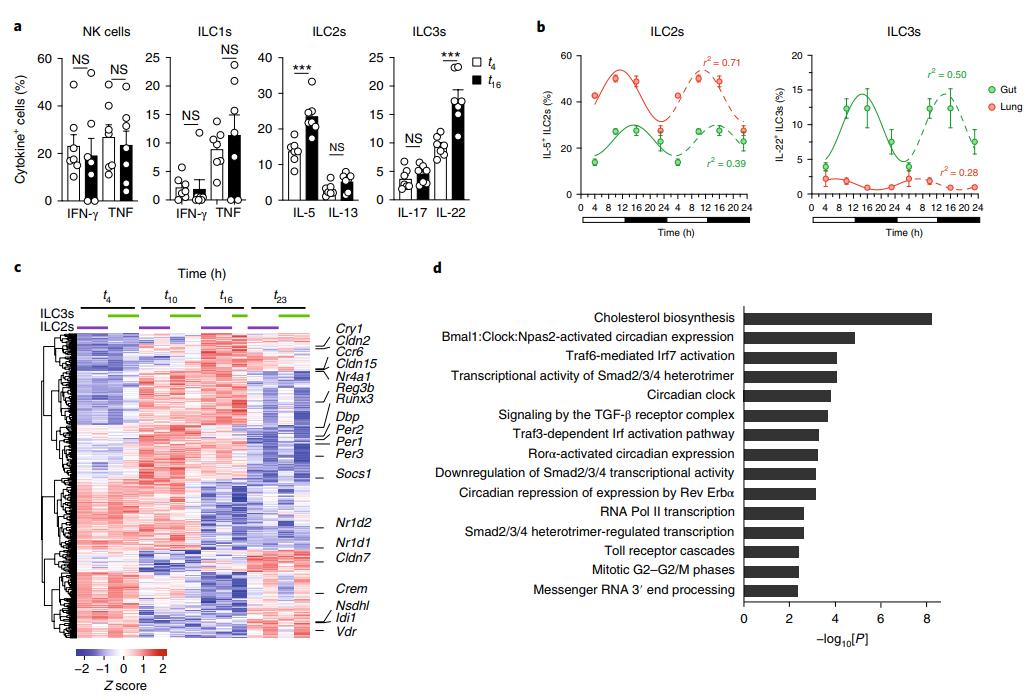
圖1:野生型小鼠的ILC2和ILC3活性在穩(wěn)態(tài)的活動(dòng)和靜止階段振蕩
結(jié)果二、內(nèi)在的時(shí)鐘基因部分調(diào)節(jié)ILC中的細(xì)胞因子
為了了解如何調(diào)節(jié)ILC功能的節(jié)律性,檢查了生物鐘基因Arntl的貢獻(xiàn),該基因在調(diào)節(jié)蛋白質(zhì)(特別是細(xì)胞因子)的振蕩產(chǎn)生中起著關(guān)鍵作用。 芳烴受體核轉(zhuǎn)運(yùn)子像蛋白1(ARNTL)有節(jié)奏地與DNA結(jié)合以激活核心時(shí)鐘基因2的表達(dá)。 將來(lái)自野生型和Il7rCre×Arnt1 fl / fl小鼠的骨髓細(xì)胞的均等混合物(以下稱(chēng)為ArntlΔIL7R)混合在一起,這些混合物在所有淋巴樣譜系中均有條件缺失Arnt1(數(shù)據(jù)未顯示),注入經(jīng)致死劑量照射的野生動(dòng)物中 類(lèi)型的收件人。結(jié)果表明,ARNTL對(duì)于IL-22的基礎(chǔ)表達(dá)很重要,但是它僅部分控制ILC3中IL-22的節(jié)律性產(chǎn)生。
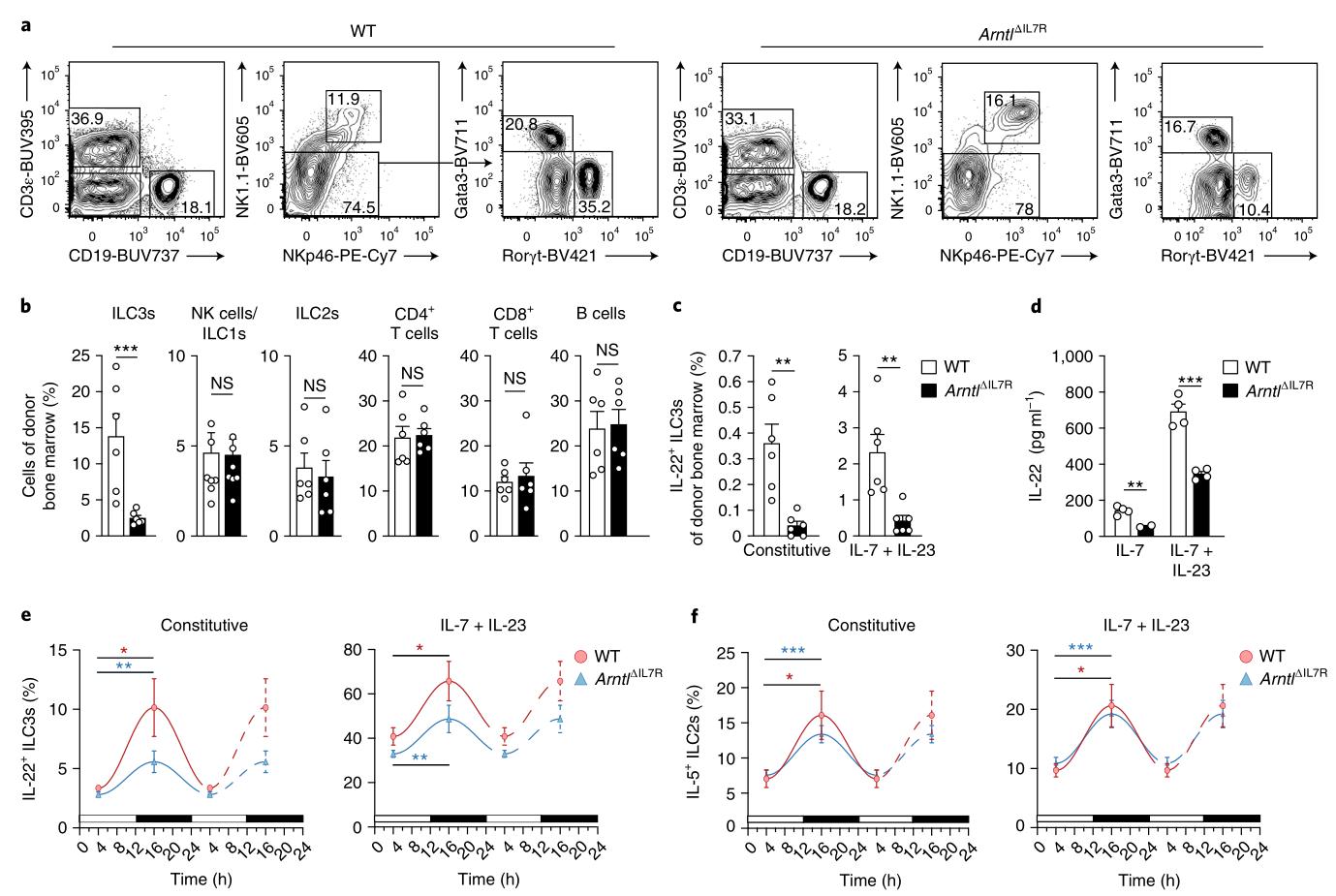
圖2:分子鐘僅部分調(diào)節(jié)細(xì)胞因子分泌的晝夜節(jié)律表達(dá)
結(jié)果三、熱量攝入與ILC節(jié)律性同步
接下來(lái),調(diào)查了腸外ILC3s中IL-22的節(jié)律性產(chǎn)生是否受外在因素調(diào)控。 首先,追蹤了整個(gè)24小時(shí)明暗循環(huán)中的小鼠食物消耗。為了測(cè)試微生物群是否可能導(dǎo)致食物限制后ILC產(chǎn)生細(xì)胞因子的頻率增加,對(duì)僅在黑暗階段(t12 –t24)或光照階段(t0 –t 12)喂養(yǎng)的野生型小鼠進(jìn)行連續(xù)治療, 在飲用水中使用抗生素2周。 對(duì)照小鼠不接受抗生素治療,隨意進(jìn)食。 這些觀察結(jié)果表明,與食物消耗有關(guān)的外在信號(hào)是小腸ILC3s局部調(diào)節(jié)IL-22產(chǎn)生的原因,而引流淋巴結(jié)或肺部的ILC3則不受影響。
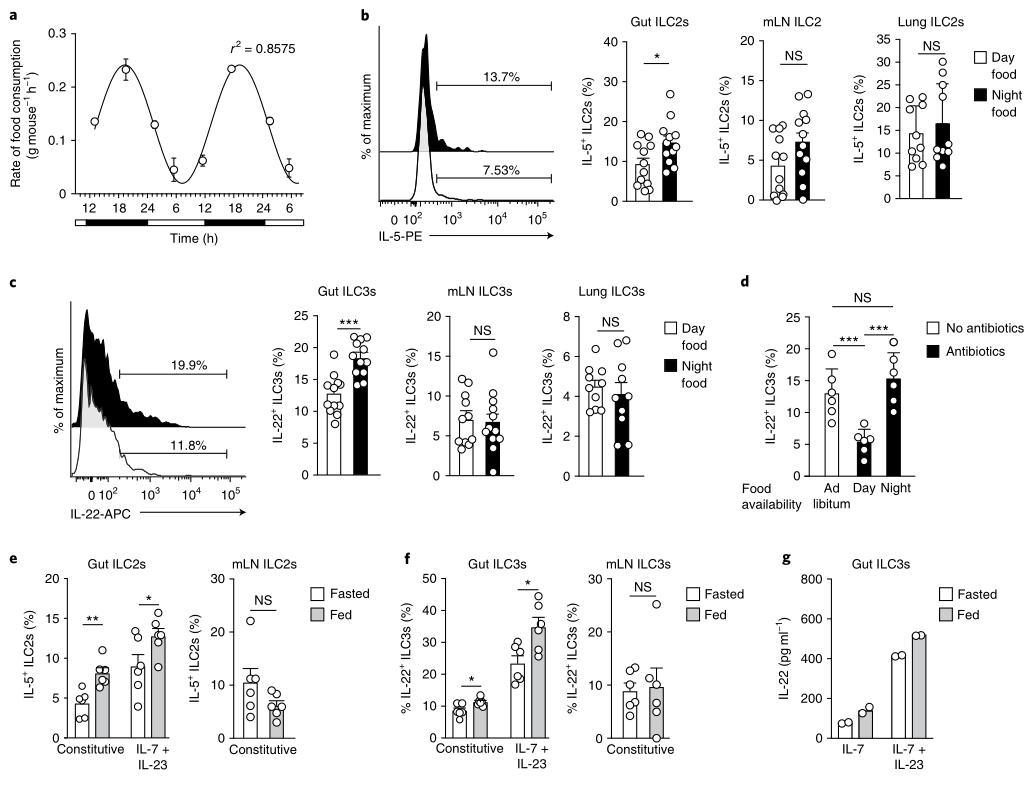
圖3:食物攝入調(diào)節(jié)腸ILC2s和ILC3s的細(xì)胞因子分泌
結(jié)果四、腸ILC3表達(dá)神經(jīng)肽受體VIPR2
為了闡明控制腸道ILC中觀察到的組織特異性調(diào)控程序的機(jī)制,對(duì)來(lái)自小腸和野生型小鼠結(jié)腸的t-4時(shí)分選的Lin-CD127+ CD90+ ILC進(jìn)行了單細(xì)胞RNA–Seq 在12小時(shí)的光照/ 12小時(shí)的黑暗周期中,隨意進(jìn)食。 使用t分布隨機(jī)鄰居嵌入(t-SNE)進(jìn)行的數(shù)據(jù)分析34區(qū)分了8種。 因此,腸中的ILC3表達(dá)VIPR2,并位于VIP +神經(jīng)元附近,在進(jìn)食后頻率增加而在禁食后減少。
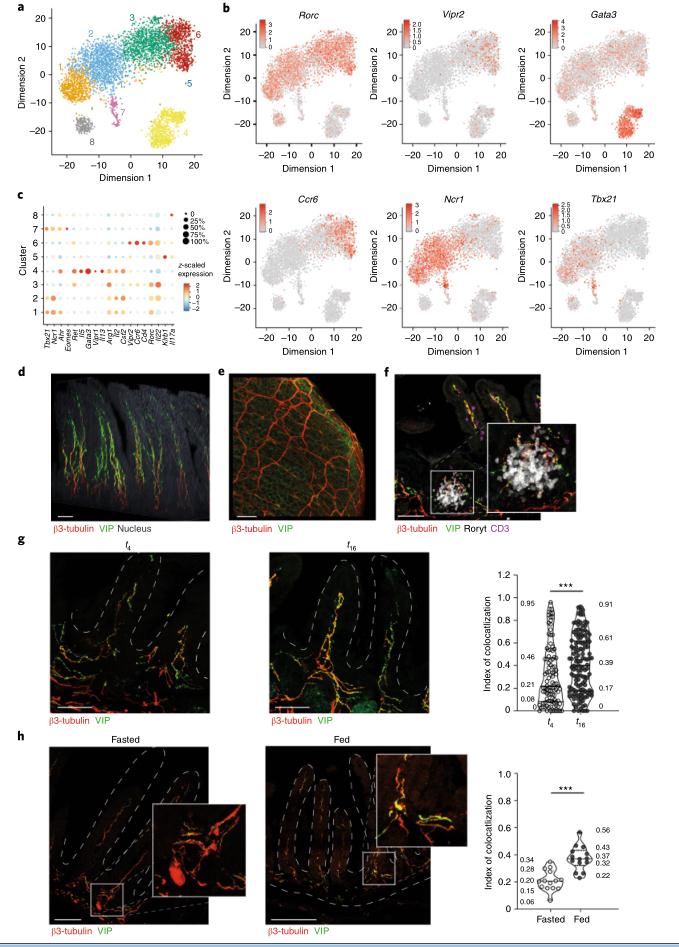
圖4: 腸ILC3子集表達(dá)VIPR2,并位于表達(dá)VIP的神經(jīng)元附近
結(jié)果五、飼養(yǎng)協(xié)調(diào)ILC3s中IL-22的產(chǎn)生
為了評(píng)估暴露于VIP是否在ILC3s中調(diào)節(jié)細(xì)胞因子的產(chǎn)生,刺激了從野生型小鼠固有層分離的CD45 +淋巴細(xì)胞,在存在或不存在VIP的情況下用IL-7和IL-23禁食16 h,持續(xù)4.5 h。模擬用cAMP直接刺激并激活蛋白激酶39的二丁酰環(huán)AMP(d-cAMP)被用作繞過(guò)VIPR2參與的陽(yáng)性對(duì)照。這些發(fā)現(xiàn)表明,體外VIP信號(hào)傳導(dǎo)可以通過(guò)在ILC3上直接激活VIPR2來(lái)增強(qiáng)IL-22的產(chǎn)生。接下來(lái),腹膜內(nèi)注射VIP或磷酸鹽緩沖鹽水(PBS)到野生型小鼠中,并在注射后2 h從小腸分析了Lin-Gata3+Rorγt-ILC2s和Lin-Gata3-Rorγt+ NKp46 +/- ILC3s。 Vipr2-/-小鼠的腸道ILC子集數(shù)量相似,包括CD4 +和CD4-ILC3,與野生型小鼠相比(擴(kuò)展數(shù)據(jù)圖7b)表明,VIPR2不是腸道中ILC3的發(fā)育或維持所必需的。因此,VIP–VIPR2軸推動(dòng)了腸道ILC3s體內(nèi)IL-22的分泌。
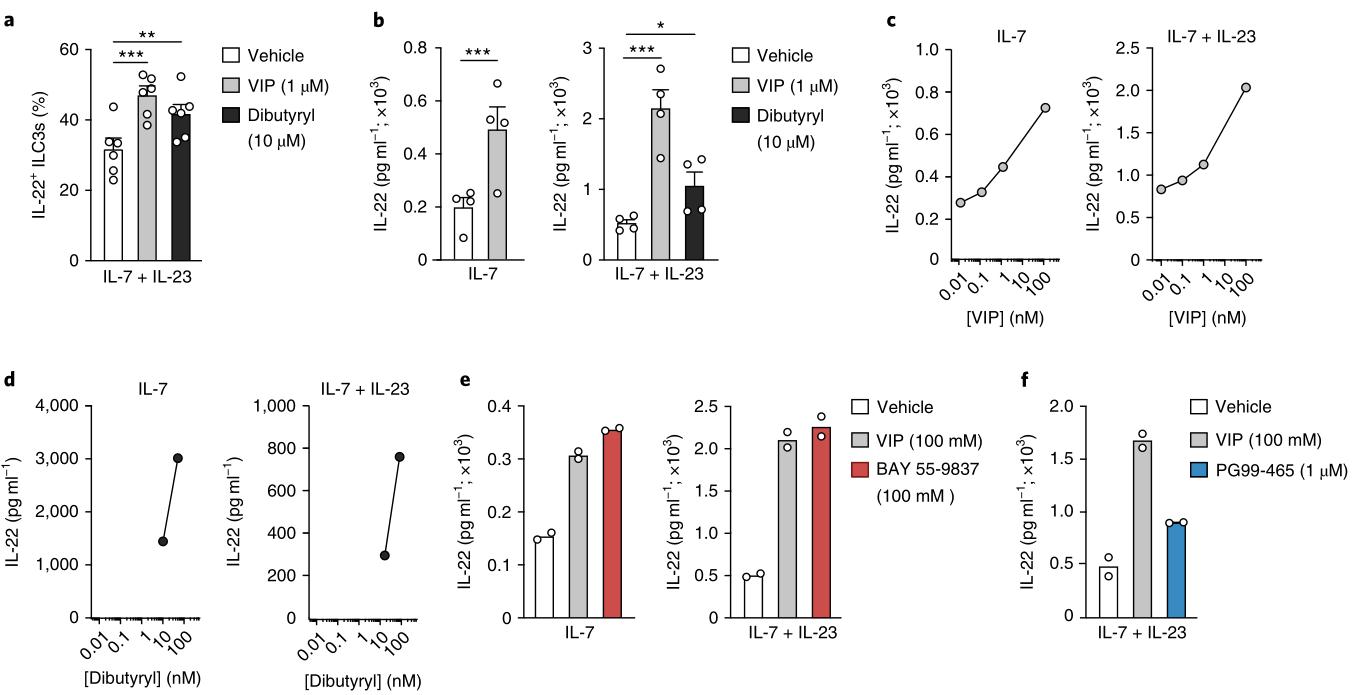
圖5: VIP直接調(diào)節(jié)白細(xì)胞介素3產(chǎn)生的IL-22
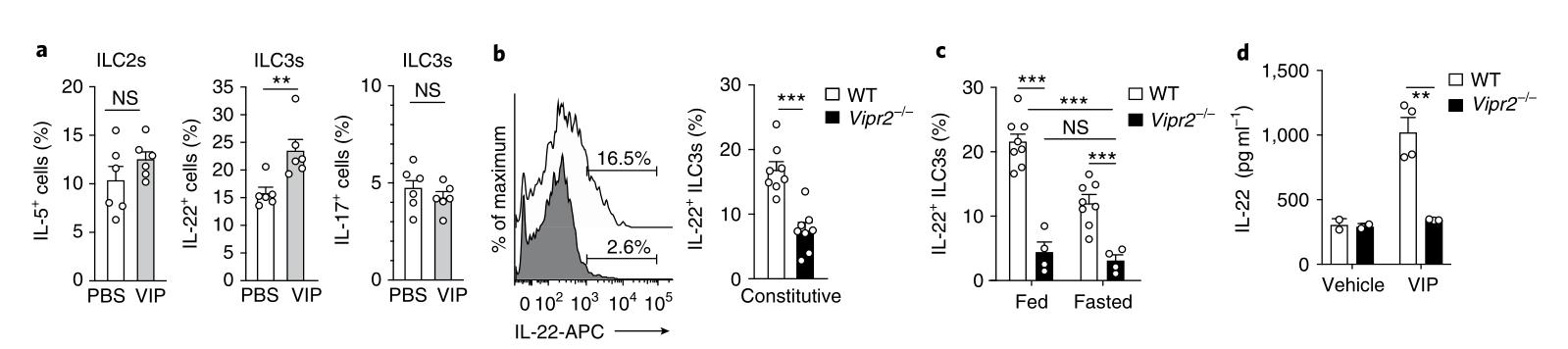
圖6: VIPR2信號(hào)調(diào)節(jié)體內(nèi)ILC3分泌的IL-22
結(jié)果六、ILC3s中的VIPR2維持上皮屏障
為了測(cè)試VIP是否在維持腸道上皮屏障中起作用,用低劑量的DSS(1.5%wt / vol)處理野生型和Vipr2-/-小鼠5 d。結(jié)果表明,盡管其他腸道淋巴細(xì)胞可能會(huì)導(dǎo)致Vipr2-/-小鼠腸道破壞的嚴(yán)重程度,但VIPR2+ ILC3在DSS誘導(dǎo)的炎癥過(guò)程中對(duì)腸道上皮的保護(hù)具有重要作用。
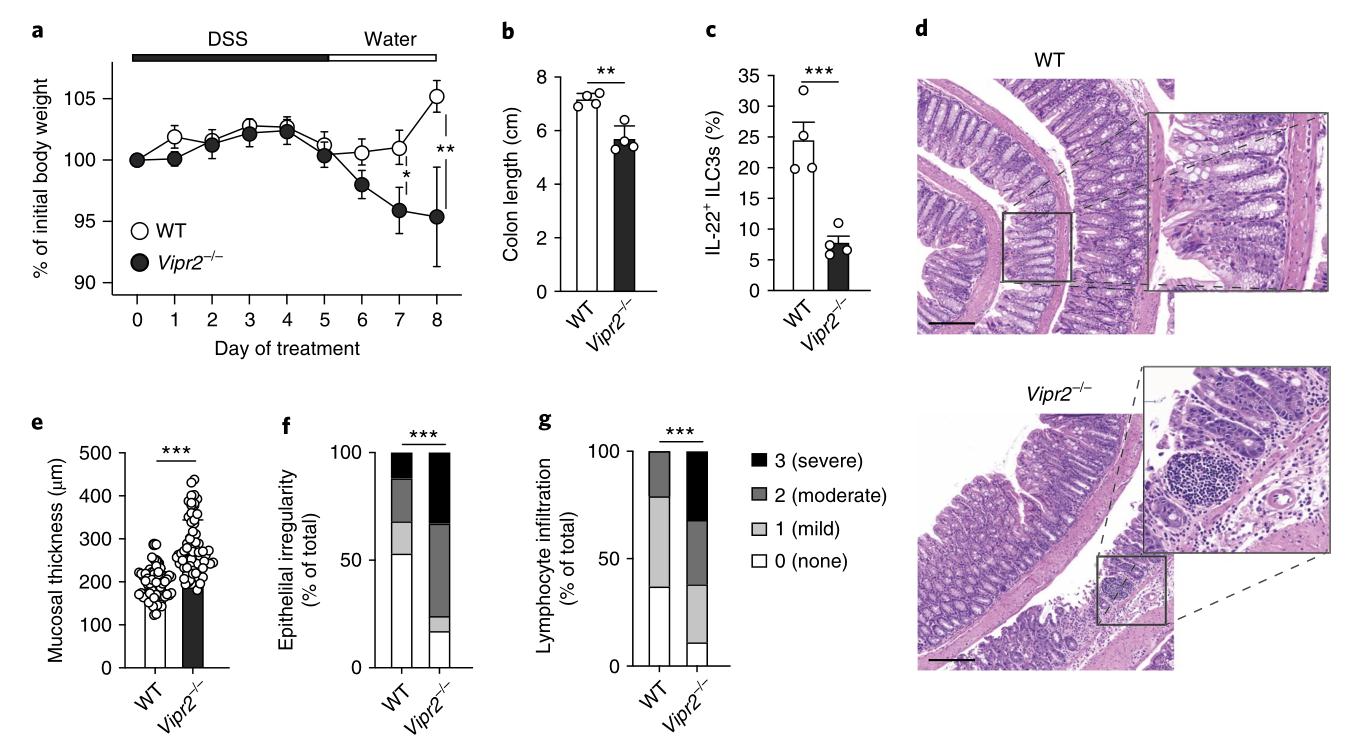
圖7: VIPR2信號(hào)對(duì)于調(diào)節(jié)體內(nèi)腸道完整性至關(guān)重要
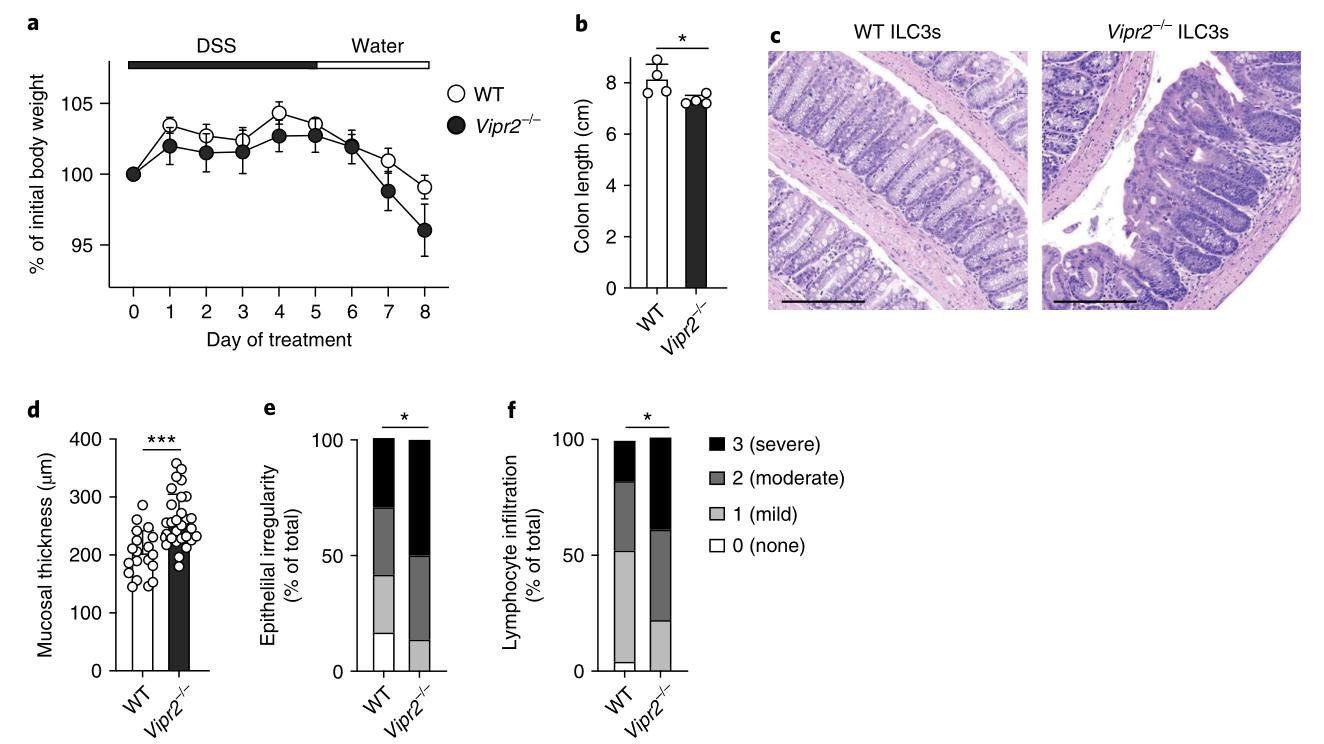
圖8:VIPR2?/ ?ILC3s提供保護(hù)免受DSS誘導(dǎo)的炎癥
結(jié)論:
該研究確定了調(diào)節(jié)腸中IL-22表達(dá)的信號(hào)之一,并且可能在與IL-22相關(guān)的免疫病理學(xué)中也很重要。這些觀察結(jié)果揭示了一些機(jī)制,這些機(jī)制將腸道中的保護(hù)性反應(yīng)與腸道中的刺激性負(fù)荷相匹配,并可能協(xié)調(diào)體內(nèi)穩(wěn)態(tài)組織修復(fù)途徑的誘導(dǎo)。






