Molecular Cell報道m6A修飾調節環狀RNA天然免疫
近期,國際頂級分子生物學雜志Molecular Cell上報道了斯坦福大學研究人員最新研究結果:N6-Methyladenosine Modification Controls Circular RNA Immunity。小編在這分享給大家。環狀RNA是目前的研究熱點之一,但其在免疫調節中的作用及其作為細胞內的一種RNA是否與模式識別受體作用的研究仍然十分缺乏。在五月發表于Cell雜志中的一篇文章報道了內源的環狀RNA能抑制protein kinase R和調節病毒感染后的天然免疫應答反應,小編也曾分享給大家。
本文的研究出發點為研究外源的環狀RNA(circFOREIGN)的免疫原性。通過表達純化外源環狀RNA并已佐劑方式處理小鼠后,circFOREIGN能提升T細胞的細胞因子和血清抗體水平;同時circFOREIGN也能促進腫瘤免疫作用。進一步的研究發現,circFOREIGN的m6A修飾在體內和體外都能減弱免疫反應,而且這種作用是通過m6A讀碼蛋白YTHDF2的結合產生的。工作結果如圖1模式圖所示。這項研究揭示了宿主細胞通過化學修飾來區分自身和外源環狀RNA,這與DNA修飾調節的限制性內切酶系統類似,極大的豐富了我們的認知。小編猜測這也是探索m6A修飾功能的一個新方向。

圖1 m6A修飾調節環狀RNA天然免疫模式圖
下面展示文中部分數據。如圖2-4所示。
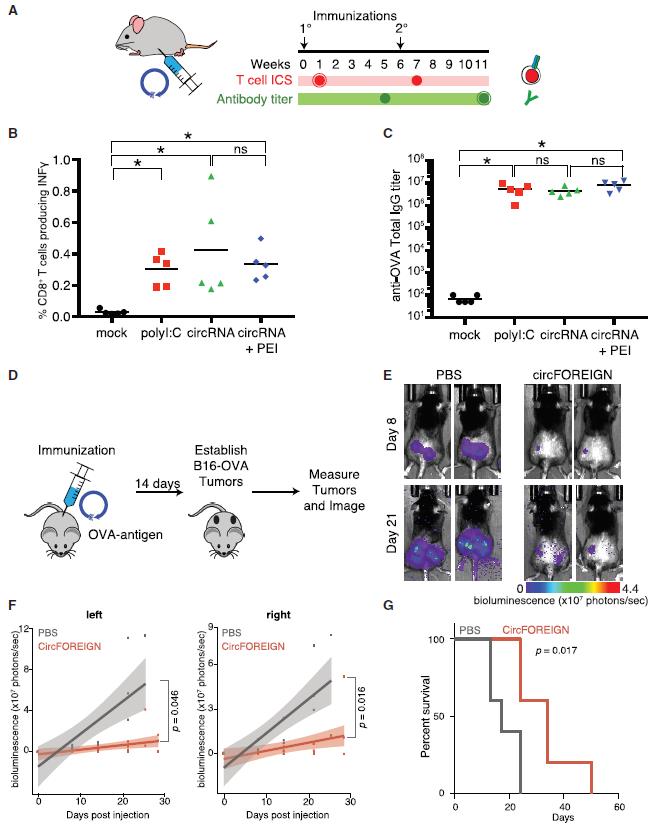
圖2 circFOREIGN在體內能誘導免疫反應
在不同組別RNA與雞卵清蛋白混合皮下注射小鼠后,再檢測T細胞中細胞因子水平和血清抗體滴度。結果顯示環狀RNA具有免疫佐劑的作用。圖中線性RNA病毒模擬物poly I:C為陽性對照,PEI為包裝轉染試劑。在OVA-B16黑色素瘤模型中,circFOREIGN的處理能顯著抑制腫瘤的生長。
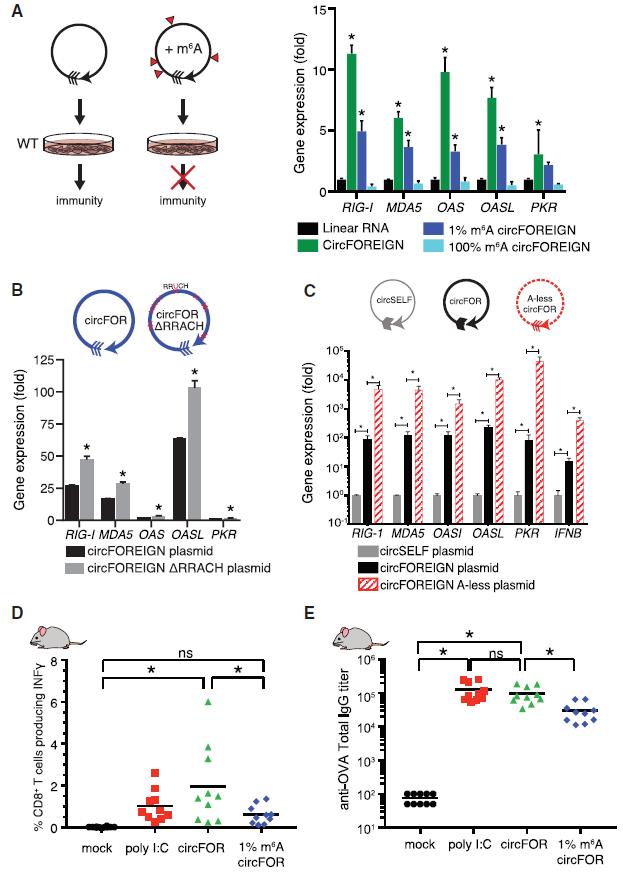
圖3 m6A修飾減弱circFOREIGN體內和體外的免疫應答
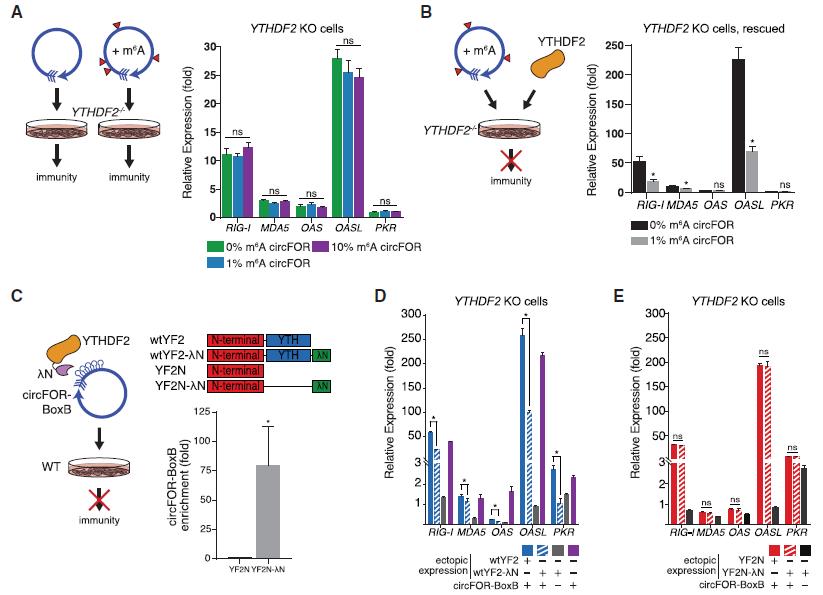
圖4 m6A修飾的circFOREIGN通過YTHDF2的結合逃逸天然免疫識別






