Nature immunology揭示LncRNA調節抗病毒天然免疫上游通路的新機制
抗病毒天然免疫中,宿主識別外源RNA并清除。RIG-I是抗病毒天然免疫中的重要基因,它識別RNA病毒后聚集于線粒體與MAVS作用,傳遞信息至下游信號通路,從而激活包括I型干擾素在內的抗病毒反應通路。作為其中一種RNA病毒感受分子,前人研究中在創新性的發現了宿主自身也存在lncRNA與之結合并調節其活性。相關通路中是否還有結合lncRNA調節方式呢?
在前人報道中, TRIM25結合RNA后抗病毒反應作用增強;而登革熱病毒的RNA能與TRIM25結合并抑制其功能。該文作者便深入研究了lncRNA對TRIM25的調節作用。最終發現Lnczc3h7a通過scaffold作用促進TRIM25與RIG-I的結合,該結合促進了MAVS/IRF3通路的激活。這可能是宿主抵御病毒RNA阻斷RIG-I活性的一種防御方式。
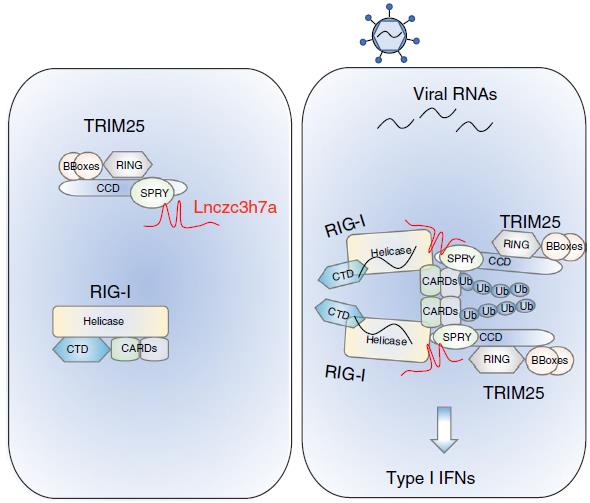
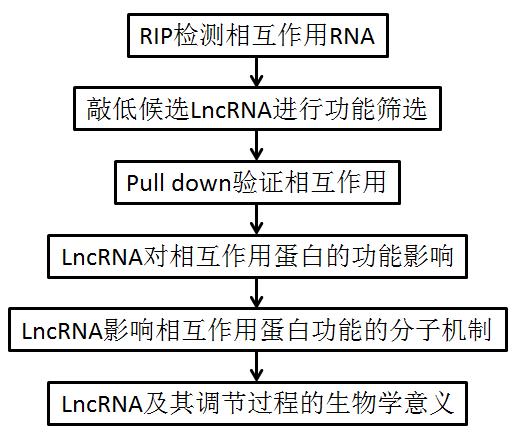
圖1 研究結果模式圖和流程圖
作者首先在Flag-TRIM25過表達的小鼠巨噬細胞系RAW264.7中通過RIP-Seq檢測了VSV感染前后與TRIM25相互作用的lncRNAs。然后確立VSV感染后富集豐度最高的20個lncRNAs為候選指標。通過siRNA在小鼠腹腔巨噬細胞中逐一敲低相應lncRNA后,作者一一檢測了VSV感染后細胞相應的IFNB1轉錄水平變化。敲低編號RIP.6683的lncRNA后,VSV感染后的IFNB1水平顯著下降。因此作者認為該lncRNA參與調解該過程。該lncRNA為新發現lncRNA且被命名為Lnczc3h7a。作者對其特征進行了一系列鑒定:長603個核苷酸,含polyA尾,位于小鼠編碼基因Zc3h7a的內含子區域,無蛋白質翻譯。但在人基因組上未能擴增出該序列。
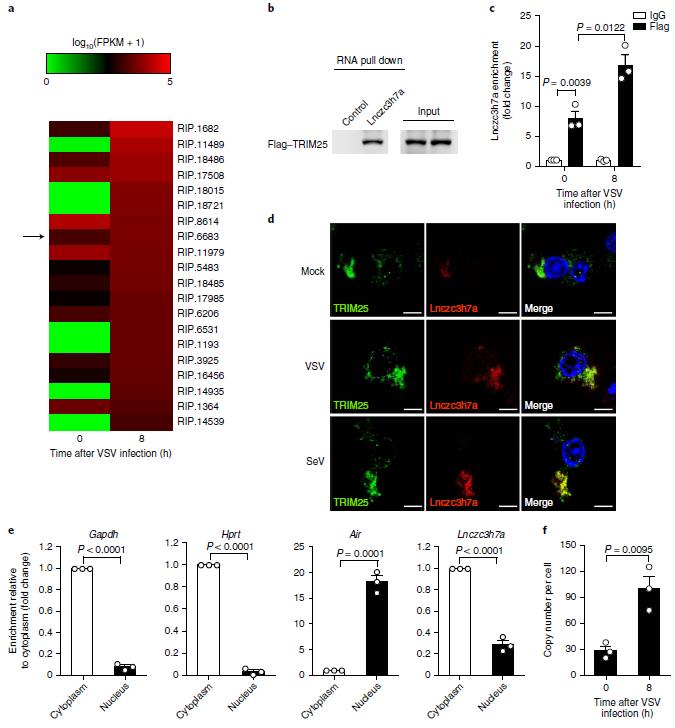
圖2 Lnczc3h7a能與TRIM25結合
作者通過生物素標記的Lnczc3h7a pull down也能檢測到TRIM25的富集。而且VSV感染后,兩者的相互作用更強。FISH實驗表明,SeV和VSV感染后,Lnczc3h7a表達量升高;而且Lnczc3h7a與TRIM25共定位。進一步檢測其他病原體刺激后Lnczc3h7a的表達變化發現,RNA病毒和IFNB1的處理上調其表達的作用最為顯著。在細胞和小鼠模型中敲低和敲除Lnczc3h7a后,作者檢測到RIG-I介導的下游抗病毒基因在VSV感染后激活水平顯著降低。通路下游激活標志p-IRF3水平也顯著下降。這進一步證明了Lnczc3h7a對RIG-I介導的RNA病毒響應具有正向調節作用。
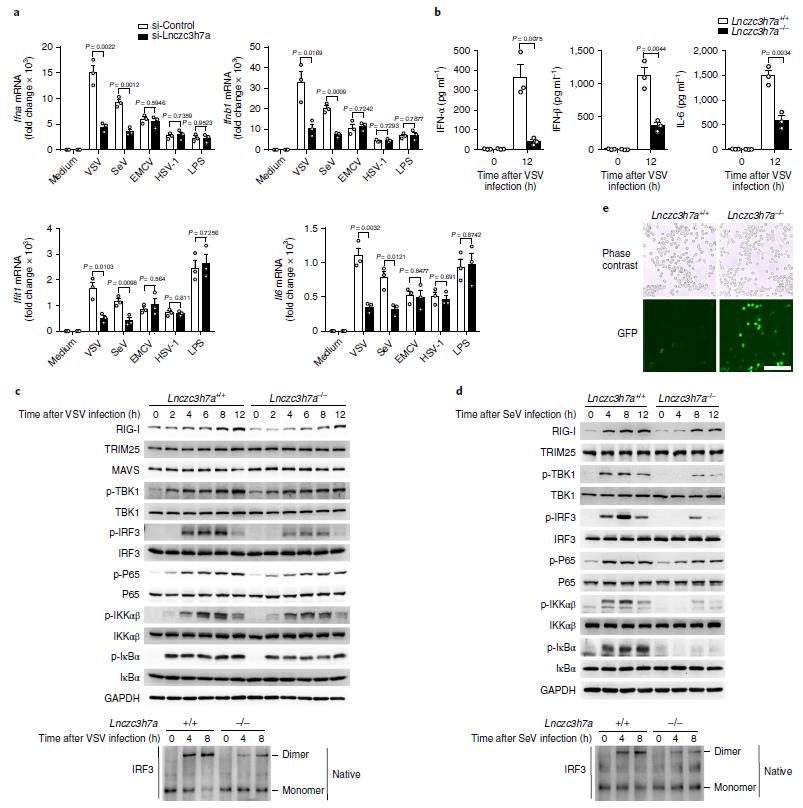
圖3 Lnczc3h7a促進TRIM25下游抗RNA病毒信號通路的激活
Lnczc3h7a過表達并不影響TRIM25的寡聚化和泛素化,也不影響MAVS的泛素化。通過截斷實驗作者發現是TRIM25的SPRY結構域與Lnczc3h7a相互作用。過表達Lnczc3h7a能促進RIG-I的K63泛素化以及RIG-I和TRIM25的共定位。這些結果表明Lnczc3h7a結合TRIM25,促TRIM25與RIG-I的結合以及RIG-I的K63泛素化。
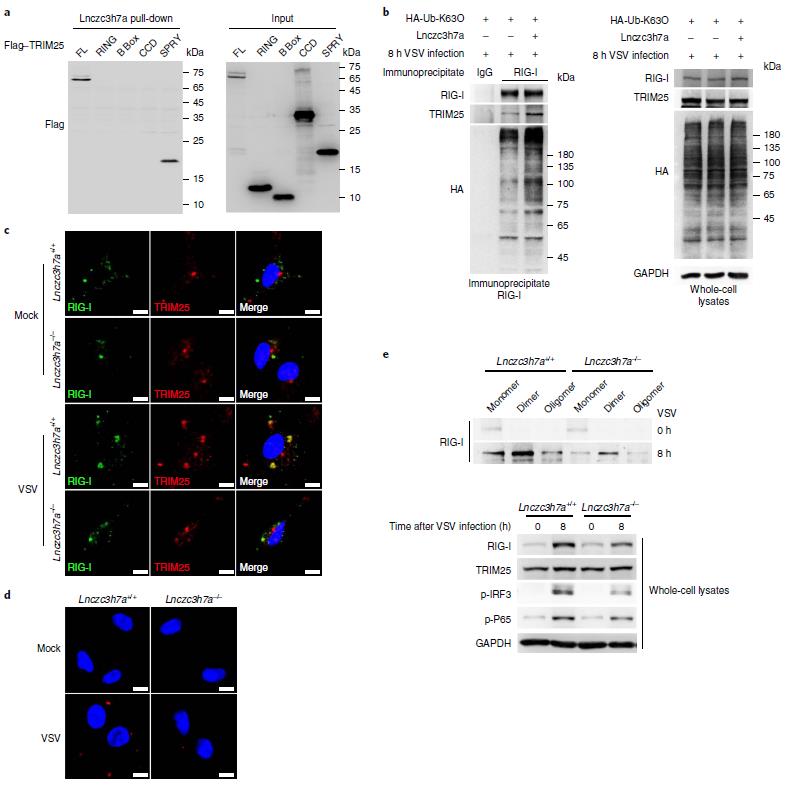
圖4 Lnczc3h7a促進TRIM25介導的RIG-I K63泛素化
接下來,作者開始研究Lnczc3h7a如何調節TRIM25與RIG-I的相互作用。在VSV感染后,作者檢測到Lnczc3h7a和RIG-I的相互作用;而未感染時則沒有。在敲除TRIM25后,VSV感染后的Lnczc3h7a與RIG-I相互作用消失。GST-pull down實驗表明Lnczc3h7a與RIG-I的helicase結構域相互作用。而該結構域只在激活后暴露。Pull down實驗也表明Lnczc3h7a主要與活化的寡聚體RIG-I結合。因為該結構域能識別病毒RNA,所以作者檢測了Lnczc3h7a是否會與病毒RNA競爭性結合該結構域。作者未檢測到它們之間的競爭性結合,這說明它們可能各種有不同的結合位點。進一步的實驗證明了Lnczc3h7a與RIG-I的結合不能使其激活。

圖5 Lnczc3h7a與活化的RIG-I的解旋酶結構域相結合
通過iCLIP實驗,作者檢測到TRIM25結合位點在Lnczc3h7a的308和311位附近;RIG-I結合位點在Lnczc3h7a的332位附近。在Lnczc3h7a敲除細胞中,回復表達該區域刪除突變的Lnczc3h7a均不能回復其功能,而野生型Lnczc3h7a能回復其促進TRIM25和RIG-I結合的功能。如圖6c所示,紅色信號代表TRIM25和RIG-I之間的相互作用。
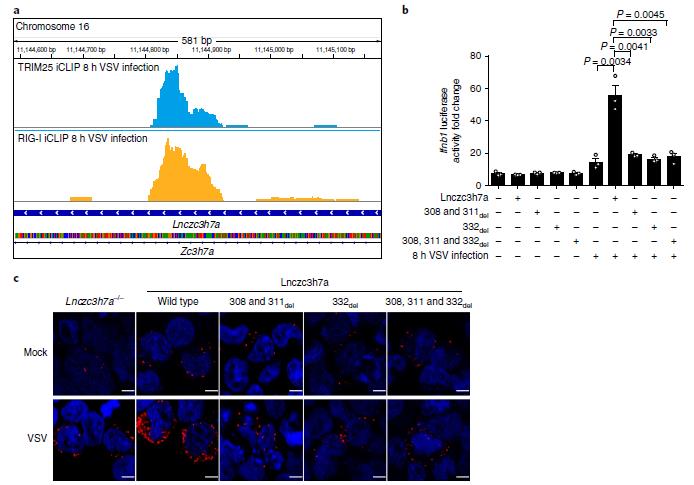
圖6 Lnczc3h7a通過其308、311和332附近序列促進TRIM25和RIG-I之間的相互作用
該文為我們研究lncRNA在信號通路上游的調控作用提供了很好的參考。Lnczc3h7a在人基因組同樣位置未檢測到lncRNA轉錄,那人體內是否有同樣的調控機制和是哪一個lncRNA分子參與調解是值得研究的內容。同時,病毒感染后Lnczc3h7a的表達上升的調控機制也是值得關注的問題。






