BMP4通過Ube2s和Chmp4b介導的染色體穩定性保護mESCs的發育潛力
化學定義培養基被廣泛用于培養小鼠胚胎干細胞(mESCs),其中N2B27作為血清的替代品,GSK3β和MEK抑制劑(2i)有助于促進基態多能性。最近的研究表明,MEKi可能導致不可逆的缺陷,損害了mESCs的發育潛力。我們證明了在化學條件下骨形態發生蛋白(BMP)信號的缺乏是多能性受損的主要原因之一。機制上,BMP4激活BMP信號通路可通過調控下游靶點Ube2s和Chmp4b來維護mESCs的染色體完整性和增殖能力。BMP4具有明顯的體內發育潛力和長期的多能性保存。BMP4驅動的多能性改善優于減弱MEK抑制。綜上所述,我們的研究表明BMP信號的適當激活在調節功能多能性方面是必不可少的,揭示了BMP4應應用于無血清培養系統。本文于2022年8月發表于Protein & Cell (IF=15.328)上
技術路線:

主要研究結果:
(1) 與S/2i-mESC相比,N/2i-mESCs具有有限的多能性
我們首先從攜帶Oct4-ΔPE-EGFP (OG2)報告子的囊胚中衍生出傳統血清條件下的mESC系。本研究的株系具有正常核型和高效力(圖1A-D)。將三個細胞系分別適應S/2i和N/2i條件15天,并與S條件下相同傳代后的原細胞系進行比較(圖1A)。在三種條件下培養的mESCs都表現出緊密填充和圓頂的菌落,并顯示出顯著的Oct4-EGFP的一致維持(圖1B)。然而,N/2i-mESCs的菌落形態明顯變小,表明增殖能力受損(圖1B)。這些N/2i-mESC表現出嚴重的非整倍性,并隨著培養時間的延長而惡化(圖1C)。相比之下,在S/2i-mESCs中未發現這些異常,提示無血清條件下缺乏的一些因素可能是導致這些缺陷的原因。與相應的S-mESCs相比,所有S/2i-mESCs在皮膚和種系中的嵌合性顯著增強(圖1D-F)。四倍體胚胎互補(TEC)試驗進一步證實,N/2i-mESCs在體內的發育嚴重受損,因為無法產生全ESC小鼠(圖1G)。綜上所述,我們發現S/2i-mESCs具有非常好的發育潛力,而在N/2i條件下,由2i驅動的功能改善被削弱,N/2i-mESCs表現出染色體不穩定、增殖紊亂和發育潛力受限。

圖1:與N/2i-mESCs相比,S/2i-mESCs具有更好的發育潛力。
(2) N/2i條件下失活的TGFβ、BMP、AKT信號通路在S/2i條件下得到改善
為了揭示N/2i-mESCs與S/2i-mESCs相比發育潛力受限的潛在分子機制,我們進行了RNA測序。主成分分析(PCA)表明N/2imESCs的轉錄組與S/2i-mESCs的轉錄組有很大的不同(圖2A)。差異表達基因(DEGs)分析顯示,男性N/2i-mESCs與男性S/2i-mESCs相比,有3233個基因發生顯著變化(圖2B)。干細胞分化、細胞周期、干細胞維持和胚胎發育等過程主要在N/2i-mESCs中被下調,說明N/2i-和S/2i-mESCs在許多方面是不同的(圖2C)。我們對多個關鍵信號通路進行了基因集富集分析(GSEA)(圖2D)。通過基因本體論分析,我們分析了兩性S/2i mESCs中特異上調的1581個基因(圖2E),發現TGFβ和PI3K-Akt信號通路明顯富集(圖2F)。通過motif調用分析發現,這些上調的基因中有許多是Klf和Smad家族成員的靶點(圖2G)。上述三個信號通路的代表性基因的表達確實在N/2i-mESCs中下調,在S/2imESCs中恢復(圖2H)。綜合來看,N/2i-mESCs中tgf-β、BMP和AKT信號通路被滅活。作為對比,這些通路在S/2i-mESCs中被恢復,這可能是觀察到的發育改善的原因(圖1D-G)。
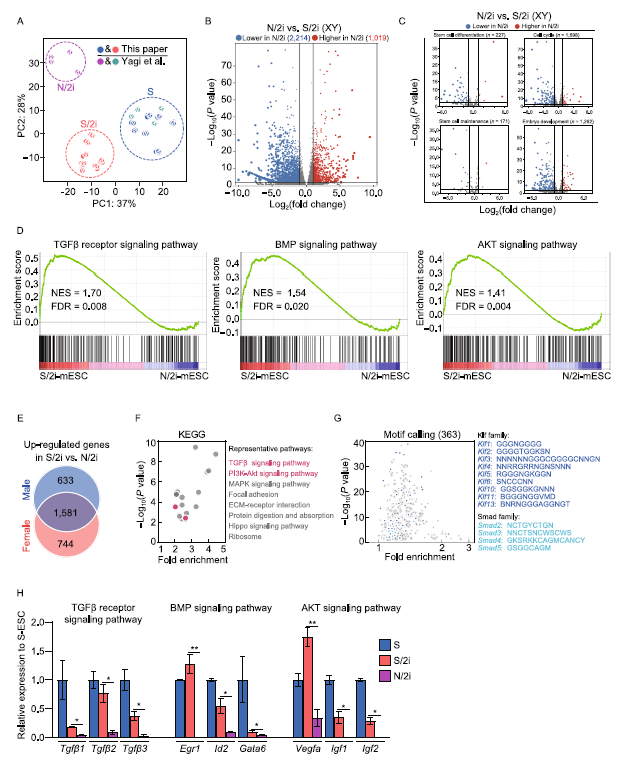
圖2:S/2i條件下TGFβ、BMP、AKT信號通路的失活得到改善。
(3) BMP4保護了染色體的完整性,并保留了mESCs的發育潛力
我們對已被證明可分別激活TGFβ、BMP或AKT信號通路的生長因子進行了小范圍篩選。將mESC在添加特異性生長因子的N/2i條件下培養15天,用于分析和比較(圖3A)。BMP4的效果最好,其次是BMP7和BMP2,說明在N/2i條件下,BMP信號通路對維持染色體完整性至關重要(圖3B)。BMP信號的重新激活可以進一步恢復N/2i-mESCs的增殖能力;受損的細胞周期得到恢復,停留在G1期的細胞減少,細胞周期持續時間縮短(補充圖未展示)。我們隨后研究了BMP信號的激活是否能從功能上提高N/2i-mESCs的發育潛力。在N/2i mESCs中添加BMP4可顯著提高皮膚中的嵌合率180%(圖3C,E)和種系中的嵌合率150%(圖3D,E)。這種改善在所有測試的mESC系中都是一致的(圖3F,G)。隨著BMP4的補充,異常高的N/2i-mESCs的吸收率顯著降低(補充圖未展示)。最后,我們進行了TEC試驗,以測試這些mESC的自主發育潛力。與N/2i-mESC形成對比,N/2i+BMP-mESC可以有效地生成活的all-ESC小鼠(圖3H)。綜上所述,BMP4的激活可以保留mESCs的發育潛力,并維護其染色體完整性。
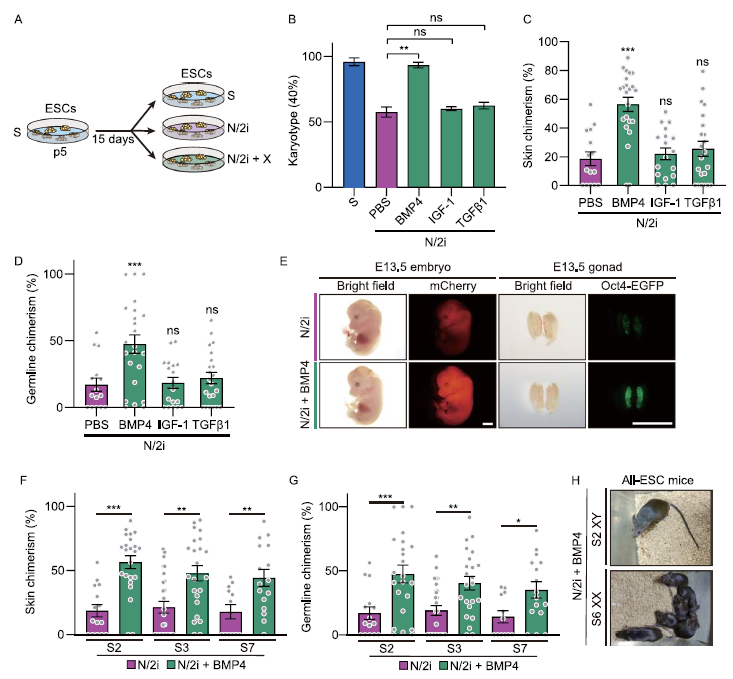
圖3:BMP4保護了染色體的完整性,并保留了mESCs的發育潛力。
(4) Ube2s和Chmp4b對BMP4介導的染色體完整性維護和多能性維護至關重要
N/2imESCs中相對于S/2i-mESCs中失調的染色體分離和細胞周期的相關基因可能是BMP信號通路的潛在下游靶點(圖4A,B)。Timp2等5個基因僅在N/2i-mESCs中異常表達,補充BMP4可以恢復這些基因,其中Ube2s和Chmp4b最為明顯(圖4C)。Ube2s和Chmp4b與調控染色體分離和細胞周期密切相關(圖4A,B)。我們通過shRNA介導的基因敲除在N/2i+BMP4條件下生成Ube2s-和Chmp4b缺陷的mESCs,并通過免疫印跡和RT-qPCR分析驗證這些基因的敲除(圖4D)。shUbe2s- or shChmp4b-mESCs表現出嚴重的非整倍性和DNA損傷。這些缺陷在含有BMP4的條件下不能被修復,表明Ube2s和Chmp4b是BMP4的關鍵靶點(圖4E,F)。ishUbe2s-或ishChmp4b-mESCs產生的畸胎瘤比對照mESCs產生的畸胎瘤小得多(圖4G),說明這些mESCs的增殖受到嚴重損害。與具有明顯三種層分化細胞的對照組畸胎瘤相比,這些微小的畸胎瘤分化較差(圖4G),說明Ube2s或Chmp4b的短期敲除足以引起非整倍體,從而進一步破壞mESCs的分化能力(圖4E)。在嵌合試驗中應用ishUbe2s-mESCs或ishChmp4b-mESCs作為供體細胞后,只能獲得少量嵌合胚胎,并且這些胚胎在皮膚和性腺中分別呈現出較低的mCherry+和Oct4-EGFP+細胞比例(圖4H,I)。我們生成了Ube2s-和Chmp4b過表達的N/2i-mESC并進行了分析(圖4J)。這兩種細胞系在N/2i條件下表現出較高的整倍體細胞比例和恢復的增殖能力(圖4K)。Ube2s過表達的N/2i-mESCs在體內發育潛力增強,吸收速率降低,而Chmp4b過表達的影響相對適中(圖4L,M)。綜上所述,Ube2s和Chmp4b是BMP4的關鍵下游靶點,它們對BMP4介導的染色體完整性保護,正常增殖能力和發育潛能的維持至關重要。

圖4:Ube2s和Chmp4b對BMP4介導的染色體完整性和多能性維護至關重要。
(5) BMP4可恢復N/2i-mESCs的轉錄組失調,并長期保持其多能性
我們發現N/2i+BMP4條件可以在較長培養時間下保持mESCs的發育潛力。N/2i+BMP-mESC在培養55天后產生的嵌合胚的嵌合率甚至高于僅培養15天的N/2i-mESC(圖5A)。這種多能性保存對mESC的種系傳遞能力非常重要,因為長時間培養的N/2i-mESC產生的嵌合胚胎幾乎失去了性腺中的Oct4-EGFP信號(圖5A)。我們通過RNA-Seq分析BMP4對轉錄組的影響。PCA和分層聚類圖表明,N/2i+BMP4-mESCs的轉錄組與N/2i-mESCs的轉錄組差異很大,與血清條件下的轉錄組(S-和S/2imESCs)相似(圖5B)。許多在N/2i-mESCs中異常下調的多能性關鍵基因只有在BMP4補充的條件下才能成功恢復(圖2C)。DEG分析進一步顯示,在N/2i條件下,受BMP4影響的1975個顯著變化基因中,有1633個基因上調(圖5C)。1633個上調基因的KEGG通路上的基因本論顯示,TGFβ和PI3K-Akt信號通路明顯富集,通過motif調用分析,這些基因中有許多是Klf和Smad家族成員的下游靶點(圖5D,E)。這一發現與在S/2i-mESCs和N/2i-mESCs中的結果相似(圖2F,G),進一步證實了BMP4在血清系統中的關鍵作用。GSEA研究表明,N/2i-mESCs中受損的tgf-β、BMP和AKT信號通路在BMP4補充后顯著恢復(圖2D,5F)。綜上所述,BMP4在化學定義的條件下很大程度上恢復了關鍵基因和信號通路的失調,并可以在長期培養中維持mESCs的增強發育潛能。
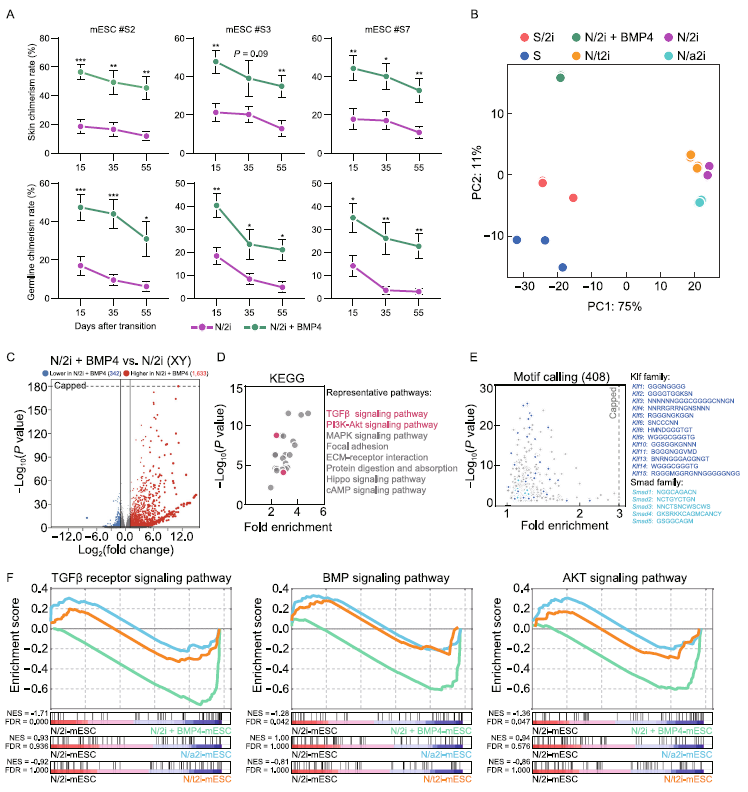
圖5:BMP4可恢復N/2i-mESCs的轉錄組失調,并長期保持其多能性。
(6) 與N/a2i-和N/t2i-mESCs相比,N/2i+BMP4-mESCs表現出明顯的多能性特征
N/2i+BMP4-mESCs比N/2imESCs具有更強的發育潛力。將mESC系#S2分別適應N/2i+BMP4、N/a2i和N/t2i條件15天。在這三種無血清條件下培養的適應的mESCs均表現出一致的Oct4-EGFP維持。與N/a2i-mESCs或N/t2i-mESCs相比,N/2i+BMP4-mESCs在體內發育潛力最高(圖6A,B)。免疫印跡和ELISA表明,BMP4幾乎不影響ERK1/2的磷酸化(圖6C,D)。全基因組亞硫酸氫鹽測序(WGBS)表明BMP4對DNA甲基化恢復沒有影響。S/2i、N/2i和N/2i+BMP4均導致mESCs中明顯的全基因組低甲基化,而減弱MEK的抑制則維持親本差異甲基化區域(DMRs)(圖6E)。印跡控制區域(ICRs)甲基化在15天的培養條件轉換后,所有組均未顯示出很大的變化(圖6F)。為了進一步了解N/2i+BMP4-、N/a2i-和N/tt2i-mESCs之間的轉錄差異,我們進行了RNA-seq分析。與N/2i+BMP4相比,N/a2i或N/t2i引起的基因表達變化相對溫和(圖5C)。N/2i-、N/a2i-和N/tt2i-mESCs表現出非常相似的轉錄組和相對不活躍的全局轉錄水平,這與N/2i+BMP-mESCs不同(圖5B,6G,H)。減弱MEK的抑制并不能恢復mESCs中受損的tgf-β、BMP和AKT信號通路(圖5F,6I,J)。綜上所述,與N/a2i-和N/tt2i-mESCs相比,N/2i+BMP4-mESCs表現出更好的多能性,我們推薦在無血清體系下,N/2i+BMP4條件下mESCs的質量最好。
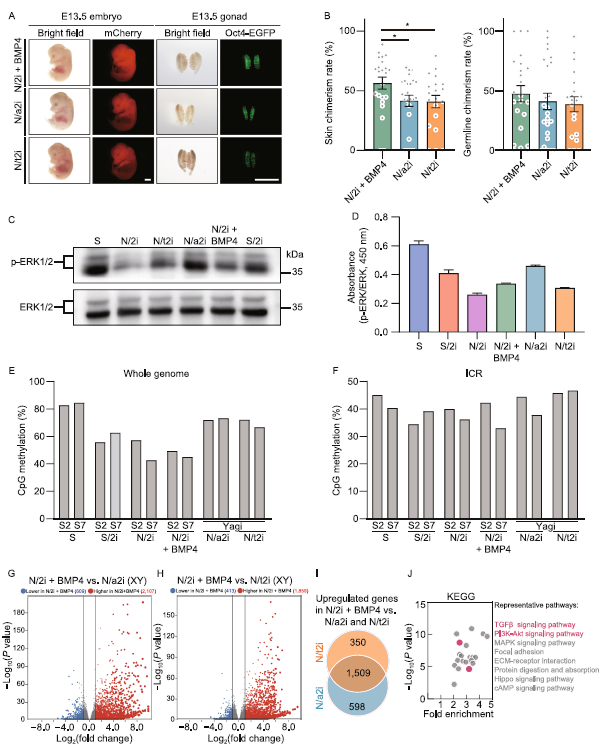
圖6:與N/a2i-和N/t2i-mESCs相比,N/2i+BMP4-mESCs表現出明顯的多能性特征。
結論:綜上所述,BMP4在無血清條件下維持mESCs染色體完整性和多能性方面具有不可替代的作用。不斷改進培養條件的組成部分將有助于增強多能性的維持,并對多能性調控有更多的了解,更重要的是,如何在基礎研究和再生醫學中進一步利用這一特性。
參考文獻:
Wang, M., Zhao, K., Liu, M., Wang, M., Qiao, Z., Yi, S., Jiang, Y., Kou, X., Zhao, Y., Yin, J., Li, T., Wang, H., Jiang, C., Gao, S., & Chen, J. (2022). BMP4 preserves the developmental potential of mESCs through Ube2s- and Chmp4b-mediated chromosomal stability safeguarding. Protein & cell, 13(8), 580–601. https://doi.org/10.1007/s13238-021-00896-x.






