環狀RNA Cwc27通過抑制Pur-α活性促進阿爾茨海默癥發病機制
環狀RNA(circRNAs)在參與各種生物過程和參考多種疾病方面受到越來越多的關注。雖然阿爾茨海默癥(AD)中差異表達的circRNA已經建立,但與AD直接相關的關鍵circRNA在基因表達和疾病相關認知中的精確特征和功能尚不清楚。在此,作者篩選并鑒定了circCwc27這一與AD相關的新型circRNA。該研究于2022年2月發表在《Cell Death Differentiation》,IF:10.717。
技術路線:
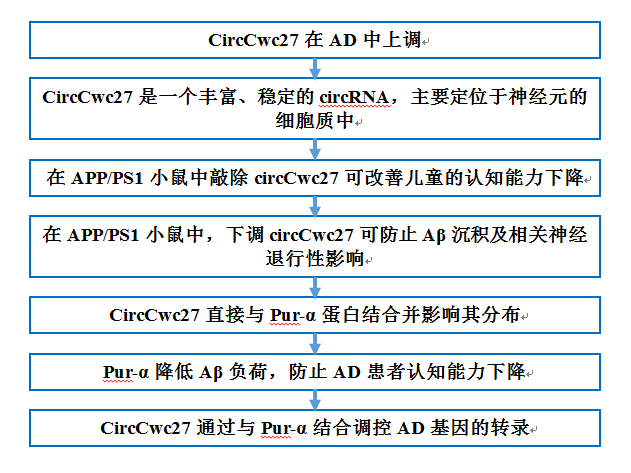
主要研究結果:
1. CircCwc27在AD中上調
作者的目標是篩選AD早期有希望的circRNA,收集6月齡的APP/PS1轉基因和WT對照小鼠海馬體。共有131個circRNA顯著失調,熱圖中顯示了上調和下調最高的15個circRNA(圖1A)。在這30個circRNA中,Rybak-Wolf等人鑒定出13個在人和小鼠之間保守的circRNA。APP/PS1小鼠和WT小鼠的海馬體比較中,有4個circRNA顯著上調,4個circRNA顯著下調(圖1B)。在APP/PS1小鼠的海馬區觀察到AD患者的顳葉皮質和血漿中檢測到circCwc27(mmu_circ_0004423)明顯升高(圖1C),并且在海馬區表達量最高(圖1D)。
2. CircCwc27是一個豐富、穩定的circRNA,主要定位于神經元的細胞質中
在大腦皮層和海馬體中觀察到circCwc27高度表達,這是大腦中兩個脆弱的區域(圖1E)。此外,在APP/PS1小鼠和WT小鼠的大腦中,circCwc27主要表達在神經元而非神經膠質細胞中(圖1F和G)。同時檢測了circCwc27的絕對拷貝數,結果顯示,每個人的海馬神經元中平均有98個circCwc27拷貝,SH-SY5Y細胞中有78個circCwc27拷貝(圖1H)。
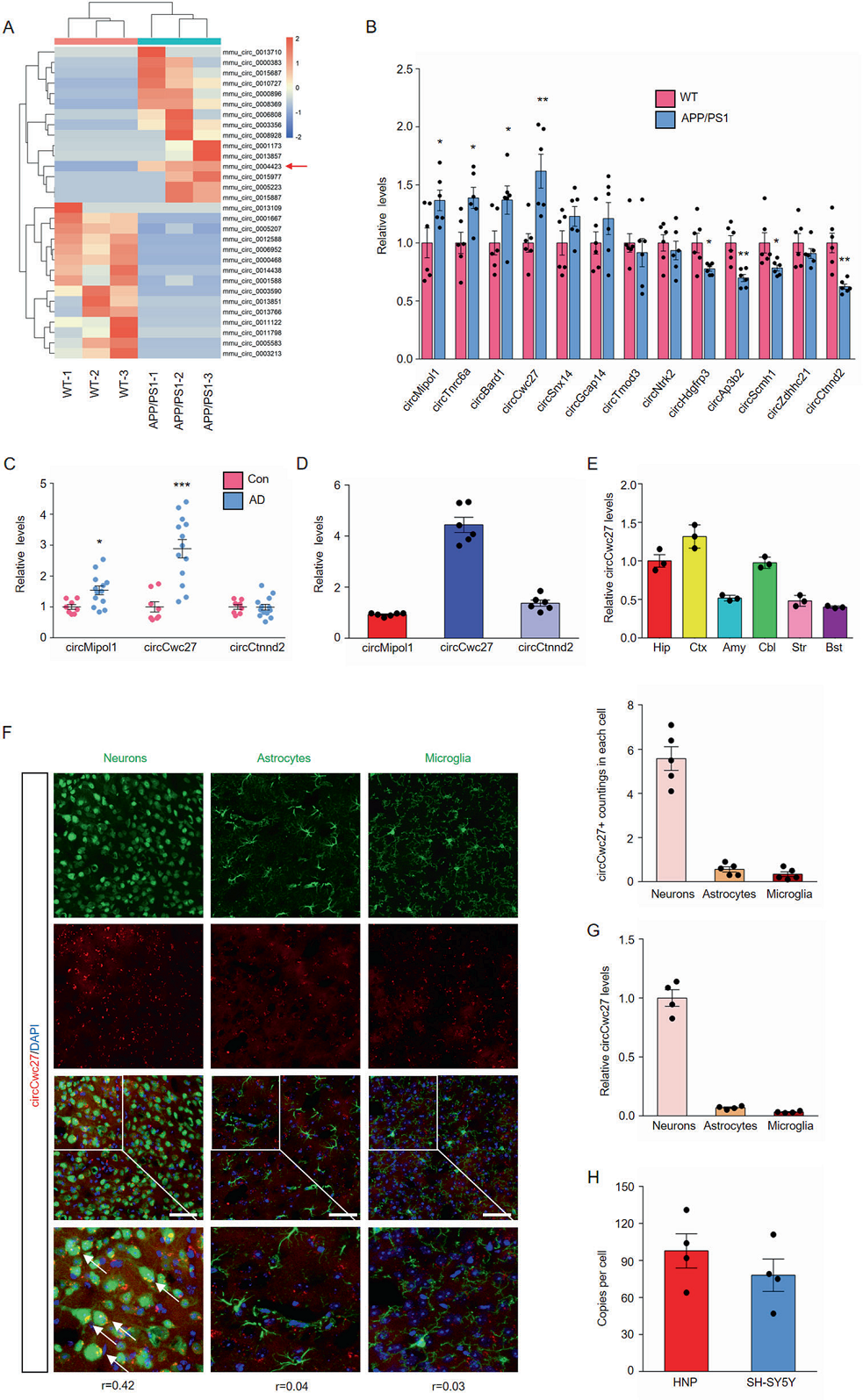
圖1. CircCwc27是一個高度豐富且穩定的circRNA,在AD中表達上調
3. 在APP/PS1小鼠中敲除circCwc27可改善兒童的認知能力下降
將表達shRNA circCon-GFP(LV-sh-circCon)或shRNA circCwc27-GFP(LV-sh-circCwc27)的慢病毒微注射到9月齡小鼠側腦室,2個月后分析小鼠的記憶和空間學習能力(圖2A)。綠色熒光蛋白(GFP)信號主要分布在整個皮層和海馬區,并與神經元共定位(圖2B和C)。CircCwc27表達顯著下調,慢病毒轉導后Cwc27水平保持不變(圖2D)。Y迷宮自發交替行為測試顯示APP/PS1小鼠微注射LV-sh-circCon后,交替性明顯下降,而抑制circCwc27則能顯著阻止這種下降(圖2E)。組間相同的條目數不支持運動功能缺損(圖2F)。
在訓練階段,APP/PS1小鼠中微注射LV-sh-circCon,發現隱藏平臺的潛伏期明顯延長,而微注射LV-sh-circCwc27提高了學習能力(圖2G和H)。在探針試驗中,記憶保持是通過在包含隱藏平臺的象限所花費的時間來衡量的。結果表明,下調circCwc27可以改善APP/PS1小鼠的空間記憶(圖2I和K)。另外,所有組小鼠的游泳速度都相似(圖2J)。綜上所述,這些數據表明,敲除circCwc27在很大程度上改善了AD的認知衰退。

圖2. 在APP/PS1小鼠模型中敲除circCwc27可改善空間學習記憶
4. 在APP/PS1小鼠中,下調circCwc27可防止Aβ沉積及相關神經退行性影響
應用Aβ抗體(NAB228)對APP/PS1小鼠腦組織進行染色,結果顯示微注射LV-sh-circCwc27明顯降低了斑塊負荷(圖3A)。注射LV-sh-circCwc27后,大腦皮層和海馬區可溶性和不可溶性Aβ40和Aβ42水平均持續下降(圖3B-E)。此外,觀察到circCwc27的表達與APP/PS1小鼠組Aβ40(圖3F)或Aβ42水平(圖3G)成正相關。在小鼠海馬中微注射LV-sh-circCwc27,Aβ與營養不良神經細胞共定位的區域顯著減少(圖3H)。WT小鼠微注射LV-sh-circCwc27不影響突觸相關蛋白的表達,而APP/PS1小鼠明顯抑制其下降(圖3I)。APP/PS1小鼠微注射LV-sh-circCwc27可顯著降低小膠質細胞和星形膠質細胞的活化(圖3J)。上述結果表明,circCwc27基因的下調在AD的神經炎癥和神經退行性作用中發揮了保護作用。
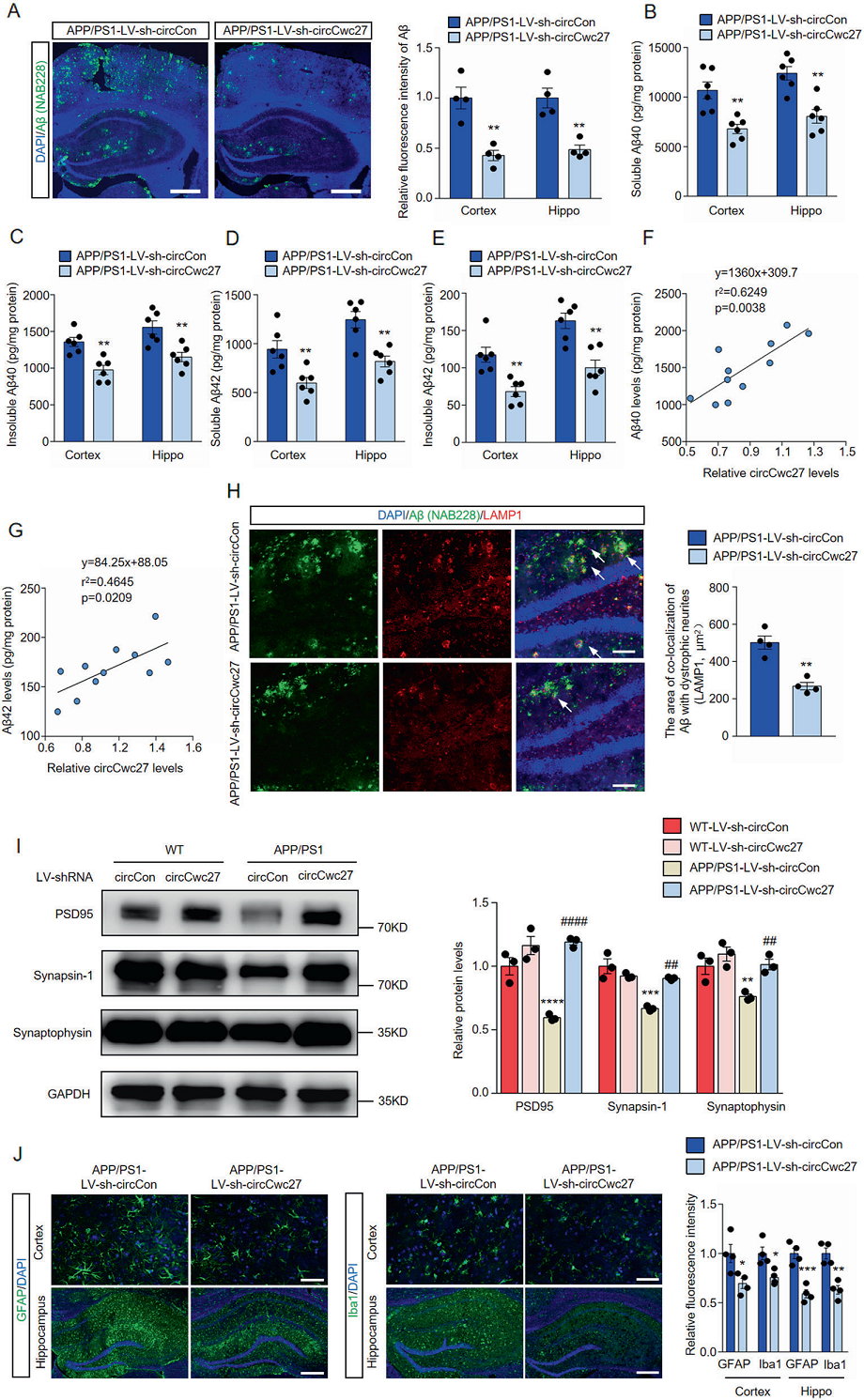
圖3. 敲除circCwc27可改善APP/PS1小鼠的AD病理
5. CircCwc27直接與Pur-α蛋白結合并影響其分布
下一步的目標是闡明circCwc27引起AD病理的分子機制。通過RNA免疫沉淀(RIP),觀察到內源性circCwc27沒有在AGO2上富集(圖4A)。因此,進行RNA下拉分析和質譜(MS)分析,在APP/PS1小鼠海馬中尋找潛在的circCwc27相互作用的蛋白(圖4B)。共有154個蛋白被circCwc27連接探針拉下,這些蛋白大多在大腦中富集。GO富集分析顯示,這些蛋白大多與RNA/DNA結合相關(圖4C)。
RIP檢測結果表明,Pur-α抗體和HNRNPK抗體可拉低circCwc27,而不是SH-SY5Y細胞中的其他三個候選者(圖4D)。RNA下拉結果也驗證了circCwc27與Pur-α的直接相互作用(圖4E)。再進一步驗證了circCwc27與Pur-α的內源性共定位(圖4F)。RIP檢測結果顯示,與circCwc27直接結合的只有PUR重復結構域(66-246aa),沒有其他結構域(圖4G)。
與WT小鼠相比,APP/PS1和APP/PS1-LV-sh-circCon小鼠海馬區circCwc27介導的Pur-α水平顯著上調(圖4H)。敲除circCwc27在APP/PS1小鼠能顯著降低circCwc27與Pur-α的結合(圖4H)。在RIP測定中也得到了類似的結果(圖4I)。免疫印跡結果顯示,APP/PS1小鼠細胞核Pur-α表達明顯降低,胞漿Pur-α表達增加(圖4J和K)。注射LV-sh-circCwc27可顯著促進Pur-α的核分布(圖4J和K)。總之,結果表明,增加circCwc27與Pur-α相互作用并將其捕獲在細胞質中,而敲除circCwc27可促進Pur-α的核轉位。

圖4. CircCwc27與Pur-α蛋白相互作用并影響其分布
6. Pur-α降低Aβ負荷,防止AD患者認知能力下降
將攜帶Flag-labeled Control-GFP(Flag-AAV9-Control)或Pur-α(Flag-AAV9-Pur-α)的腺相關病毒制劑微注射到APP/PS1小鼠海馬中,觀察Pur-α對AD病理的影響。立體定向注射兩個月后,海馬區出現明顯的綠色熒光和約42 kDa的Flag表達,表明有效的信號轉導(圖5A-C)。值得注意的是,在Pur-α過表達的大腦中,circCwc27的表達沒有變化(圖5D)。與對照組相比,過表達Pur-α可顯著減少APP/PS1小鼠海馬區Aβ沉積和促炎細胞因子(圖5E和F)。微注射Flag-AAV9-Pur-α在很大程度上保護APP/PS1小鼠的記憶形成嚴重缺陷(圖5G-I)。綜上所述,這些結果表明Pur-α可以減少Aβ沉積,挽救空間記憶損傷。

圖5. Pur-α減少Aβ沉積,防止AD認知能力下降
7. CircCwc27通過與Pur-α結合調控AD基因的轉錄
對微注射LV-sh-circCon和LV-sh-circCwc27的APP/PS1小鼠海馬區進行了RNA測序,鑒定出339個差異表達基因(圖6A)。此外,學習和記憶基因富集顯著上調(圖6B-D)。在APP/PS1小鼠和AD患者中,大部分circCwc27調控的基因表達都發生了改變(圖6E和F)。ChIP-qPCR驗證了Pur-α直接結合到由circCwc27控制的AD異常基因的啟動子上(圖6G)。通過敲除circCwc27,Pur-α與這些基因啟動子的結合降低被逆轉(圖6H)。總之,circCwc27通過與Pur-α結合,減少了Pur-α對AD相關基因啟動子的招募。

圖6. CircCwc27通過與Pur-α結合調控AD基因的轉錄
結論:
總之,作者的研究結果表明,circRNA-蛋白相互作用的重要功能結果,即circCwc27通過與調控蛋白Pur-α結合,可能在AD發病過程中發揮關鍵作用,并代表了一個具有臨床轉化潛力的AD治療靶點。






