m6A修飾通過肝星狀細胞自噬信號通路調控鐵死亡
肝纖維化是一種復雜的生理和病理生理狀況,與瘢痕形成機制有關。細胞外基質的沉積是肝纖維化的核心事件,肌成纖維細胞基質主要由活化的 HSC 產生。今天我們來講一篇關于m6A修飾調控鐵死亡的文章,文章題名為:N6-methyladenosine modification regulates ferroptosis through autophagysignaling pathway in hepatic stellate cells,發表于Redox Biology期刊(IF=11.79)
m6A 修飾在HSC鐵死亡期間上調
Erastin、Sorafenib和RSL3處理明顯抑制了大鼠 (HSC-T6)、人 (HSC-LX2) HSC細胞,但鐵死亡抑制劑(ferrostatin- 1) 而不是壞死性凋亡抑制劑 (necrostatin-1) 和凋亡抑制劑 (ZVAD-FMK) 完全挽救了細胞生長抑制。erastin、Sorafenib 和RSL3 治療還顯著顯著增加了細胞內MDA和鐵水平,降低了谷胱甘肽水平和脂質ROS積累。是ferrostain-1,而不是 necrostatin-1 和 ZVAD-FMK,削弱了HSC 鐵死亡。總的來說,這些結果充分證實了erastin、sorafenib和RSL3可以在體外觸發HSC ferroptosis。
m6A RNA甲基化定量測定和斑點印跡顯示,在用Sorafenib、erastin 和 RSL3 處理后,HSC細胞m6A 修飾水平顯著增加。與其他甲基轉移酶相比,METTL4 的蛋白質和mRNA表達顯著上調。FTO在HSC鐵死亡中顯著下調。這些發現表明m6A修飾增加是由于HSC鐵死亡期間METTL4和FTO的失調。
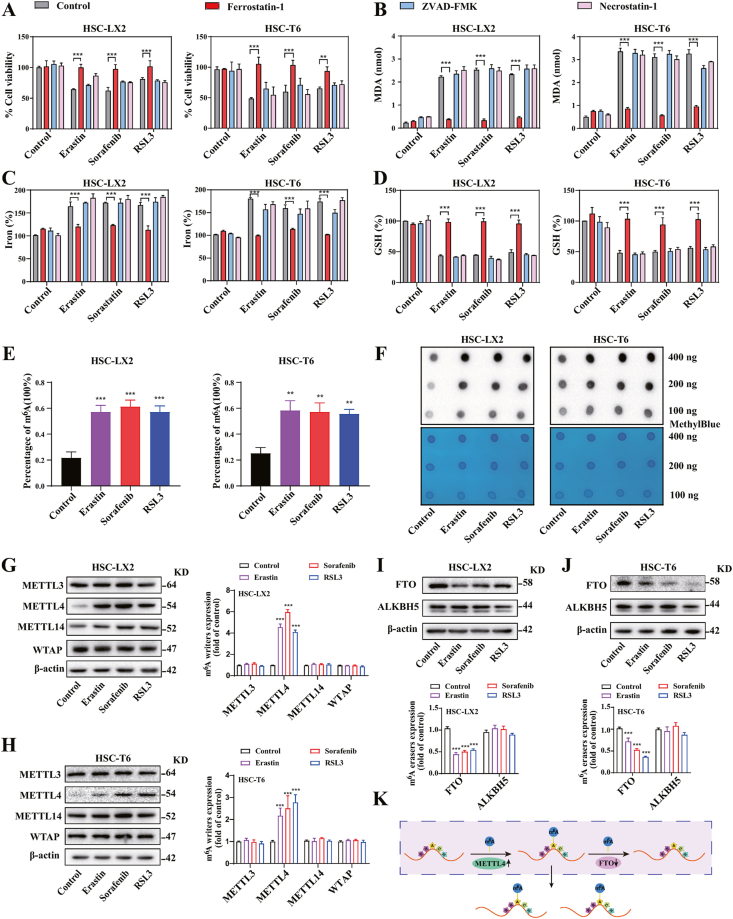
抑制m6A修飾賦予HSC鐵死亡的抗性
m6A RNA甲基化定量分析證實,METTL4敲低和FTO過表達都可以降低Erastin誘導的HSC-LX2中m6A修飾的上調。METTL4敲低和FTO過表達顯著消除了erastin和sorafenib處理對HSC-LX2和HSC-T6細胞的生長抑制。METTL4敲低和FTO過表達明顯破壞了erastin和sorafenib誘導的細胞內鐵、MDA和ROS水平,提升了谷胱甘肽水平。在FTO過表達條件下,liproxstatin-1和ferrostain-1 在內的鐵死亡抑制劑顯著逆轉了erastin 誘導的生長抑制。透射電子顯微鏡分析證實,erastin 處理大大減少了線粒體并減少了脊的數量,而 FTO 質粒完全消除了鐵死亡細胞的典型變化。這些數據表明,鐵死亡誘導劑處理對m6A修飾的上調可能有助于 HSC 鐵死亡,但不會導致壞死性凋亡和細胞凋亡。
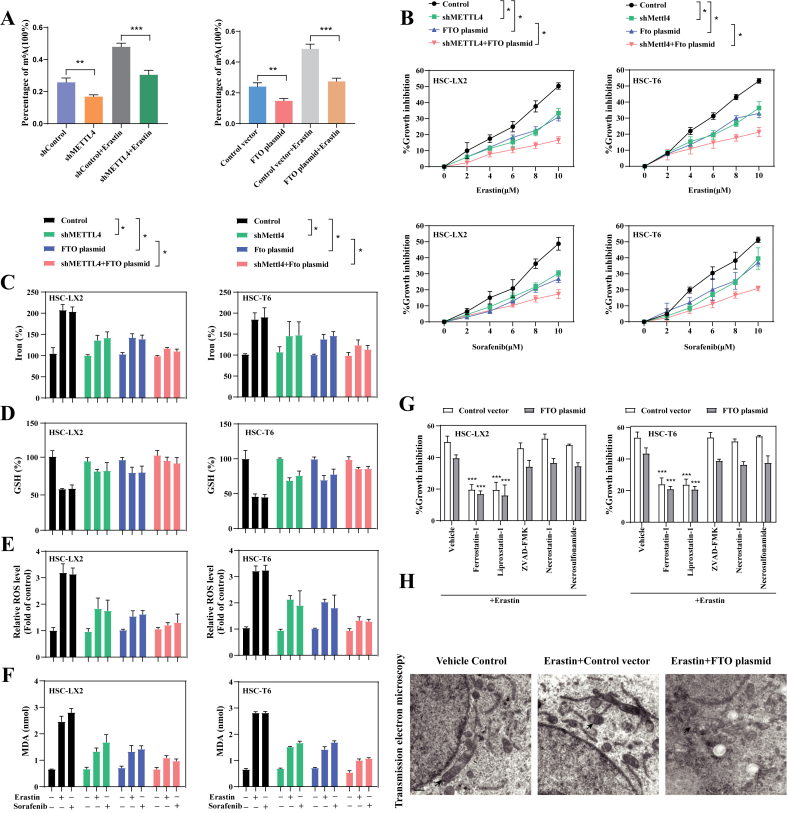
通過m6A修飾抑制減少鐵死亡與自噬失活有關
進行了 RNA 測序 (RNA-seq),以進一步探索m6A修飾促進 HSC 鐵死亡的分子機制。在 FTO 過表達的HSC-LX2細胞中,424個mRNA顯著增加,而317個 mRNAs明顯減少。這其中包含一些鐵死亡相關基因,例如 SLC7A11、SLC3A2、GPX4。KEGG)分析和 GO 分析充分表明,HSC鐵死亡過程中自噬信號可能受到m6A修飾的調節。我們發現自噬信號傳導中的關鍵靶基因 BECN1 的表達在 FTO 過表達后顯著降低。m6A RNA免疫沉淀 (MeRIP) qPCR 顯示,在HSC鐵死亡中,BECN1中m6A修飾的水平增加,但在ATG3、ATG4A、ATG5、ATG7、ATG9A、ATG12和ATG16L1中沒有增加。METTL4敲低和FTO過表達顯著降低了BECN1的蛋白質表達,而其他自噬相關基因沒有大的差異。METTL4敲低和FTO過表達介導的m6A降低有效抑制erastin 誘導的HSC中LC3-I向LC3-II 的轉化。熒光圖片顯示m6A降低抑制了erastin 誘導的自噬流。透射電子顯微鏡檢測進一步證實FTO質粒對m6A修飾的下調減少了HSC鐵死亡中的自噬囊泡。這些數據表明 m 6 A 修飾誘導鐵死亡與自噬激活有關。
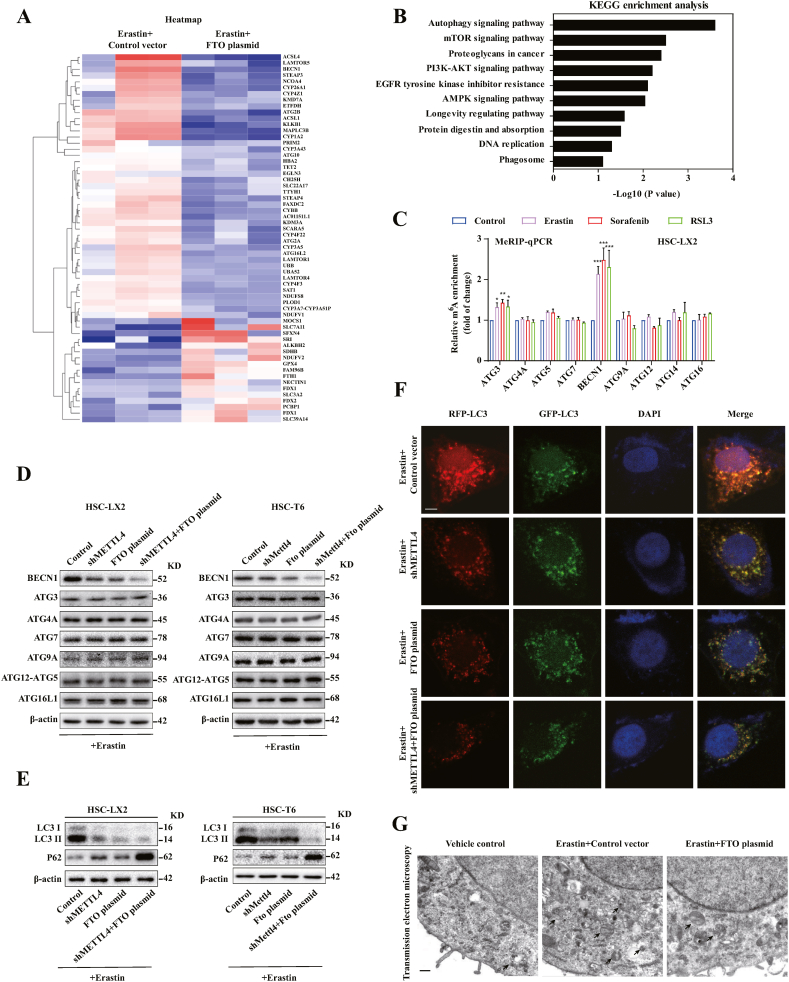
BECN1誘導自噬損害m6A修飾抑制賦予的HSC鐵死亡抗性
BECN1過表達在HSC鐵死亡過程中完全削弱了m6A修飾抑制誘導的BECN1下調。BECN1過表達恢復了自噬體的產生和自噬通量。在存在 m 6 A 修飾還原的情況下。Erastin 和sorafenib誘導的生長抑制被 FTO過表達和 METTL4 敲低破壞,而BECN1過表達在HSC鐵死亡期間顯著促進生長抑制。erastin和sorafenib治療在HSC中METTL4敲低或FTO過表達處理完全消除了鐵的積累、MDA、谷胱甘肽耗竭和脂質 ROS 積累。然而,BECN1過表達,抑制m6A 修飾并未顯著削弱鐵死亡事件。這些發現表明 BECN1過表達激活自噬削弱了抑制m6A修飾對HSC鐵死亡的抵抗力。

YTHDF1通過識別m6A結合位點促進BECN1mRNA 穩定性和激活自噬
YTHDF1蛋白和mRNA在 HSC鐵死亡期間顯著上調。放射菌素D實驗顯示YTHDF1過表達后BECN1的mRNA半衰期較對照載體組延長。蛋白酶處理顯示YTHDF1過表達后BECN1的蛋白質半衰期沒有顯著差異。RIP-PCR顯示YTHDF1能夠富集BECN1,RNA pulldown實驗顯示,YTHDF1 可以很容易地與 BECN1 CDS 而不是 BECN1 的3'-UTR和5'-UTR轉錄本相互作用。MeRIP qPCR 還顯示m6A修飾在BECN1 CDS中顯著富集。轉染了BECN1 CDS的HSC-LX2 細胞中的熒光素酶活性顯著增加。BECN1 mRNA 序列的CDS中的兩個m6A修飾位點序列。實驗顯示實BECN1-CDS-Mut2破壞了 YTHDF1 和 BECN1 mRNA 的結合,而不是 BECN1-CDS-WT和BECN1-CDS-Mut1。RNA穩定性分析表明,YTHDF1質粒延長了BECN1-CDS-WT mRNA和BECN1-CDS-Mut1 mRNA的半衰期,但沒有延長BECN1-CDS-Mut2 mRNA的半衰期。此外,蛋白質印跡結果還表明BECN1-CDS-Mut2 明顯破壞了erastin 誘導的 BECN1 蛋白上調。這些數據表明YTHDF1過表達通過與A1276的m6A結合位點CDS區域的結合來促進BECN1 mRNA 的穩定性。

m6A修飾的HSC特異性抑制損害erastin誘導小鼠肝纖維化中HSC鐵死亡
肉眼觀察肝纖維化模型組與對照組相比纖維化病理改變,而erastin治療減輕了CCl 4誘導的肝纖維化。用VA-Lip-Mettl4-shRNA、VA-Lip-Fto-質粒和VA-Lip-Ythdf1-shRNA預處理完全破壞了erastin對肝纖維化的改善。蘇木精和伊紅 (H&E) 染色、馬森染色和天狼星紅染色表明,erastin 處理顯著減少了中央靜脈中的膠原沉積。VA-Lip-Mettl4-shRNA、VA-Lip-Fto-質粒和VA-Lip-Ythdf1-shRNA明顯逆轉了erastin對肝纖維化的影響。免疫組化染色顯示VA-Lip-Mettl4-shRNA、VA-Lip-Fto-質粒和VA-Lip-Ythdf1-shRNA完全消除了erastin對α-SMA表達的抑制作用。結果表明VA-Lip-Mettl4-shRNA、VA-Lip-Fto-質粒和VA-Lip-Ythdf1-shRNA完全消除了被erastin抑制的Acta2、Col1a1、Fn1和Des的mRNA表達。VA-Lip-Mettl4-shRNA、VA-Lip-Fto-質粒和 VA-Lip-Ythdf1-shRNA 顯著阻止了對 m 6 A 修飾的erastin 的上調。VA-Lip-Mettl4-shRNA、VA-Lip-Fto-質粒和VA-Lip-Ythdf1-shRNA通過erastin處理阻斷了自噬的激活,其特征是Becn1和Map1lc3b表達降低,Sqstm1和Fth1表達增加。VA-Lip-Mettl4-shRNA、VA-Lip-Fto-質粒和 VA-Lip-Ythdf1-shRNA對 m 6 A 修飾的抑制完全損害了以 Ptgs2為特征的鐵死亡、氧化還原活性鐵還原和 MDA 消除。這些結果支持了以下假設:鼠肝纖維化中的 HSC 特異性 m 6 A 修飾抑制損害了erastin誘導的HSC鐵死亡。

索拉非尼單藥治療的人類 HSC中m6A修飾上調、促進自噬和鐵死亡
為了在臨床上評估m6A修飾的潛在機制,分析了10名接受索拉非尼單藥治療的肝硬化并發HCC患者的部分肝切除標本和10名未接受任何治療的肝硬化患者的肝活檢標本。然后,根據先前的報道,使用激光捕獲顯微切割從收集的肝組織中分離出原代HSC。與之前的研究結果一致,與未經處理的肝活檢樣本相比,索拉非尼治療的肝切除樣本中纖維化標志物 ACTA2、COL1A1 和 FN1 的 mRNA 水平顯著降低。正如預期的那樣,PCR分析顯示METTL4和YTHDF1 的表達上調,但 FTO 的表達在索拉非尼單藥治療樣本中下調。m 6定量分析表明,與未處理的對照相比,用索拉非尼處理的原代 HSC中 m 6 A 修飾水平顯著增加。此外,索拉非尼治療可能會上調人 HSC 中鐵蛋白吞噬標志物 BECN1 和 MAP1LC3B 的水平,并下調鐵蛋白吞噬底物 SQSTM1 和 FTH1 的水平。重要的是,索拉非尼治療增加了原代 HSC 中鐵死亡標志物 PTGS2 的表達,以及包括氧化還原活性鐵超載、脂質過氧化和 GSH 缺失在內的鐵死亡事件。綜上所述,這些發現表明索拉非尼單一療法有助于上調 m 6 A 修飾、激活自噬和誘導來自纖維化患者的人類 HSC 中的鐵死亡。







