外泌體circSHKBP1與胃癌進(jìn)展間關(guān)系大揭秘
circRNAs(circRNAs)在多種癌癥的發(fā)生發(fā)展中起著重要的調(diào)控作用。然而,circRNAs在胃癌(GC)中的生物學(xué)功能及其分子機(jī)制尚不清楚。今天小編為大家?guī)戆l(fā)表于“molecular cancer”上的文章“Exosomal circSHKBP1 promotes gastric cancer progression via regulating the miR-582-3p/HUR/VEGF axis and suppressing HSP90 degradation”,為大家詳細(xì)介紹circSHKBP1在胃癌發(fā)展中的機(jī)制。

在本研究中,通過RNA測(cè)序鑒定差異表達(dá)的環(huán)狀RNA。通過一系列體外和體內(nèi)實(shí)驗(yàn)研究了circSHKBP1在GC中的生物學(xué)功能。通過實(shí)時(shí)定量PCR和RNA原位雜交檢測(cè)circSHKBP1的表達(dá),通過western blot、pull down、RNA免疫沉淀、熒光素酶檢測(cè)和挽救實(shí)驗(yàn)證實(shí)了circSHKBP1的分子機(jī)制。最后,使用小鼠異種移植和生物發(fā)光成像檢查體內(nèi)circSHKBP1的臨床相關(guān)性。我們的研究結(jié)果表明,外泌體circSHKBP1調(diào)控miR-582-3p/HUR/VEGF通路,抑制HSP90降解,并促進(jìn)GC進(jìn)展。
結(jié) 果:
1.circSHKBP1作為GC生物標(biāo)志物的鑒定
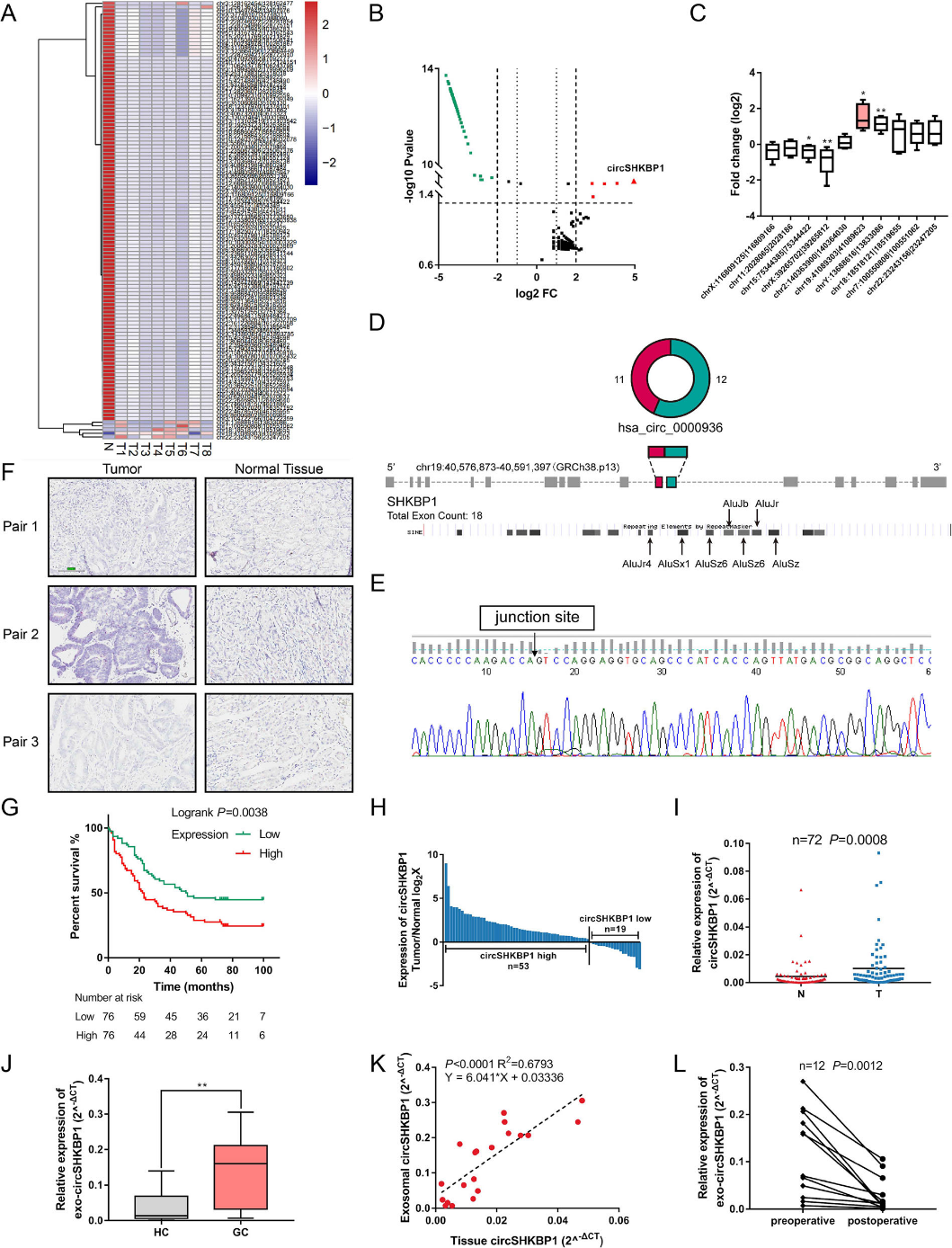
通過對(duì)GC組織和匹配的相鄰正常組織的RNA測(cè)序分析,我們共鑒定出1445個(gè)不同的circRNA。共有119個(gè)circRNAs在癌組織和正常組織中有差異表達(dá),其中5個(gè)circRNAs上調(diào),114個(gè)circRNAs下調(diào)(圖1a和b)。然后,我們進(jìn)一步通過qRT-PCR分析,發(fā)現(xiàn)circSHKBP1是GC中表達(dá)差異最大的circRNA(圖1c)。
CircSHKBP1來源于蛋白編碼位點(diǎn)SHKBP1,在人類組織中廣泛表達(dá)。CircSHKBP1是由SHKBP1基因的第11和第12外顯子與兩側(cè)內(nèi)含子中的幾個(gè)Alu元件反向剪接而產(chǎn)生的(圖1d)。我們?cè)O(shè)計(jì)了跨越連接位點(diǎn)的聚合引物,通過Sanger測(cè)序證實(shí)了逆轉(zhuǎn)錄產(chǎn)物(圖1e)。然后,我們分析了circSHKBP1在配對(duì)GC組織和正常組織中的表達(dá)情況。qRT-PCR分析顯示,與正常組織相比,在GC組織中circSHKBP1表達(dá)上調(diào)(圖1h,i)。此外,ISH檢測(cè)顯示,circSHKBP1在GC組織中的豐度遠(yuǎn)高于匹配的正常組織(圖1f),并且circSHKBP1的表達(dá)與TNM晚期、血管侵犯和不良預(yù)后相關(guān)(圖1g)。接著,鑒定了來自血清的外泌體中的circSHKBP1。與預(yù)期的一樣,來自血清外泌體的circSHKBP1在GC患者中比健康對(duì)照組更豐富(圖1j)。此外,血清外泌體中的circSHKBP1水平與胃癌患者腫瘤中的水平一致,約為腫瘤中的水平的6倍(圖1k)。我們還研究了胃癌切除術(shù)前后血清中circSHKBP1的表達(dá),發(fā)現(xiàn)腫瘤切除后circSHKBP1的表達(dá)急劇下降,表明胃癌組織是外泌體circSHKBP1的來源(圖1l)。這些結(jié)果表明circSHKBP1是一種來自GC組織的上調(diào)的circRNA,circSHKBP1的高表達(dá)與TNM晚期及胃癌不良預(yù)后相關(guān)。
2.CircSHKBP1在體外促進(jìn)GC細(xì)胞的增殖、遷移和侵襲
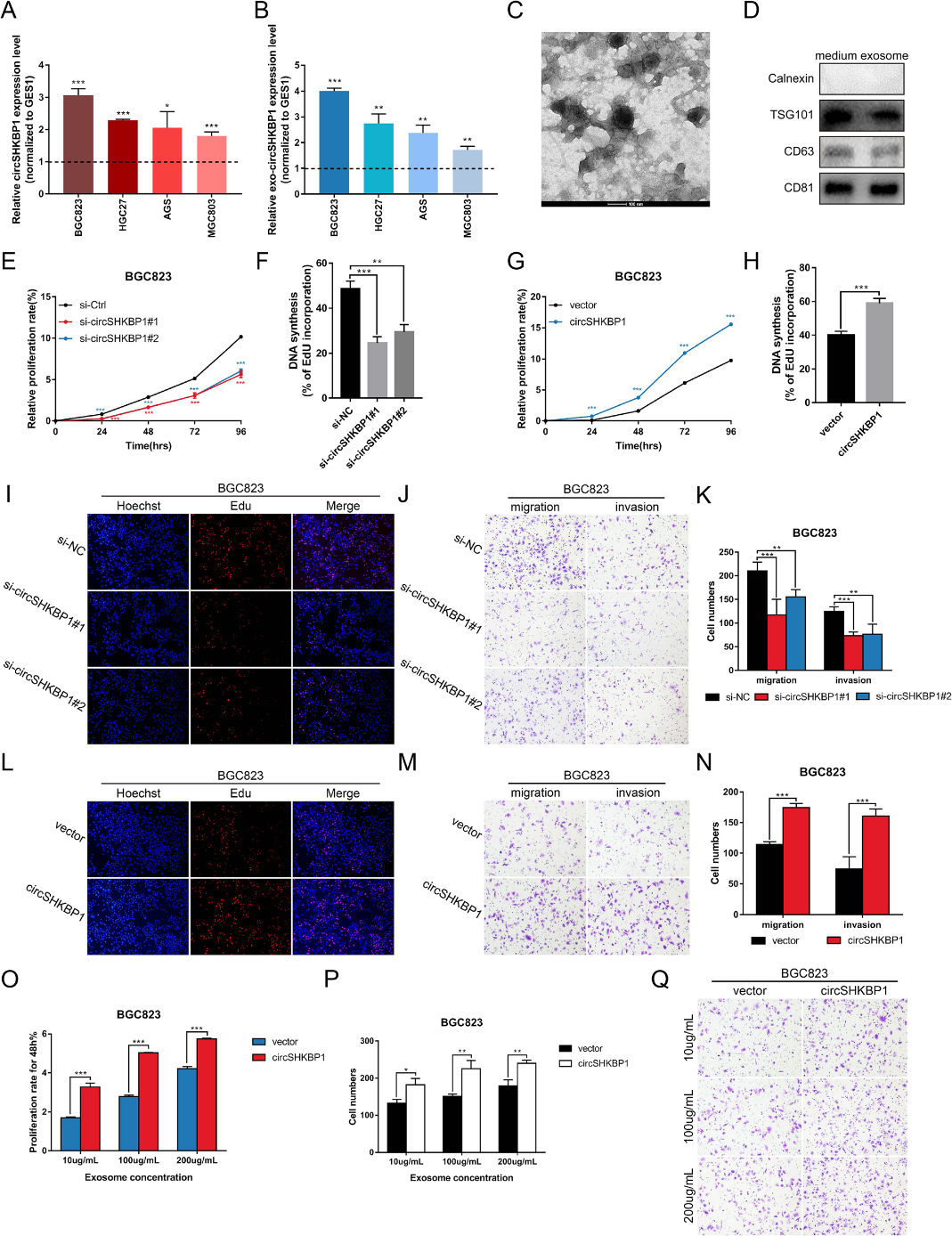
為了研究circSHKBP1是否影響胃癌細(xì)胞的生物學(xué)過程,我們首先分析了circSHKBP1在人胃癌細(xì)胞系和胃正常上皮細(xì)胞系GES1中的表達(dá)情況。與GES1細(xì)胞相比,circSHKBP1在4種GC細(xì)胞系中均過表達(dá),在BGC823和HGC27的表達(dá)尤為明顯(圖2a)。與GES1細(xì)胞相比,外泌體circSHKBP1在GC細(xì)胞系中也過表達(dá)(圖2b-d)。因此,我們?cè)诮酉聛淼姆治鲋惺褂昧薆GC823和HGC27細(xì)胞。
接著,我們對(duì)circSHKBP1進(jìn)行了干擾。 CCK8和EdU檢測(cè)顯示,沉默circSHKBP1顯著抑制了GC細(xì)胞的增殖(圖2e,f,i)。Transwell檢測(cè)顯示,沉默circSHKBP1抑制了GC細(xì)胞的遷移和侵襲能力(圖2j,k)。然而,過表達(dá)circSHKBP1增加了GC細(xì)胞的增殖、遷移和侵襲(圖2g,h,l-n)。
最后,我們從轉(zhuǎn)染circSHKBP1質(zhì)粒的BGC823和HGC27細(xì)胞的培養(yǎng)液中提取外泌體,并與不同濃度未處理的GC細(xì)胞共培養(yǎng)。正如預(yù)期的那樣,外泌體circSHKBP1的過表達(dá)也影響了GC細(xì)胞的增殖、遷移和侵襲,促進(jìn)了惡性細(xì)胞表型(圖2o-q)。這些結(jié)果表明circSHKBP1促進(jìn)了GC細(xì)胞的生長和轉(zhuǎn)移。
3.CircSHKBP1作為miR-582-3p的海綿
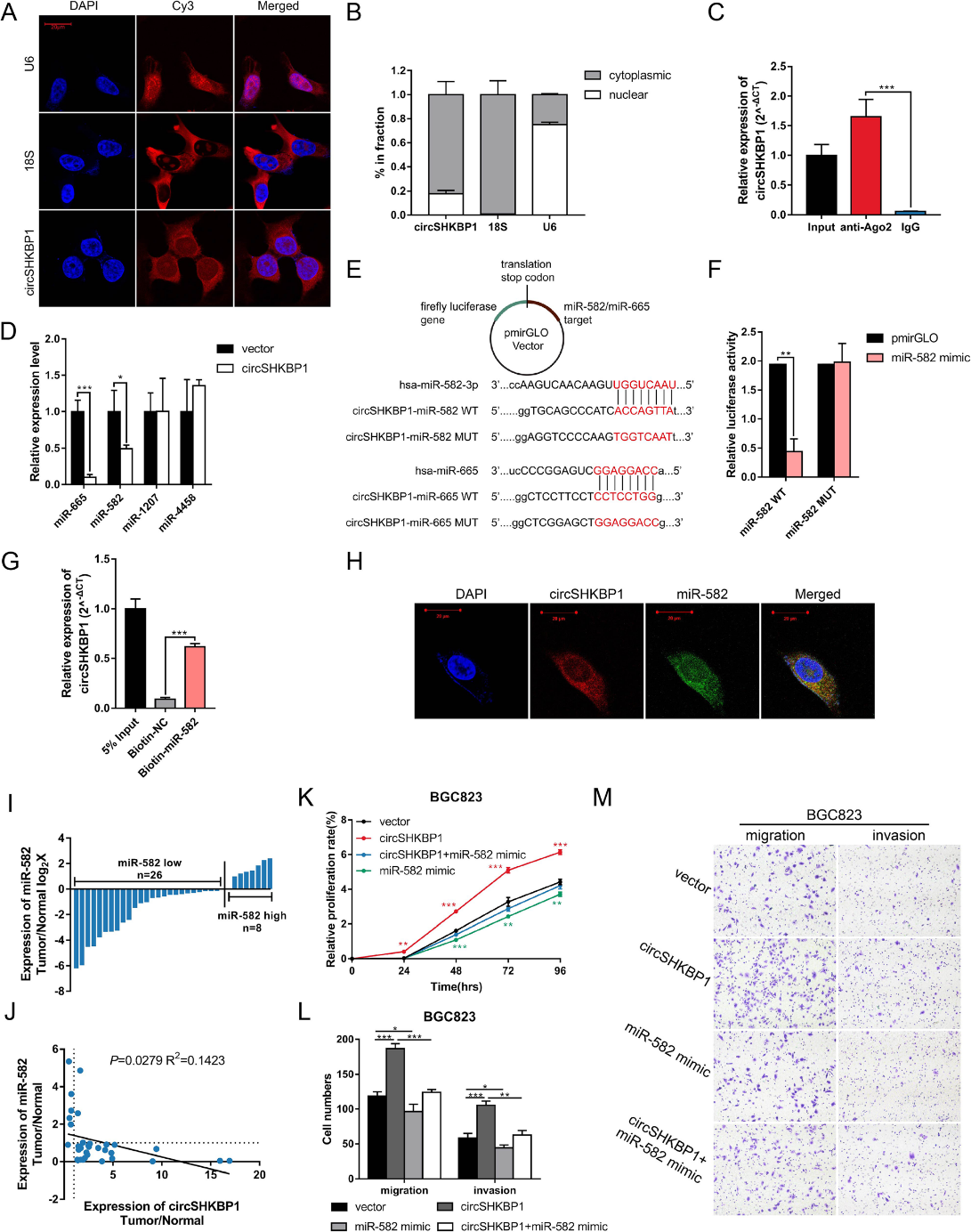
為了研究circSHKBP1在GC細(xì)胞中的作用機(jī)制,我們首先確認(rèn)了它在GC細(xì)胞中的定位。FISH分析和qRT-PCR分析表明,circSHKBP1優(yōu)先定位于GC細(xì)胞的細(xì)胞質(zhì)內(nèi)(圖3a和b)。鑒于circRNAs作為miRNA海綿已被廣泛研究,我們接下來研究了circSHKBP1的miRNA結(jié)合能力。我們進(jìn)行RIP檢測(cè),觀察到在BGC823細(xì)胞中內(nèi)源性circSHKBP1下拉,被特異性地富集(圖3c),這表明circSHKBP1起著miRNA海綿的作用。四個(gè)可能的miRNAs(miR-582-3p,miR-665,miR-1207和miR-4458)被預(yù)測(cè)。我們檢測(cè)到這些miRNAs在circSHKBP1過表達(dá)的GC細(xì)胞中的表達(dá),發(fā)現(xiàn)miR-582-3p和miR-665下調(diào)(圖3d)。為了驗(yàn)證miR-582-3p/miR-665和circSHKBP1之間的直接相互作用,我們進(jìn)行了雙熒光素酶報(bào)告基因檢測(cè)(圖3e)。結(jié)果表明,與miR NC模擬物相比,miR-582-3p模擬物使circSHKBP1-miR-582-3p組的相對(duì)熒光素酶活性降低,而circSHKBP1-miR-582-3p突變體組的熒光素酶活性沒有變化(圖3f)。我們還進(jìn)行了生物素標(biāo)記的RNA下拉試驗(yàn),證實(shí)了circSHKBP1和miR-582-3p的吸收(圖3g)。此外,F(xiàn)ISH實(shí)驗(yàn)證實(shí)了circSHKBP1和miR-582-3p在細(xì)胞質(zhì)中共定位(圖3h)。qRT-PCR顯示,GC腫瘤中miR-582-3p水平低于配對(duì)正常組織,miR-582-3p與circSHKBP1的表達(dá)呈負(fù)相關(guān)(圖3i和j)。
最后我們證實(shí)miR-582-3p的生物學(xué)功能。CCK8和Transwell分析表明miR-582-3p模擬物抑制了GC細(xì)胞的增殖、遷移和侵襲,而circSHKBP1的過表達(dá)消除了這種對(duì)GC細(xì)胞發(fā)育的抑制作用(圖3k-m)。
4.CircSHKBP1通過上調(diào)HUR促進(jìn)VEGF的翻譯
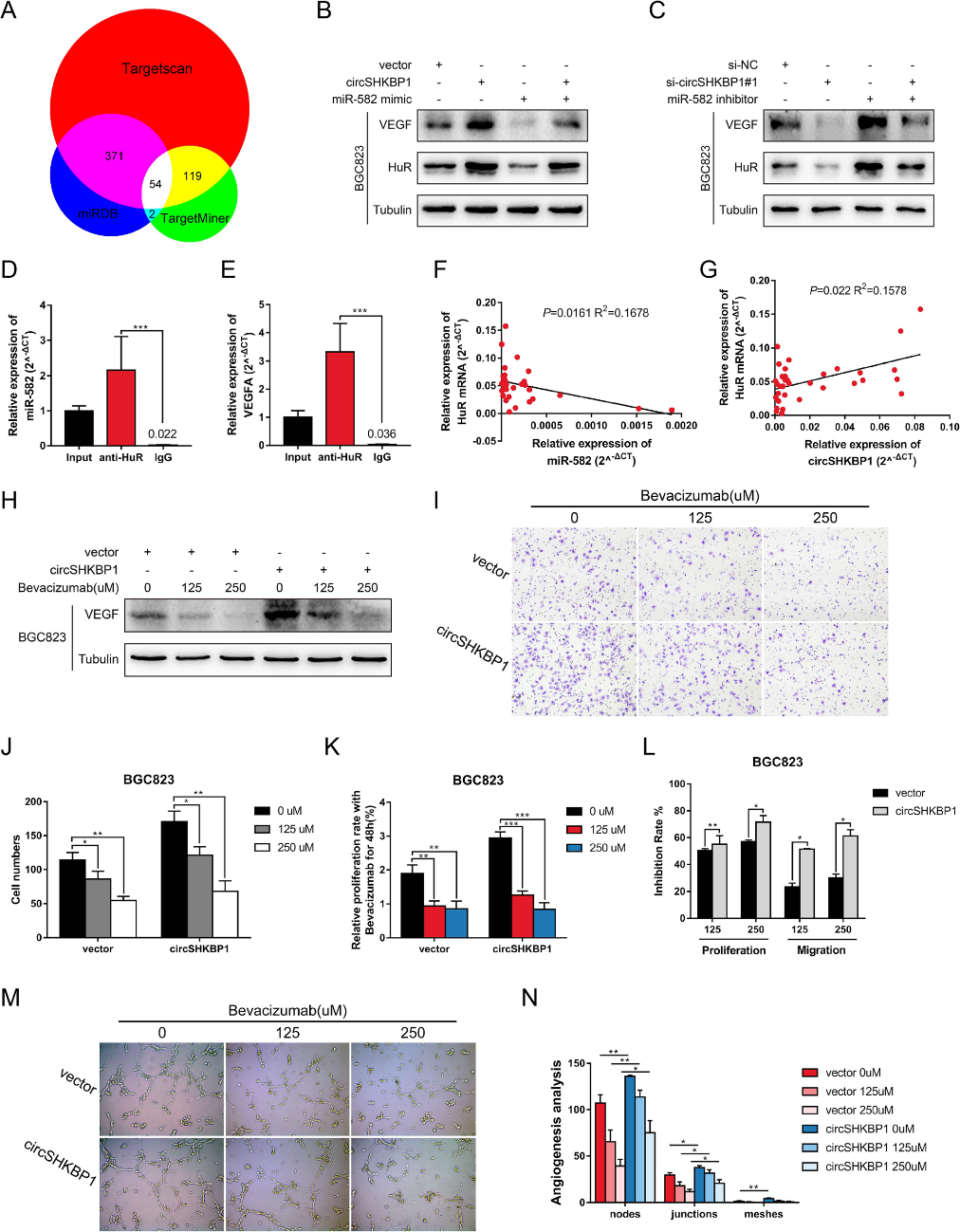
通過生物信息學(xué)分析網(wǎng)站,我們發(fā)現(xiàn)了54個(gè)miR-582-3p候選靶蛋白(圖4a),其中HUR和EIF2S1被報(bào)告為VEGF信號(hào)通路的一部分。血管內(nèi)皮生長因子(VEGF)是促進(jìn)內(nèi)皮細(xì)胞增殖的重要因素之一,因此我們對(duì)VEGF途徑進(jìn)行了深入研究。WB分析顯示,過表達(dá)circSHKBP1增加了HUR和VEGF的水平(圖4b)。此外,miR582-3p模擬物降低了HUR和VEGF蛋白水平(圖4b)。同樣,沉默circSHKBP1降低了HUR和VEGF的水平,miR-582-3p抑制劑恢復(fù)了這些水平(圖4c)。與對(duì)照組相比,HUR的RIP顯示VEGF mRNA和miR-582-3p顯著富集(圖4d和e),進(jìn)一步證實(shí)HUR是miR-582-3p的靶點(diǎn),HUR直接與VEGF mRNA結(jié)合。我們還檢測(cè)了GC組織中HUR mRNA的水平,發(fā)現(xiàn)HUR的表達(dá)與miR-582-3p呈負(fù)相關(guān),而與CircSHKBP1呈正相關(guān)(圖4f和g)。我們用不同濃度的貝伐單抗處理CircSHKBP1過表達(dá)的GC細(xì)胞,以確定CircSHKBP1是否通過VEGF加速腫瘤進(jìn)展。WB分析顯示,VEGF水平隨著貝伐單抗?jié)舛鹊脑黾佣档停▓D4h)。貝伐單抗以濃度依賴的方式降低GC細(xì)胞增殖和遷移能力(圖4i-k),并且CircSHKBP1過表達(dá)細(xì)胞的抑制率遠(yuǎn)高于對(duì)照組(圖4l)。試管形成試驗(yàn)進(jìn)一步證實(shí),CircSHKBP1促進(jìn)VEGF分泌并誘導(dǎo)血管生成,貝伐單抗可抑制這一點(diǎn)(圖4m和n)。
5.CircSHKBP1直接與HSP90相互作用并抑制其降解
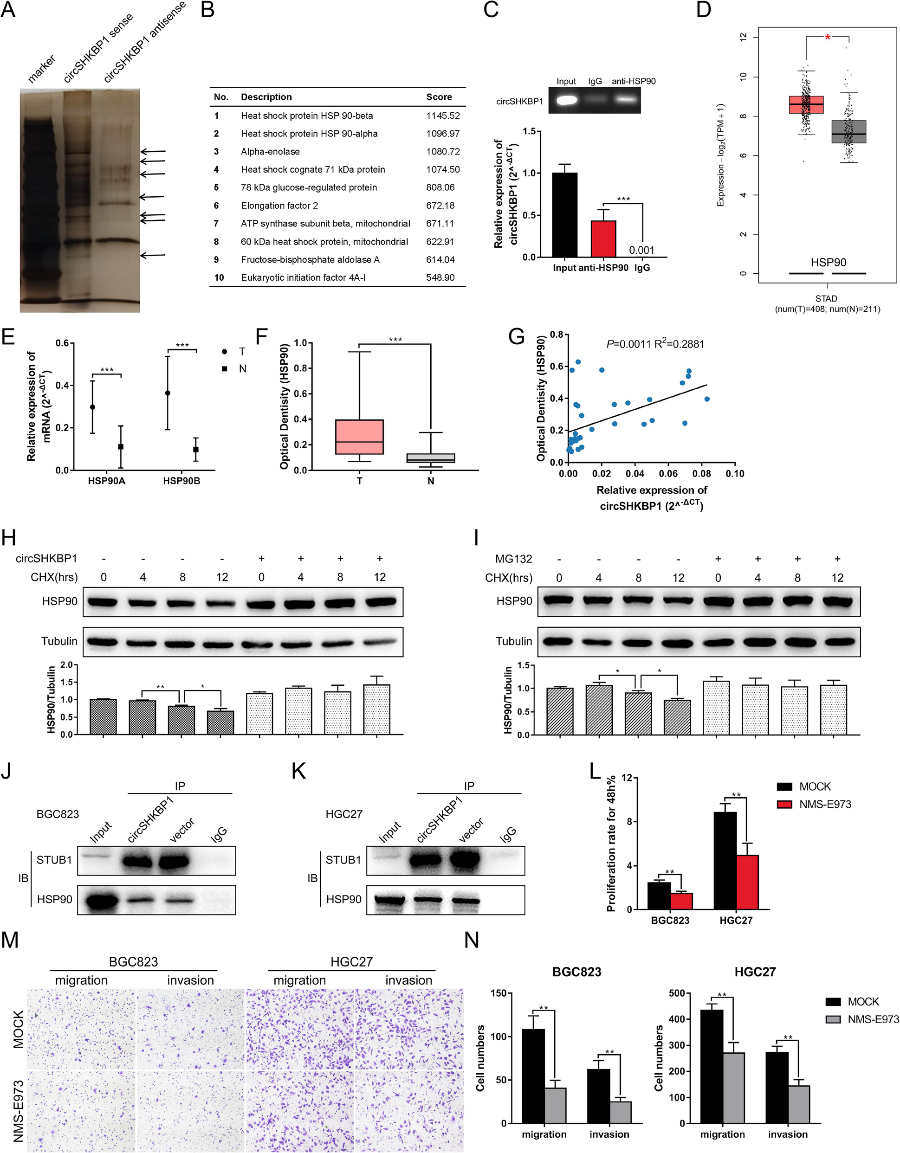
我們?cè)O(shè)計(jì)了一種特異性生物素標(biāo)記的CircSHKBP1探針,用于HGC27細(xì)胞的RNA下拉分析。銀染結(jié)果顯示,與對(duì)照組相比,CircSHKBP1過表達(dá)的GC細(xì)胞中多個(gè)蛋白條帶的富集(圖5a)。蛋白質(zhì)質(zhì)譜分析用于鑒定差異表達(dá)的蛋白質(zhì)。HSP90β 和HSP90α排名前兩位,都是HSP90的亞型。RIP分析顯示,與IgG相比,抗HSP90抗體拉下了豐富的CircSHKBP1(圖5c),證實(shí)了CirchHKBP1和HSP90之間的直接相互作用。通過TCGA分析,HSP90在GC中上調(diào)(圖5d)。采用qRT-PCR方法檢測(cè)組織中HSP90 mRNA水平,ELISA法檢測(cè)組織中HSP90蛋白水平。結(jié)果表明,與正常組織相比,GC腫瘤中HSP90 mRNA和蛋白均上調(diào)(圖5e,f)。考慮到circRNA和蛋白質(zhì)之間的相互作用,我們分析了HSP90蛋白的表達(dá)與CircSHKBP1之間的關(guān)系,發(fā)現(xiàn)它們是正相關(guān)的(圖5g)。WB顯示CircSHKBP1的過表達(dá)略微增加了HSP90的總量(圖5e)。然而,用CHX抑制蛋白質(zhì)合成后,當(dāng)CircSHKBP1過表達(dá)時(shí),HSP90的降解被顯著抑制(圖5h)。E3泛素連接酶STUB1已被證明泛素化HSP90。因此,我們使用蛋白酶體抑制劑MG132來阻斷HSP90的泛素化。在MG132處理下,HSP90的降解減慢(圖5i)。IP分析顯示過表達(dá)CircSHKBP1降低了與HSP90結(jié)合的STUB1數(shù)量(圖5j和k)。此外,HSP90的選擇性抑制劑NMS-E973在體外損害了CircSHKBP1circhkbp1的促腫瘤功能(圖5l-n)。這些結(jié)果表明,circSHKBP1直接與HSP90結(jié)合,通過STUB1抑制HSP90的泛素化,從而促進(jìn)GC的發(fā)育。
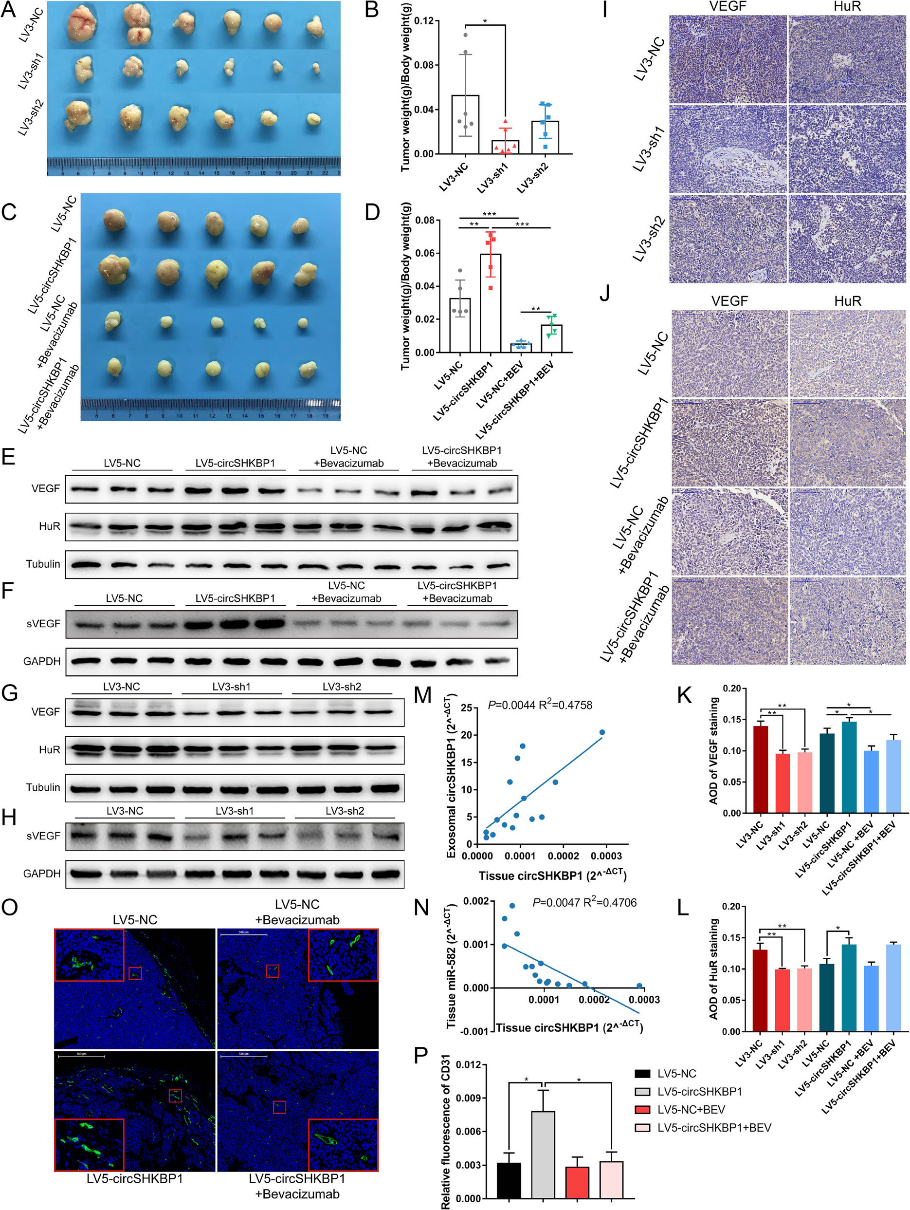
6.CircSHKBP1促進(jìn)體內(nèi)GC生長
我們構(gòu)建了沉默和過表達(dá)CircSHKBP1的細(xì)胞株。將LV3-sh1、LV3-sh2和LV3-NC細(xì)胞接種于裸鼠右大腿皮下。結(jié)果表明,在腫瘤體積和腫瘤重量/體重比方面,LV3-sh1細(xì)胞的腫瘤明顯小于LV3-NC細(xì)胞(圖6a,b)。另外,我們將LV5- CircSHKBP1和LV5-NC細(xì)胞接種于裸鼠右大腿皮下,每組半數(shù)小鼠每周給予貝伐單抗兩次。經(jīng)過21天的監(jiān)測(cè),來自LV5- CircSHKBP1細(xì)胞的腫瘤比來自LV5-NC細(xì)胞的腫瘤體積更大、重量更重。此外,貝伐單抗顯著抑制腫瘤生長(圖6c,d)。通過對(duì)小鼠血清和腫瘤中的蛋白質(zhì)進(jìn)行WB分析,我們發(fā)現(xiàn),與LV3-NC組相比,LV3-sh1和LV3-sh2組的HUR和VEGF水平降低(圖6g和h);與LV5-NC組相比,LV5- CircSHKBP1組的HUR和VEGF增加,而VEGF被貝伐單抗抑制(圖6e和f)。腫瘤組織中HUR和VEGF的IHC結(jié)果相似(圖6i-l)。接下來,我們從血清外泌體和腫瘤中提取總RNA,用qRT-PCR方法研究circSHKBP1。結(jié)果表明,外泌體circSHKBP1的表達(dá)與癌組織CircSHKBP1的表達(dá)呈線性關(guān)系(圖6m)。我們還測(cè)量了腫瘤中miR-582-3p的水平,發(fā)現(xiàn)它與circSHKBP1的水平呈負(fù)相關(guān)(圖6n)。此外,CD31在腫瘤中的IF顯示LV5-circSHKBP1組的熒光區(qū)明顯大于對(duì)照組(圖6o和p),表明血管生成活躍。
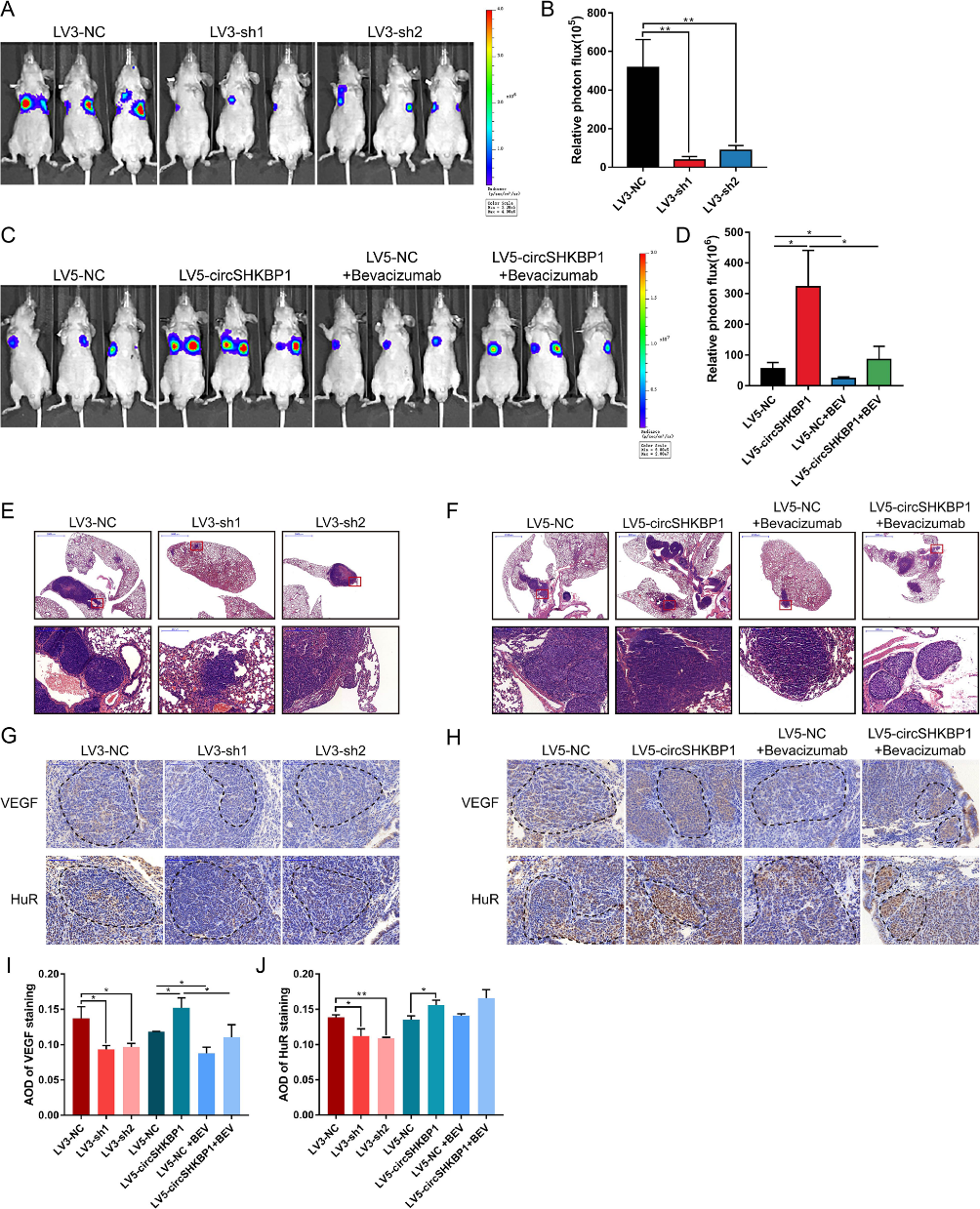
7.CircSHKBP1促進(jìn)體內(nèi)GC轉(zhuǎn)移
為了研究circSHKBP1在體內(nèi)的轉(zhuǎn)移潛能,我們首先用熒光素酶質(zhì)粒穩(wěn)定轉(zhuǎn)染上述5種細(xì)胞系,然后通過尾靜脈注射到裸鼠體內(nèi)。LV5- circSHKBP1和LV5-NC組半數(shù)小鼠每周給藥兩次貝伐單抗。結(jié)果表明,circSHKBP1基因敲除可顯著減少肺轉(zhuǎn)移病灶的數(shù)量和大小(圖7a-c)。此外,IHC顯示circSHKBP1敲低導(dǎo)致GC肺轉(zhuǎn)移灶HUR和VEGF染色明顯減少(圖7d)。生物發(fā)光成像和HE染色顯示,circSHKBP1的過表達(dá)加重了肺轉(zhuǎn)移病灶,HUR和VEGF染色增加(圖7e-h)。貝伐單抗也能抑制circSHKBP1的轉(zhuǎn)移潛能。
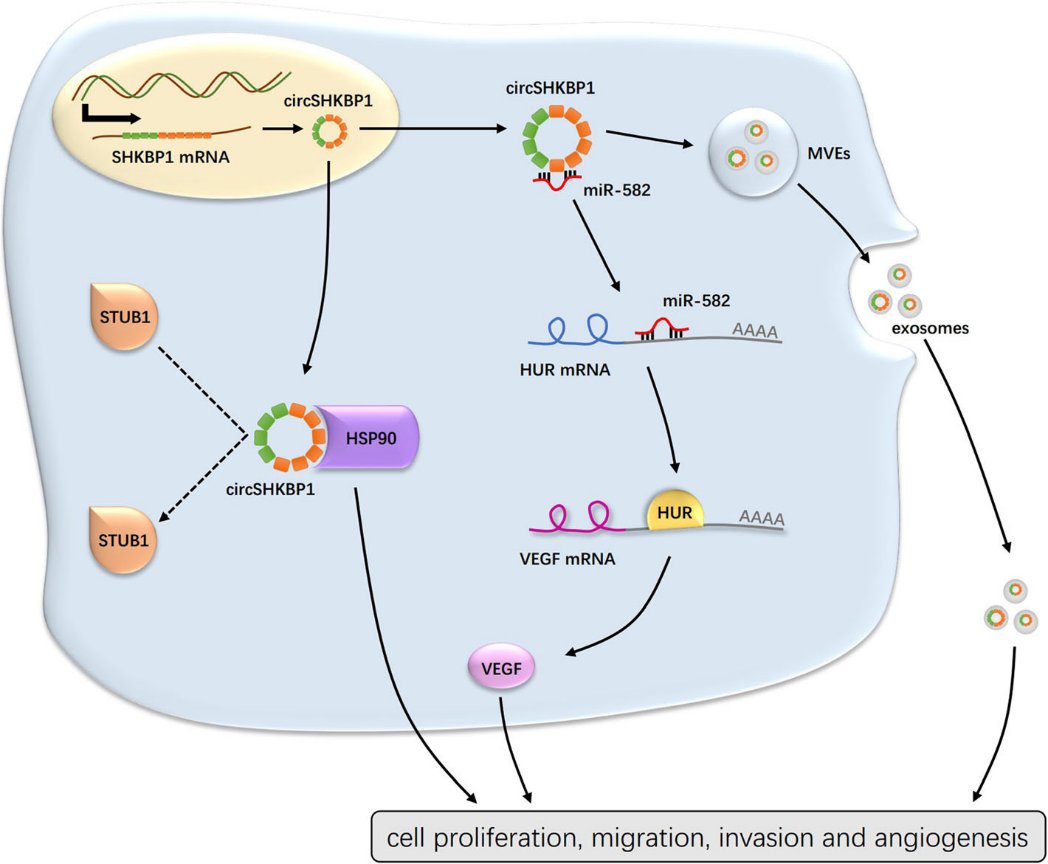
結(jié) 論:
總之,我們證明circSHKBP1在GC患者中上調(diào),并與TNM分期、血管侵犯和不良預(yù)后有關(guān)。以circSHKBP1為靶點(diǎn)的血清外泌體液體活檢可以幫助診斷和預(yù)測(cè)胃癌的進(jìn)展。CircSHKBP1通過吸收miR-582-3p來上調(diào)HUR和VEGF,并通過與STUB1競爭來誘導(dǎo)HSP90,從而促進(jìn)GC進(jìn)程。因此circSHKBP1被認(rèn)為是一種很有前途的胃癌診斷和預(yù)后的生物標(biāo)志物,是胃癌治療的潛在治療靶點(diǎn)。






