Tip 60是如何來操控BMAL 1乙酰化的呢?
乙酰化就是將有機化合物分子中的氮、氧、碳原子上引入乙酰基CH3CO-的反應,最常見的是組蛋白乙酰化。常用氯乙酰和Acetic Anhydride等作為乙酰化劑。
該研究于今年8月份,德國馬克斯·普朗克生物物理化學研究所在《Elife》雜志上發表,題為“Acetylation of BMAL1 by TIP 60 controls BRD4-P-TEFb recruitment to circadian promoters”。揭示了Tip 60對BMAL 1乙酰化的控制機制,并為Tip 60作為乙酰化反應的應用提供了理論基礎。
摘要:
許多生理過程都表現出由相互連接的激活和抑制元素組成的細胞時鐘驅動的晝夜節律。為了研究這種分子振蕩器的調節時間,我們結合了小鼠遺傳方法和關鍵晝夜節律蛋白相互作用和時鐘基因啟動子的相互作用分析。我們發現轉錄激活因子BRD4-PTEFb富集到含有E-box的晝夜節律啟動子。 在晝夜周期的激活階段期間,賴氨酸乙酰轉移酶TIP 60使轉錄激活因子BMAL1乙酰化,導致BRD4和P-TEFb暫停釋放因子的富集,隨后是晝夜節律的生產轉錄延伸。 我們提出BRD4-P-TEFb富集的啟動子是生物鐘周期中新的時間檢查點。
結果:
一、抑制CDK 9和BRD4消除了晝夜或者生理節律的振蕩
穩定表達時鐘驅動的熒光素酶報告基因Bmal1-LUC的同步成纖維細胞在26小時內持續表達。存在P-TEFb的CDK9亞基有效抑制劑flavopiridol(FP)的情況下,熒光素酶活性節律在高劑量時,節律完全喪失(圖1A)。生物鐘基因調控不僅發生在轉錄起始,還發生在Pol II暫停釋放和生產延伸的水平。用JQ1(選擇性BRD4抑制劑)處理Bmal1-LUC報告基因成纖維細胞以劑量依賴性方式抑制熒光素酶活性節律,引起周期延長(圖1B),還導致這些細胞中內源性Dbp表達節律的強烈抑制(圖1C)。在JQ1存在下,Dbp的轉錄起始位點(TSS)上BRD4和CDK9的富集顯著減少(圖1D)。在Dbp的3'末端,Pol II的Ser2磷酸化被強烈減少(圖1E),表明Pol II暫停釋放已被抑制。降低的Dbp表達可能是由于BMAL1水平較低。我們的JQ1抑制劑研究表明BRD4-P-TEFb被富集到含有E-box的時鐘控制基因Dbp中,隨后允許Pol II暫停釋放和轉錄延伸。因此,對于這種生物鐘控制的基因,Pol II暫停釋放可以作為其轉錄的重要調節步驟。
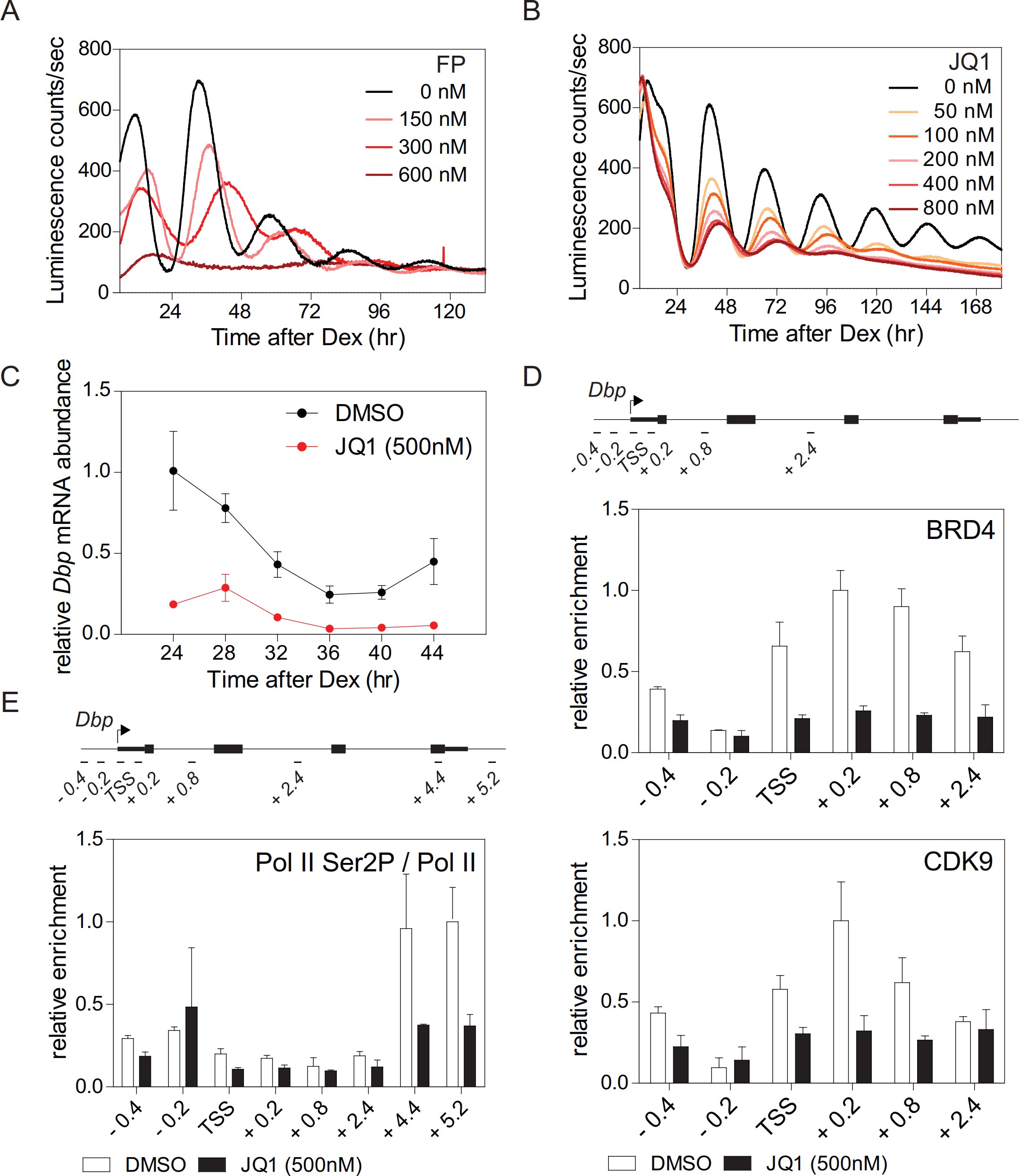
圖1.BRD 4控制時鐘基因的表達。
二、需要在賴氨酸538處乙酰化BMAL1以啟動晝夜節律的生產轉錄延伸
BRD4在暫停基因的啟動子上與轉錄因子/組蛋白的乙酰化賴氨酸結合。觀察到JQ1對細胞晝夜節律的強烈影響,提出了在BRD4靶標中存在核心時鐘組分的可能性,例如BMAL1,其在Lys538處被乙酰化可提供BRD4的結合位點。作者采用免疫沉淀實驗研究了含有工程化BMAL1K538R的對照成纖維細胞和成纖維細胞中檢查BRD4和CDK9與BMAL1的相互作用,結果表明在表達BMAL1K538R的細胞中,這種相互作用顯著降低(圖2A)。當野生型細胞經JQ1處理時,這種相互作用基本上受到抑制。 ChIP實驗證明BMAL1K538R突變細胞顯示BRD4和P-TEFb亞基CDK9向Dbp(圖2B)的TSS的富集減少。 此外,Ser2-磷酸化的Pol II的富集顯著降低(圖2B)。由于對照成纖維細胞和BMAL1K538R突變細胞均穩定表達時鐘驅動的熒光素酶報告基因,我們評估了K538R突變對發光節律的影響。在BMAL1K538R細胞中,幾乎沒有記錄三個克隆中任何一個的節律性熒光素酶報告基因表達(圖2C)。另外,在這些細胞中,內源性Dbp(圖2D) mRNA的峰表達顯著降低。BMAL1乙酰化可能另外促進轉錄起始,利于轉錄延伸而非起始是主要通過BMAL1的乙酰化調節的過程。因此,乙酰化的BMAL1將BRD4-P和TEFb富集到含有E-box的生物鐘基因,然后導致Pol II從其暫停狀態釋放,從而允許生產性延長。
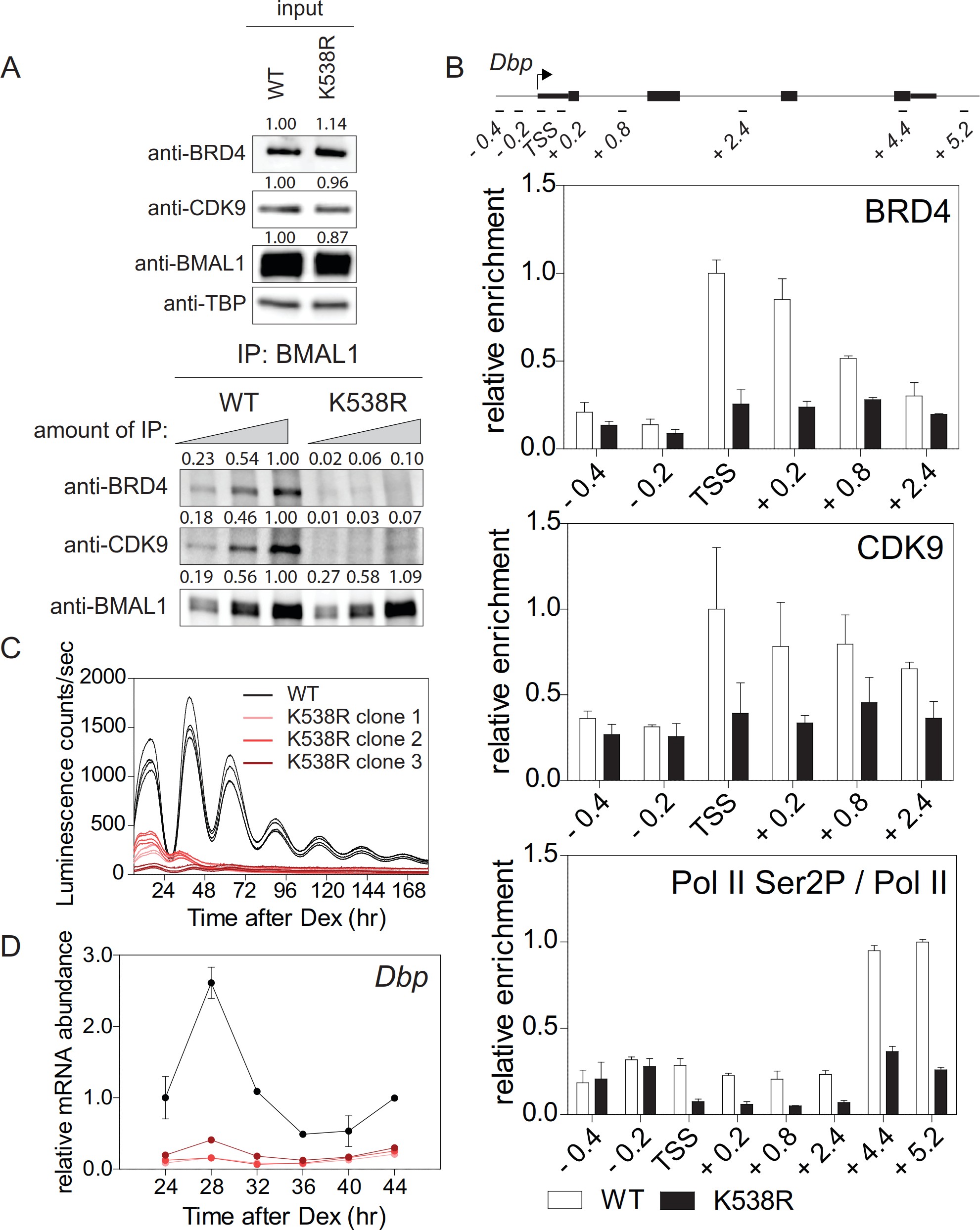
圖2.BMAL 1的Lys 538乙酰化對轉錄延伸至關重要。
三、TIP 60對于小鼠生物鐘的功能是必不可少的。
BMAL1乙酰化由CLOCK進行。研究發現在CLOCK缺陷的成纖維細胞中,BMAL1在Lys538處被乙酰化與野生型細胞中觀察到的相似程度(圖3A)。 CLOCKmutA不能使組蛋白H3和H4乙酰化,并且BMAL1的乙酰化活性大大降低。與對照相比,兩種CLOCK變體呈現出BMAL1乙酰化的最小增加(圖3B),存在CLOCK或CLOCKmutA時BMAL1乙酰化水平難以區分。總之,這些數據表明存在催化BMAL1乙酰化的替代乙酰轉移酶TIP 60,其與CLOCK-BMAL1共同純化并且乙酰化廣泛的轉錄因子。添加TIP 60,但不是酶促失活的TIP 60C369A; E403Q,強烈增強了BMAL1乙酰化(圖3B)。
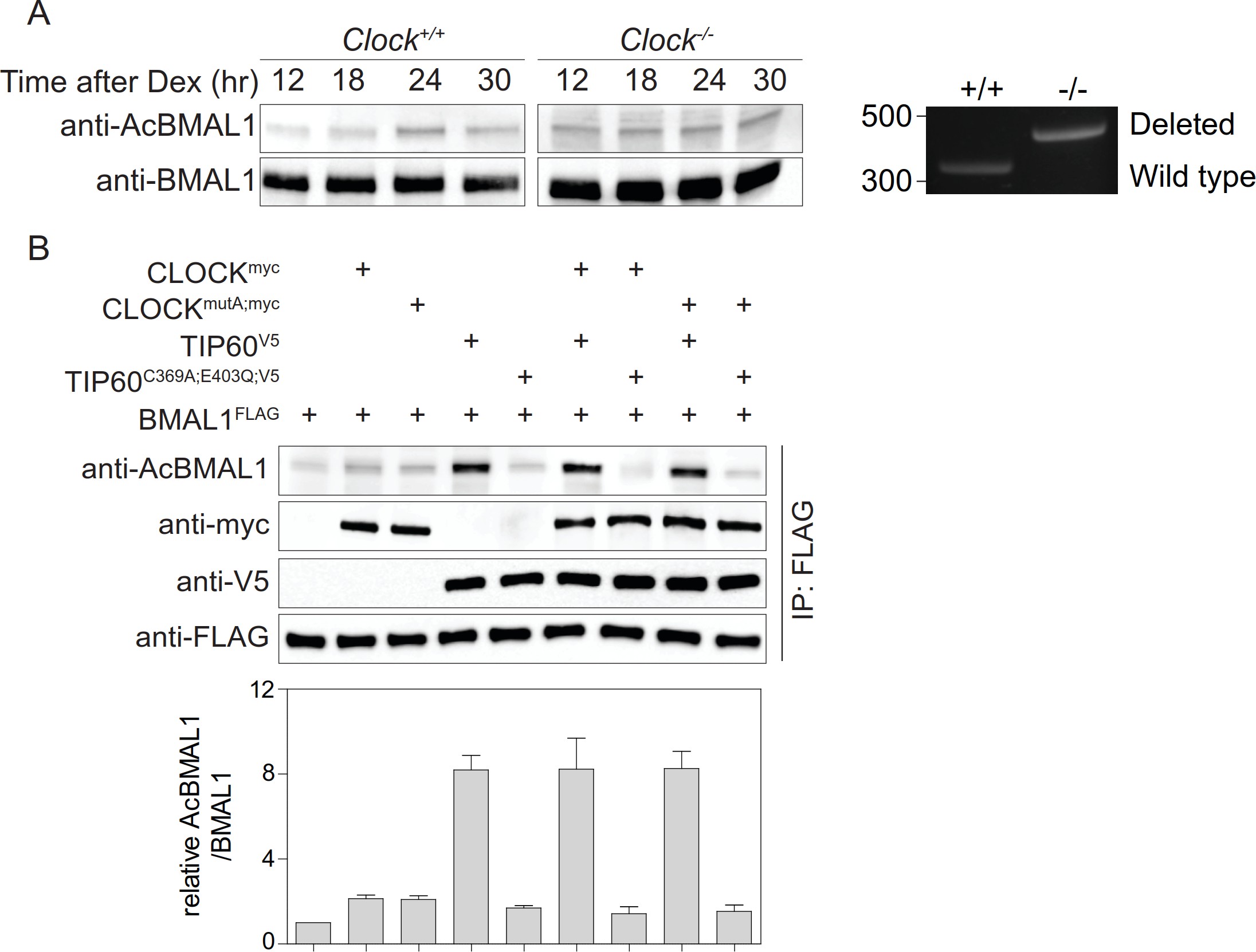
圖3.BMAL 1在缺乏時鐘的細胞中的乙酰化。
這種生物鐘新潛在調節器促使我們產生條件性Tip 60小鼠,以評估該酶的體內功能并用于體外研究分子鐘的成纖維細胞。Tip 60fl/- 攜帶Tip 60的一個條件和一個缺失等位基因的小鼠(圖4)與Syt10-CRE驅動小鼠交配。該驅動因子在SCN的有絲分裂后神經元中具有強烈活性,可以規避與TIP 60缺陷相關的細胞致死率。所有后代攜帶兩個拷貝的敲入Cre等位基因(Syt10Cre/Cre Tip 60fl /- )和一半攜帶一個拷貝的敲入Cre等位基因(Syt10Cre/+ Tip 60 fl/- )的小鼠在釋放后立即變得心律失常。恒定暗度(DD)(圖4A和B),Syt10Cre /+ Tip 60 fl/-小鼠的其余部分顯示更長(29%)或正常(21%)自由運行期。SCN中TIP 60的免疫組織化學染色顯示核信號,其在心律失常的Syt10Cre / + Tip 60 fl/- 小鼠中不存在(圖4C)。晝夜節律SCN中Per1,Dbp和Bmal1的表達模式受到嚴重抑制(圖4D),與這些動物中觀察到的行為心律失常一致。細胞融合足以誘導細胞周期靜止,從而繞過TIP 60在細胞周期調節中的作用。除管家基因之外,缺失導致熒光素酶報告基因的節律表達的顯著抑制和內源性時鐘基因的顯著降低的表達(圖4E和4F)。因此,刪除TIP 60功能對SCN體內和有絲分裂后MEF中的運動活性和時鐘基因的節律性表達具有重要影響。
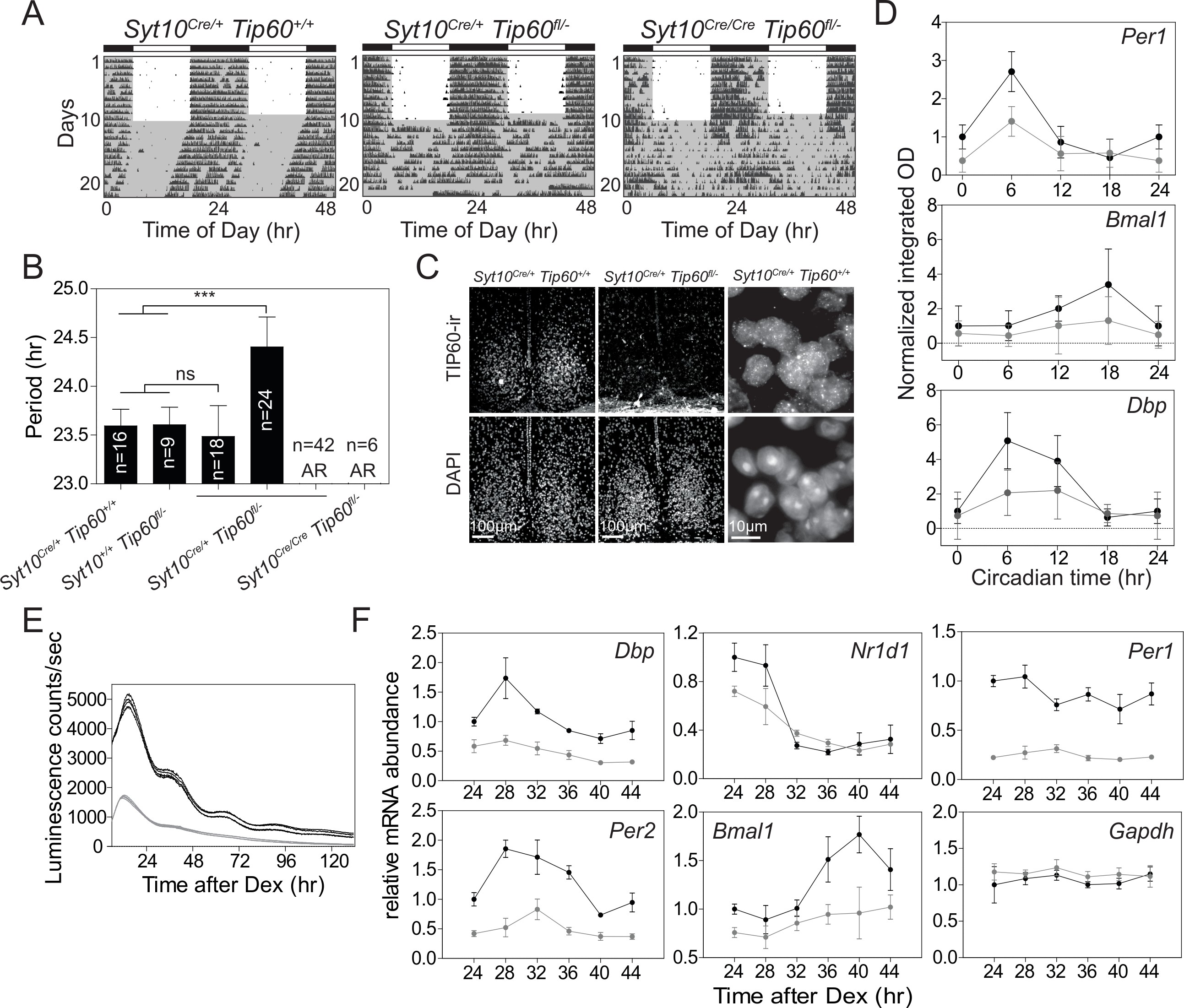
圖4.Tip 60-缺乏引起小鼠晝夜節律表型,并干擾SCN和MEFs中節律時鐘基因的表達。
四 、Tip 60乙酰化BMAL 1在賴氨酸538
小鼠嚴重的晝夜節律表型、Tip 60缺陷SCN和MEFs中時鐘基因表達的強烈變化以及共轉染實驗(圖3B)均表明BMAL1可能是Tip 60的直接基板。共轉染實驗顯示bmal 1的Lys 538以劑量依賴性的方式被Tip 60乙酰化,而缺乏乙酰轉移酶的Tip 60c369a;e403q導致類似模擬轉染細胞的BMAL 1基線乙酰化水平(圖3B;圖5A)。Lys 538似乎是Tip 60作為信號乙酰化的主要賴氨酸。 在BMAL1K538R和Tip 60共轉染細胞中,抗PAC-ack抗體明顯減少(圖5A)。Tip 60與野生型和BMAL1K538R共沉淀,表明兩者之間存在相互作用這兩種蛋白質(圖5A)。BMAL 1的乙酰化作用不影響這種相互作用。重組TIP 60GST乙酰化重組BMAL1GST在Lys 538(圖5B),在Tip 60缺陷MEFs中,內源性BMAL 1的Lys 538乙酰化明顯減少(圖5C)。 當內源性Tip 60被Bmal1-Luc報告細胞中的TIP 60C369A;E403Q替代時,內源性DBP的熒光素酶節律和mRNA節律被阻斷(圖5D和E)。總之,這些 數據提供強有力的證據表明BMAL1是TIP 60的底物。
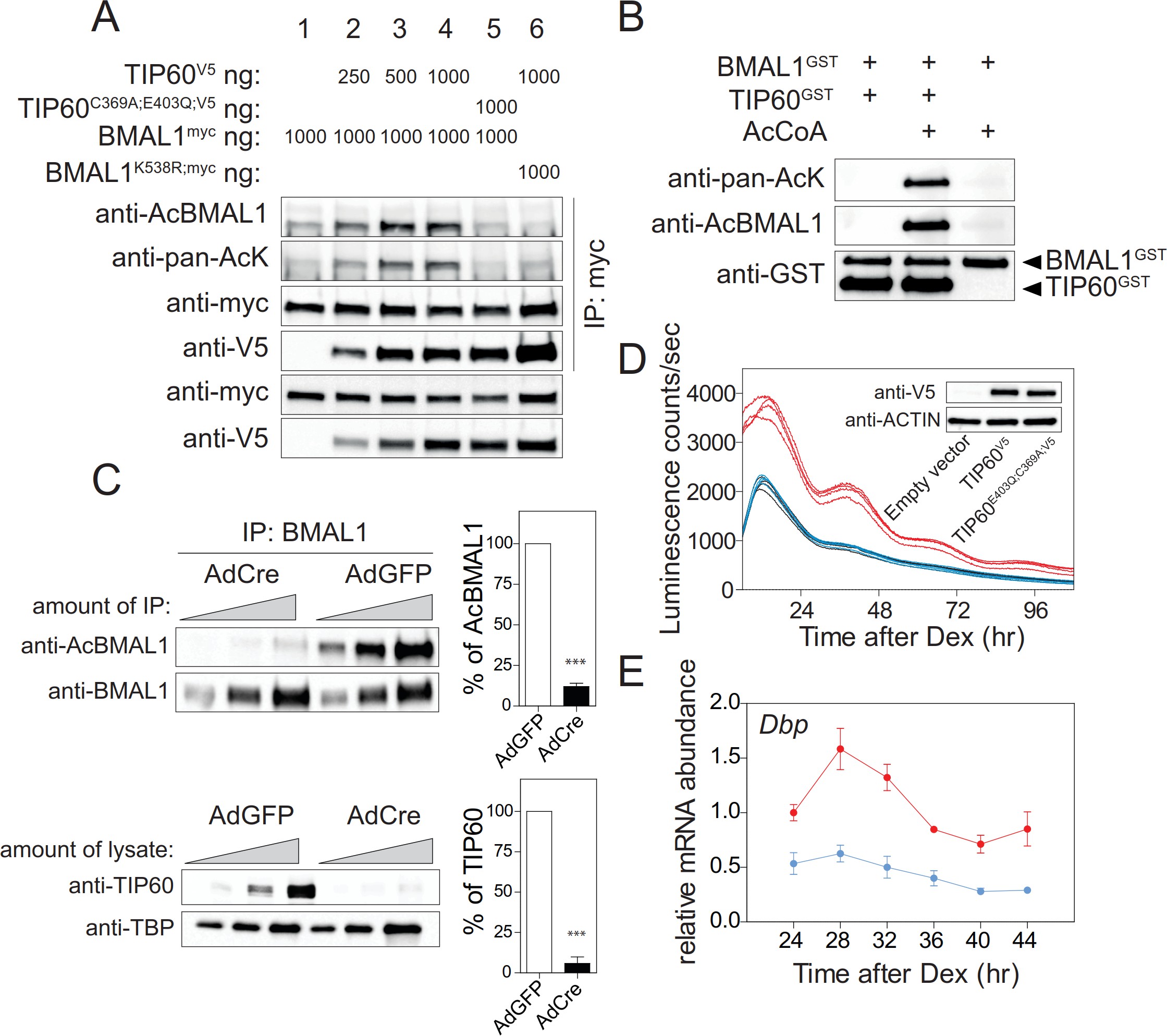
圖5.Tip 60乙酰化BMAL 1。
五、Tip 60控制晝夜節律轉錄本的產生延長
使用BRD 4和P-TEFb(圖2A和B)。此外,在BMAL1K538R細胞中,PolⅡSer2磷酸化(一種生產延長率的指標)明顯降低(圖2B)。因此,刪除Tip 60應該廢除BRD4-P-TEFb富集和POL II暫停發布。事實上,在融合的Tip 60缺陷的Dex同步纖維瘤中 TS,BMAL 1是低乙酰化的(圖5C和6A),BMAL 1和BRD 4(圖6A和B)以及BMAL 1和CDK 9(圖6C)之間的相互作用嚴重喪失。芯片實驗顯示 在DBP、PER 1和Nr1d1基因的tss上,BRD 4和CDK 9的富集量明顯減少,而Ser2磷酸化的POLⅡ占用率降低(圖6D)。
以上數據表明,BMAL 1的乙酰化在轉錄延伸中起著關鍵作用。Tip 60乙酰化BMAL 1,Tip 60缺失不應該影響轉錄起始。刪除TIP 60不影響TIFIEA富集到DBP、Per1和NR1D1基因的TSS。
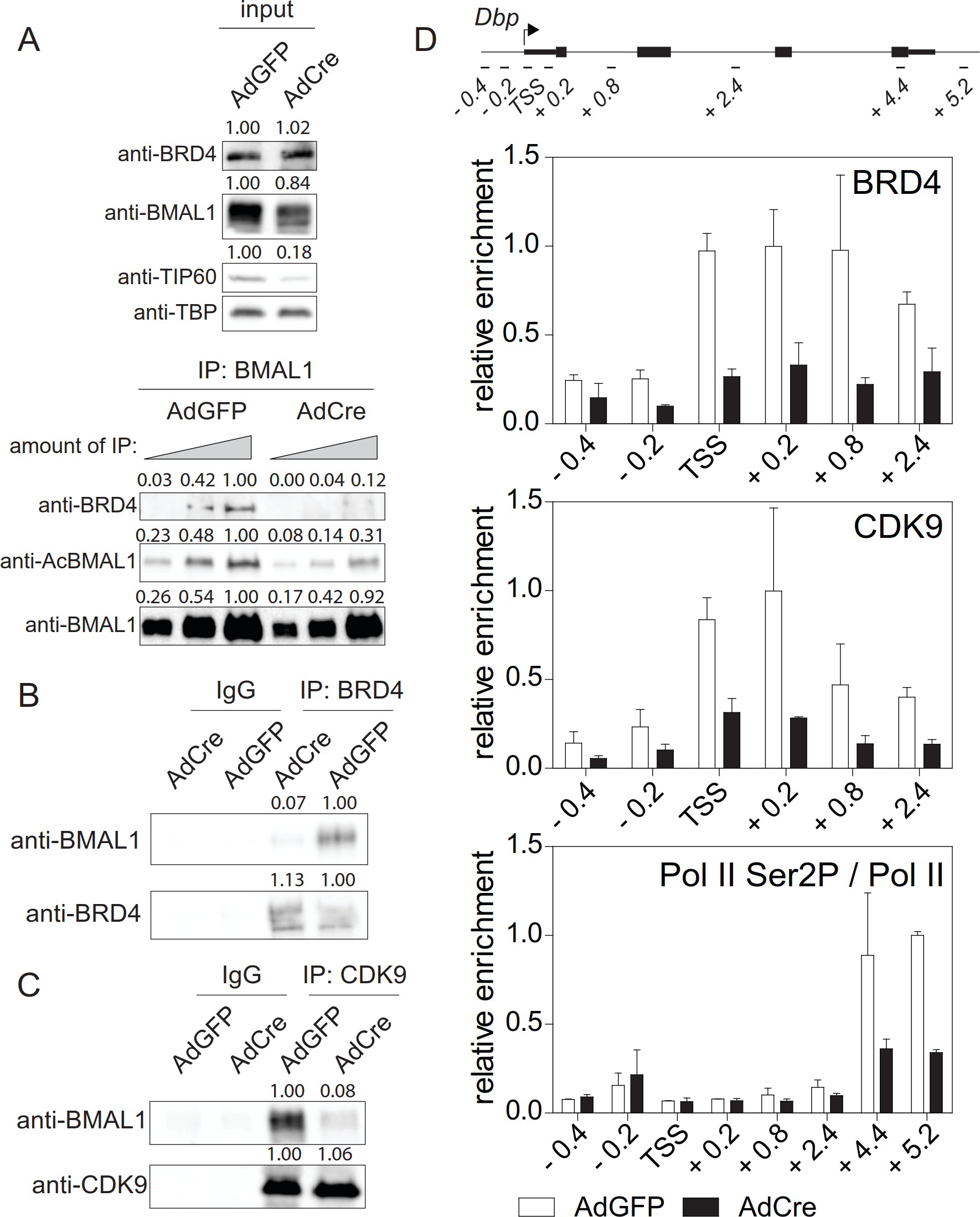
圖6. TIP 60控制生產延長率。
六 、晝夜節律轉錄體產生延長的節律性
我們的實驗證明TIP 60介導的BMAL1的乙酰化是生物鐘振蕩器的陽性肢體的必要元素。 TIP 60介導的BMAL1乙酰化導致BRD4和暫停釋放因子P-TEFb富集至時鐘基因TSS。反而允許CLOCK-BMAL1控制基因的生產性延長。在E-box控制的時鐘基因的啟動子的暫停釋放因子的時間占有情況中也應該看到正晝夜調節的正調節和負調節之間的平衡。在細胞同步后大約24小時,我們觀察到在Dbp,Per1和Nr1d1基因的啟動子處BMAL1和乙酰化BMAL1的最強富集(圖7A)。核提取物中乙酰化BMAL1的濃度在此時呈現最大值(圖7B)。BRD4的占據在靶基因啟動子處達到峰值(圖7A),并且Pol II的Ser2磷酸化顯示最大值(圖7A)。因此,Dbp,Per1和Nr1d1 mRNA的豐度在24和28小時之間達到峰值(圖7A)。總之,我們的數據顯示依賴于TIP 60的BRD4富集,Pol II暫停釋放和生產延長在晝夜周期中精確定時,并且以這種方式對生物鐘振蕩器施加時間控制。
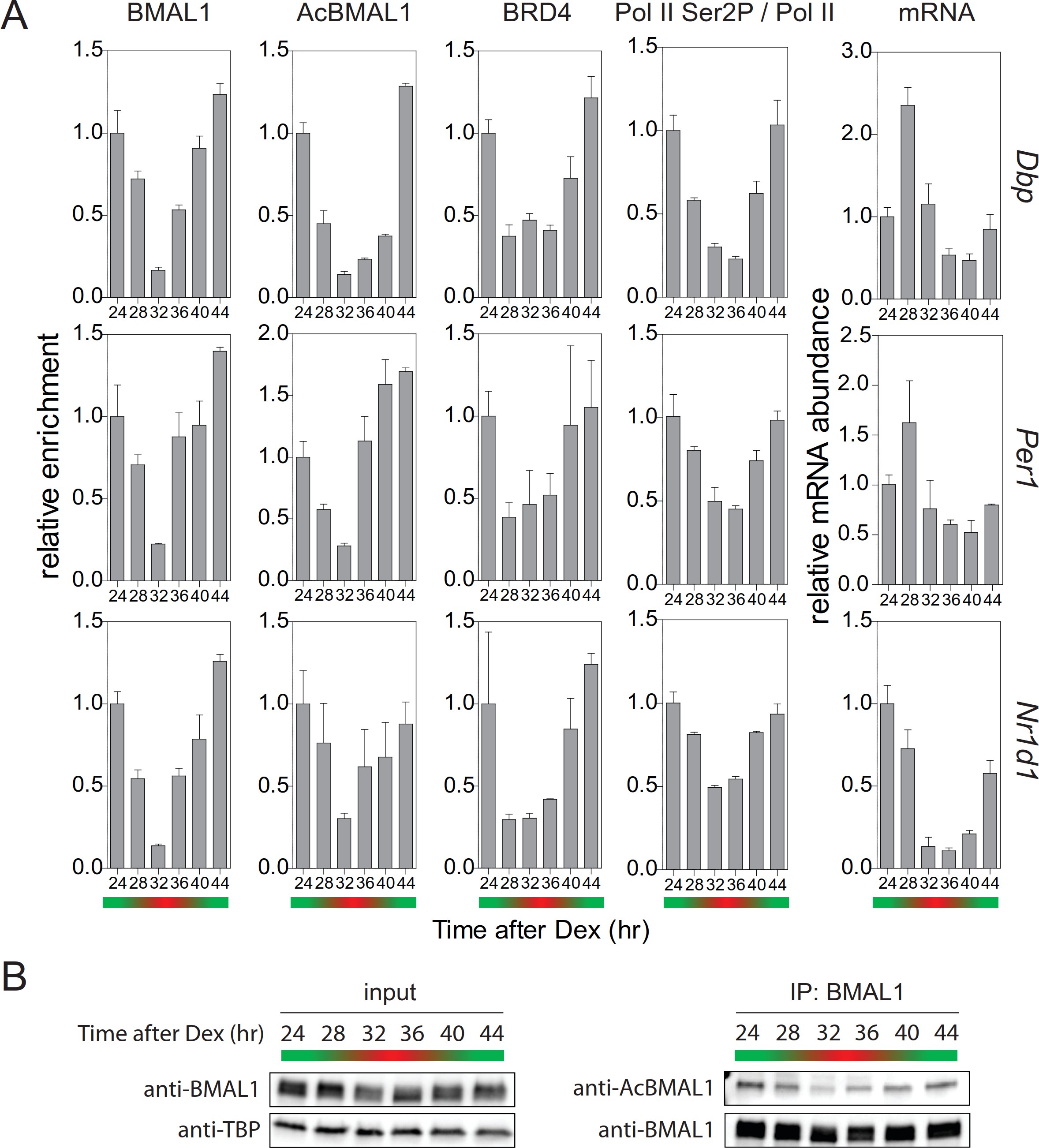
圖7.生產延長的有節奏的輪廓。
結論:
暫停釋放涉及到由Tip 60介導的BMAL 1的Lys 538的染色質乙酰化反應,Bmal1乙酰化允許向AcBMAL 1富集輔助激活劑BRD 4。BRD 4依次富集暫停釋放因子P -TEFb,其激酶亞基CDK 9然后磷酸化POLⅡ的Ser2,導致POLⅡ從停頓狀態釋放,從而使含有E-box的晝夜節律基因得以產生延長。






